磷酸川芎嗪温敏凝胶纤毛毒性的研究
2013-12-17朱艳华刘廷荣阎雪莹王吉锡许树军
朱艳华,刘廷荣,阎雪莹,王吉锡,许树军
(黑龙江中医药大学,黑龙江 哈尔滨 150040)
磷酸川芎嗪药理作用确切,临床应用广泛。目前已有注射液、片剂、胶囊剂等剂型应用于临床,主要用于治疗各种心脑血管疾病。磷酸川芎嗪温敏凝胶通过鼻腔给药,可以通过血脑屏障发挥药效,其特性是在室温下具有较好流动性的液体,用药后可在鼻腔温度下形成凝胶状,明显延长药物在鼻腔内的滞留时间。然而有些鼻用制剂在给药后会影响鼻腔和鼻黏膜纤毛系统的功能,严重时可使鼻黏膜纤毛运动发生不可逆的停止。所以本实验对磷酸川芎嗪温敏凝胶使用时是否会对鼻腔有影响做了研究。
1 试剂与材料
光学显微镜XSZ-H型(重庆光学仪器厂);磷酸川芎嗪温敏凝胶(批号20101203,自制);磷酸川芎嗪(TMPP,批号20100403,北京市燕京药业有限公司);氯化钠注射液(批号100718506,石家庄四药有限公司);去氧胆酸钠(批号20100305,北京奥博星生物技术有限公司);盐酸麻黄碱注射液(批号20100706-2,东北制药集团公司沈阳第一制药厂);其它试剂均为分析纯。
中华大蟾蜍(体质量30~35g),雌雄兼用,黑龙江中医药大学GLP实验中心提供。
2 方法与结果
2.1 纤毛毒性考察方法
选择体质量30~35g的中华大蟾蜍30只,随机分为6组,每组5只。采用在体蟾蜍上腭模型法[1]。先将蟾蜍用探针破坏脊髓,然后将其仰卧固定在手术板上,使其上腭裸露,以防止吞咽药液。在上腭黏膜处滴加药液0.5ml,将上腭黏膜完全浸没,浸润30min。用生理盐水将药液冲洗净,然后用眼科剪刀和镊子将蟾蜍两眼中间部位的上腭黏膜分离,约3mm×3mm大小。立即用生理盐水冲洗黏膜的血块、杂物等,将黏膜纤毛面向上平铺于载玻片上,盖上盖玻片,生理盐水制片,用40×10倍显微镜观察纤毛摆动情况。观察结束后,将制片置于加有少量蒸馏水饱和层析缸中,密闭,环境温度20~25℃。每隔一定时间将制片取出,在盖玻片边缘滴加适量生理盐水,同法镜下观察纤毛摆动情况,若纤毛仍有摆动现象,则将标本再放回层析缸中,继续观察,直至停止,记录纤毛从给药开始至停止摆动所持续时间。
2.2 纤毛毒性评价方法
2.2.1 纤毛持续摆动时间百分率
纤毛持续摆动时间的百分率是受试液组的纤毛持续摆动时间与生理盐水对照组的纤毛持续摆动时间的比值。百分率越高,表示药物对纤毛运动影响越小,对纤毛毒性越小[2]。
2.2.2 纤毛形态学改变
采用可拍照的生物数码显微镜,观察给予各种受试药液后的纤毛形态,并进行拍照。
2.3 实验结果
2.3.1 纤毛持续摆动时间百分率
给予原料药磷酸川芎嗪(0.01%)和磷酸川芎嗪温敏凝胶(0.01%)后,纤毛持续摆动时间相对于生理盐水的百分率在70%~80%之间,说明原料药液和含药凝胶均对纤毛运动有一定影响;而空白凝胶组的相对百分率较高,说明凝胶辅料无明显纤毛毒性。结果见表1。
表1 受试溶液对纤毛持续摆动时间的影响(±s,n=5)
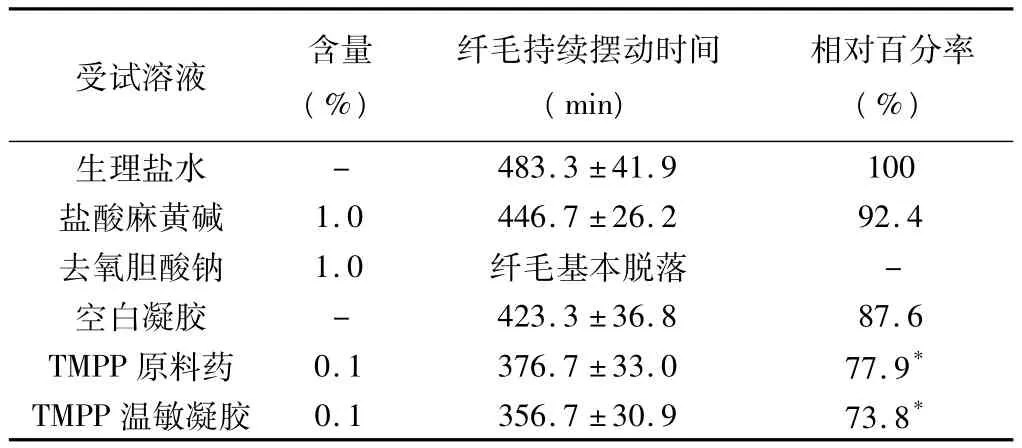
表1 受试溶液对纤毛持续摆动时间的影响(±s,n=5)
注:与生理盐水组比较,*P <0.05。
受试溶液含量(%)纤毛持续摆动时间(min)相对百分率(%)483.3 ±41.9 100盐酸麻黄碱 1.0 446.7 ±26.2 92.4去氧胆酸钠 1.0 纤毛基本脱落-空白凝胶-423.3±36.8 87.6 TMPP 原料药 0.1 376.7 ±33.0 77.9*TMPP 温敏凝胶 0.1 356.7 ±30.9 73.8生理盐水-*
2.3.2 纤毛形态学变化
采用在体蟾蜍上腭模型法制片,光学显微镜下(×400)观察各受试溶液组的纤毛形态及摆动情况。生理盐水组和盐酸麻黄碱组,清晰整齐,有规律的向同一个方向摆动,且十分活跃、频率很高;去氧胆酸钠组,视野范围内无法找到摆动纤毛,纤毛已基本脱落,表明去氧胆酸钠对纤毛运动有严重的不可逆的抑制作用,对黏膜组织有严重的破坏作用;空白凝胶组情况与盐酸麻黄碱组相似,纤毛清晰可见,运动灵活,可见由于凝胶溶液粘度较大,凝胶辅料对纤毛运动有一定影响,但无明显的纤毛毒性;而磷酸川芎嗪原料药组及磷酸川芎嗪温敏凝胶组观察视野内的纤毛数量和摆动灵活度上相对于生理盐水组及盐酸麻黄碱组都有一定程度的减弱。说明药物对纤毛运动有一定的影响。
3 讨论
采用盐酸麻黄碱(公认无纤毛毒性)作为阴性对照,去氧胆酸钠(公认有严重纤毛毒性)作为阳性对照,以生理盐水作为空白对照,评价磷酸川芎嗪原料药、凝胶辅料、磷酸川芎嗪温敏凝胶剂的鼻纤毛毒性。采用在体蟾蜍上腭模型法,以给药后的中华大蟾蜍上腭纤毛持续摆动时间百分率和纤毛形态学改变为指标,考察了受试液对鼻纤毛的影响。
初步实验表明,含药凝胶对纤毛有一定的毒性影响,空白凝胶抑制作用相对较小。此外,由于凝胶为半流体,有一定黏稠度,也可能是对纤毛摆动有抑制的原因之一;再者离体组织自身的缺氧、分离黏膜时破坏黏液层,都可能成为影响纤毛运动停止的原因。
本实验采用在体蟾蜍上腭模型法考察药物鼻纤毛毒性,优点是与哺乳动物鼻粘膜纤毛相似,且镜下观察较直观,可同时观察粘膜完整性、纤毛数量、纤毛脱落情况等形态学变化。但该法同时也存在不足之处:粘膜在分离时会破坏粘液层,忽视了粘液层对鼻纤毛的保护作用。应用在体蟾蜍上腭模型法评价药物的鼻粘膜纤毛毒性应注意以下因素的影响:实验动物的体重会影响实验结果,体质量较大动物的纤毛摆动时间是较小动物的60% ~70%,故本实验选用体质量为30~35g的中华大蟾蜍,以保证实验结果的准确性;黏膜的位置,为保证黏膜与药液充分接触,本实验选取蟾蜍两眼中间部位的上腭黏膜,该部位能完全被药液浸没,且可减少因粘膜部位不同带来的差异性[3]。
通过对纤毛持续摆动时间百分率和给药后纤毛形态的评价,可以看出空白凝胶抑制作用相对较小,而磷酸川芎嗪温敏凝胶对纤毛有一定毒性。文献显示,小分子化学合成药物对纤毛运动的影响较为普遍[4],也可能与磷酸川芎嗪溶液的酸度较大(pH值=3.26)、对粘膜有一定刺激性有关。
通过实验说明,本研究中所制备的磷酸川芎嗪温敏凝胶对纤毛运动有一定的影响,需要进一步包合才可以用于鼻腔给药。
[1] 林华庆,宋涛,王东凯,等.利巴韦林鼻用温敏凝胶的鼻腔纤毛毒性研究[J].中国新药杂志,2007,16(16):1258-1260.
[2] 田志发.盐酸氯胺酮喷雾剂经鼻黏膜吸收动力学及纤毛毒性研究[J].海峡药学,2009,21(1):65-67.
[3] 刘莱.氢溴酸右美沙芬鼻用热敏凝胶的研究[D].沈阳:沈阳药科大学,2005:48-53.
[4] 蒋新国,崔景斌,方晓玲,等.药物的鼻粘膜纤毛毒性及评价方法[J].药学学报,1995,30(11):848-853.
