艾滋病患者抗病毒督导治疗疗效分析*
2013-12-17李晓菲余祖江梁红霞江河清阚全程
李晓菲,余祖江,梁红霞,何 云,江河清,阚全程
1)郑州大学第一附属医院药剂科 郑州450052 2)郑州大学第一附属医院感染科 郑州450052 3)郑州市第六人民医院 郑州400050
#通讯作者,男,1963年5月生,博士,主任药师,研究方向:药学及免疫学,E-mail :johnyue1970@yahoo.com
高效抗逆转录病毒治疗(highly active antiretroviral therapy,HAART)已经成为抗人类免疫缺陷病毒(human immunodeficiency virus,HIV)感染最有力的工具。HAART 除可以用于成人、青少年外,重要的是可以应用于儿童和孕妇,能显著减少HIV 的母婴传播率,抑制病毒复制,部分恢复机体的免疫功能[1]。有效的抗病毒治疗可以降低机会性感染的发生率,提高生活质量,但不规范的抗病毒治疗,则可能导致耐药毒株的发生,降低抗病毒疗效,造成机会性感染发生,降低生命质量。为了探索适合我国的抗病毒治疗模式和规范,作者对某一艾滋病治疗示范区部分HIV 感染者进行全程督导治疗,探讨可能适合我国的HAART 模式,为我国艾滋病(acquired immunodeficiency syndrome,AIDS)正规治疗提供理论基础。
1 对象与方法
1.1 研究对象 选择2005年1月至2006年12月AIDS 治疗示范区某一乡村HIV 感染者377例,年龄18~65 岁男208例,女169例;均通过ELISA 检测和HIV 免疫印迹试验鉴定为阳性。入选标准:CD4+T 淋巴细胞1.0~3.5×105L-1,HIV-RNA >5×104拷贝/mL。排除标准:①血红蛋白<90 g/L。②WBC <2×109L-1。③嗜中性粒细胞数<1×109L-1。④血小板<7.5×1010L-1。⑤胰淀粉酶>440 U/L。⑥血肌酐>200 μmol/L。⑦天门冬氨酸氨其转移酶(ALT)>120 U/L ,丙氨酸氨基转移酶(AST)>120 U/L 和碱性磷酸酶(ALP)>450 U/L;总胆红素(TB)>40 μmol/L。
1.2 实验分组和治疗 患者随机分为督导治疗组和未督导治疗组。督导治疗组134例,男79例,女55例,年龄18~64(38.4±25.6)岁;督导治疗组243例,其中男129例,女114例,年龄19~65(39.1±24.6)岁。2组患者的治疗均采用HAART 方案:齐多夫定(AZT,东北制药厂),300 mg/次,2 次/d,二去氧肌苷(DDI,东北制药厂),200 mg/次(若体质量小于60 kg则125 mg/次),2 次/d,拉米夫定(3TC,葛兰素史克公司),300 mg/次,1 次/d,司他夫定(D4T,上海迪赛诺生物有限公司),40 mg/次(若体质量小于60 kg 则30 mg/次),2 次/d,奈韦拉平(NVP,上海迪赛诺生物有限公司)200 mg/次,2 次/d(14 d 导入期内200 mg/次,1 次/d)。督导治疗组患者:15 d 定期随访,坚持发药到手,服药到口,建立严格规章制度,采用教育等方法促进患者长期、规律服药。未督导治疗组患者未采取以上督导措施。
1.3 观测指标
1.3.1 CD4+和CD8+T 淋巴细胞计数 用EDTA K2抗凝采静脉血2 mL,轻轻颠倒混匀,16~25℃保存,48 h 内检测,每个样品准备2 个试管,分别加入抗体(CD4+或CD8+单克隆抗体)和对照同型抗体,同时加入100 μL 抗凝血液样品。混匀后放置室温10~15 min。每管加入红细胞裂解液500 μL,红细胞充分裂解后加入荧光微球100 μL,加入500 μL PBS 稀释后上机(美国Beckman 公司产品)分析结果。
1.3.2 WBC 计数 用EDTA K2抗凝采静脉血2 mL,轻轻颠倒混匀,应用Beckman Coulter HMX 血细胞分析仪检测。
1.3.3 HIV-RNA 定量检测 按照试剂盒要求(由深圳匹基生物工程公司提供),常规获得患者的血浆100 μL,加200 μL RNA 提取液,混匀,常规酚:氯仿:异戊醇提取,4℃13 000 r/min 离心,14 min 后取上清,加2 倍乙醇沉淀,离心后加体积分数为75%的乙醇洗涤,沉淀烘干后加20 μL 的无RNA 酶水溶解,依次加入随机引物行逆转录。按试剂盒要求进行PCR 定量扩增。反应条件为:42℃,45 min;94℃,5 min 后进入主循环92℃30 s,55℃30 s,72℃30 s ,45 个循环,定量检测PCR 产物。所测外周血标本病毒检测值取对数,检测病毒数值为阴性者按0 计算。
外周血内CD4+、CD8+T 淋巴细胞,WBC 和HIV-RNA 定量检测共计12 个月,其中第1 到3 个月每月检测1 次,后每3 个月检测1 次上述指标。
1.4 统计学处理 用SAS 9.1 分析数据,2组患者外周血CD4+、CD8+T 淋巴细胞、WBC 计数和HIVRNA 载量的比较采用重复测量资料的方差分析,检验水准α=0.05。
2 结果
2.1 2组患者外周血CD4+T 淋巴细胞计数 见表1。
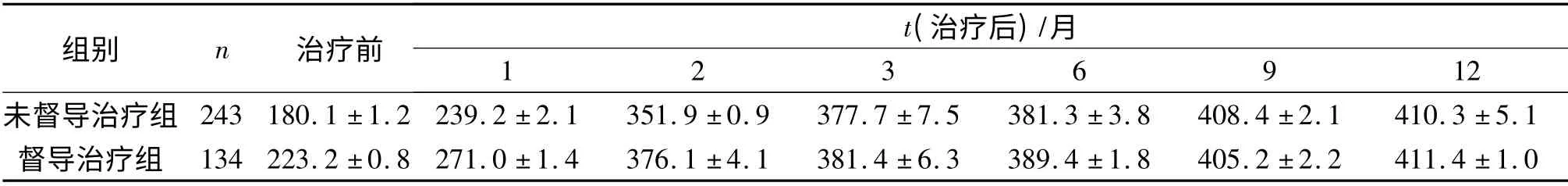
表1 2组患者外周血CD4 +T 淋巴细胞计数比较×109/L
2.2 2组患者外周血CD8+T 淋巴细胞计数 见表2。
2.3 2组患者外周血WBC 计数 见表3。5 分色法检测AIDS 人群治疗前后WBC 计数,共检测7 次(其中第1 次为治疗前)。
2.4 2组患者HIV-RNA 检测值比较 见表4。

表2 2组患者外周血CD8 T 淋巴细胞计数比较×10/L

表3 2组患者外周血WBC 计数比较×109/L

表4 2组患者HIV-RNA 检测值比较×104 拷贝/mL
3 讨论
尽管目前联合治疗还没有达到理论水平,但联合治疗是目前艾滋病患者最主要的治疗方法[2]。随着联合抗病毒治疗的疗程进行,治疗过程中出现的耐药问题越来越引起了人们的重视。发展中国家与部分发达国家药物价格昂贵,另一方面药物产生的副作用以及药物之间的大量相互作用也使患者难以接受治疗[3]。如果治疗方案不完善或者应用不当会导致病毒出现抗药性。Prosperi 等[4]研究结果显示,曾广泛应用抗病毒药物治疗后未坚持治疗,导致了HAART 的失败。另外研究[5-6]显示病毒变异和耐药株正在不断出现,甚至一种耐药可以引起药物交叉耐药。我国在开展HAART 治疗中也发现不同程度的耐药病毒株,这为防治艾滋病的传播增加了难度[7-8]。
该研究发现,2组治疗人群在抗病毒治疗过程中,细胞免疫功能显著提高:抗病毒治疗第1 个月起,CD4+T 淋巴细胞、CD8+T 淋巴细胞或者WBC计数逐渐上升,治疗3 个月后CD4+T 淋巴细胞、CD8+T 淋巴细胞和WBC 计数逐渐稳定。但HIVRNA 定量检测结果提示抗病毒治疗后前3 次获得相似的抗病毒治疗效果,从第5 次检测开始未督导治疗组HIV-RNA 检测值明显高于督导治疗组,随着时间延长,2组之间HIV-RNA 检测值的差距加大。表明随着抗病毒治疗时间的延长,未督导治疗组逐渐出现耐药,但免疫功能重建后的CD4+、CD8+T 淋巴细胞计数并没有随之下降,出现滞后。
一般认为,首次治疗方案失败后选择另一种治疗方案进行补救治疗,疗效不容乐观,短期内获得最大限度病毒抑制的可能性较低[9]。作者的上述结果表明在不规范的抗病毒治疗过程中,耐药出现时间早而且多,但CD4+、CD8+T 淋巴细胞和WBC 计数下降并未同期出现,给国人,尤其农村地区以“感觉”进行抗病毒带来困难。因此规范化的抗病毒治疗或者仅根据CD4+水平进行抗病毒治疗是不够的,需要进一步研究更完善和简单的督导治疗方案。
[1]Hammer SM,Katzenstein DA,Hughed MD,et al.A trial comparing nucleoside monotherapy with combination therapy in HIV-infected adults with CD4 cell counts from 200 to 500 per cubic millimeter.AIDS Clinical Trials Group Study 175 Study Team[J].N Engl J Med,1996,335(15):1081
[2]Perelson AS,Essunger P,Cao Y,et al.Decay characteristics of HIV-1 infection compartments during combination therapy[J].Nature,1997,387(66I9):188
[3]曹韵贞.高效抗艾滋病毒治疗的效果评论[J].国外医学:流行病学传染病分册,2000,27(1):1
[4]Prosperi MC ,Zazzi M ,Punzi G ,et al .Low rate of virological failure and maintenance of susceptibility to HIV-1 protease inhibitors with first-line lopinavir/ritonavir-based antiretroviral treatment in clinical practice[J].J Med Virol,2010,82(12):1996
[5]Rizzardini G,Capetti A.Switch to abacavir-based triple nucleoside regimens in HIV-1 infected patients never treated with suboptimal antiretroviral therapy:a review[J].Med Sci Monit,2006 ,12(12):RA269
[6]Metzger DS,Woody GE,O' Brien CP.Drug treatment as HIV prevention:a research update[J].J Acquir Immune Defic Syndr,2010,55(Suppl 1):S32
[7]Zhang FJ,Maria A,Haberer J,et al.Overview of HIV drug resistance and its implications for China[J].Chin Med J (Engl),2006,119(23):1999
[8]Cao YZ,Lu HZ.Care of HIV-infected patients in China[J].Cell Res,2005,15(11/12):883
[9]Sosman JM.Optimizing HIV care:policy implications[J].Am J Manag Care,2010,16(13 Suppl):S339
