CT三维容积重建评价慢性化脓性中耳炎听骨链破坏的价值
2013-12-10GUOYong
郭 勇 GUO Yong
逯巧慧1 LU Qiaohui
刘 阳2 LIU Yang
王庆军1 WANG Qingjun
任爱军1 REN Aijun
2.海军总医院耳鼻喉科 北京 100048
慢性化脓性中耳炎(chronic suppurative otitis media, CSOM)为临床常见病,准确评估中耳炎听骨破坏部位及程度是临床选择不同手术方式的基础。CT是检查听小骨的主要方法,也是评估慢性中耳炎的“金标准”。以往临床工作中主要采用CT轴位和(或)冠状位扫描及多平面重组进行评估,也有较多关于中耳仿真内镜(VE)的报道,但采用三维容积重建(3DVR)评价听骨破坏的研究较少[1-7]。CT分辨率的提高及重建软件的发展使细小解剖结构的3DVR更清楚、更快捷,也使3DVR用于临床实际工作成为可能。与常规2D重建方法比较,3DVR提供了更直观的图像,但其诊断准确度情况尚未见报道。本研究拟探讨3DVR评价CSOM听骨破坏的能力,为临床诊断及治疗提供依据。
1 资料与方法
1.1 研究对象 2010-06~2012-01在海军总医院行颞骨CT检查并经手术证实的48例CSOM患者,其中男21例,女27例;年龄16~64岁,平均(31.3±11.2)岁。术中观察并记录听骨破坏情况。CT检查与手术间隔时间1~10 d,平均3.9 d。
1.2 检查方法 使用 Philips Brilliance iCT 256层螺旋CT仪,患者取仰卧位,行轴位薄层扫描。扫描范围自外耳道下缘至岩骨上缘,层厚0.67 mm,螺距0.25,视野 150 mm×150 mm,矩阵 1024 ×1024。电压 120 kV,电流350 mA。采用Y-sharp算法(骨算法的一种,边缘更锐利),0.34 mm间隔重叠重建,获得120~150层图像,并传至EBW 4.0工作站进行2D及3DVR。
1.3 重建方法 2D重建图像包括轴位和冠状位。3DVR分别在冠状位、轴位定位图像上定义容积重建的6个边。在冠状位定位图像上选择砧镫关节层面,定义4个边:砧镫关节下方水平线、中耳鼓室上缘水平线、镫骨板内侧垂直线、外耳道内1/2垂直线。同时在轴位定位图像上选择锤砧关节层面,以中耳鼓室前后缘水平线为边界。对重建后的图像进行放大、旋转,可清楚地观察各听小骨结构;也可以根据显示需要对影响观察的结构进行简单切割,重建时间1.0~2.0 min。主要采用2个观察方向,即由下鼓室向上观察和由上鼓室向下观察。显示窗宽为2000 Hu,窗位为-400~500 Hu。2D、3DVR及评估分别由一名对颞骨解剖及病变诊断有丰富经验的放射科医师独立完成。
1.4 听骨评价方法 采用三分分级法[8]对12个解剖标志的听骨破坏情况进行评分,0分为解剖结构缺失;2分为解剖结构清晰、完整;1分为解剖结构可见,但不清晰或部分缺失。评价关节时,0分代表完全脱位或破坏;2分代表无脱位及破坏;1分代表半脱位或关节部分破坏。所有手术由同一位对听骨手术有丰富经验的耳科医师完成。术中医师观察并根据上述三分分级法对12个解剖标志进行评分。
1.5 统计学方法 使用SPSS 16.0软件,以术中所见为标准,2D、3DVR对12个解剖标志评分准确度比较采用χ2检验。为计算2D、3DVR的诊断敏感度、特异度、准确度,将所有评分为0定为阴性,即结构缺失;将所有评分为1或2定为阳性,即结构存在。2D、3DVR及术中所见的一致性检验采用Pearson相关分析,P<0.05表示差异有统计学意义。
2 结果
2.1 CSOM患者听骨链破坏情况 术中对12个解剖部位进行评分发现,砧骨长突、豆状突、砧镫关节破坏发生率较高,分别为66.7%、54.2%、54.2%。
2.2 2D、3DVR对听骨链破坏的评价结果 锤骨外侧突在2D图像上无法评估,2D重建评价听骨破坏的准确度均在83%以上,其对砧骨长突、豆状突、砧镫关节破坏发生率较高的部位的诊断准确度低于其他破坏发生率较低的部位。3DVR评价听骨破坏的准确度均在93%以上,对各部位评价准确度均高于2D,12个部位2D与3DVR敏感度、特异度、准确度比较,差异均有统计学意义(P<0.001),见表1及图1~6。
2.3 2D、3DVR及术中所见的一致性检验 2D、3DVR评价听骨链破坏的分级结果与手术所见分级结果呈显著正相关(r=0.841、0.970, P<0.001),2D及3DVR评价听骨链破坏的分级结果也呈显著正相关(r=0.849, P<0.001)。
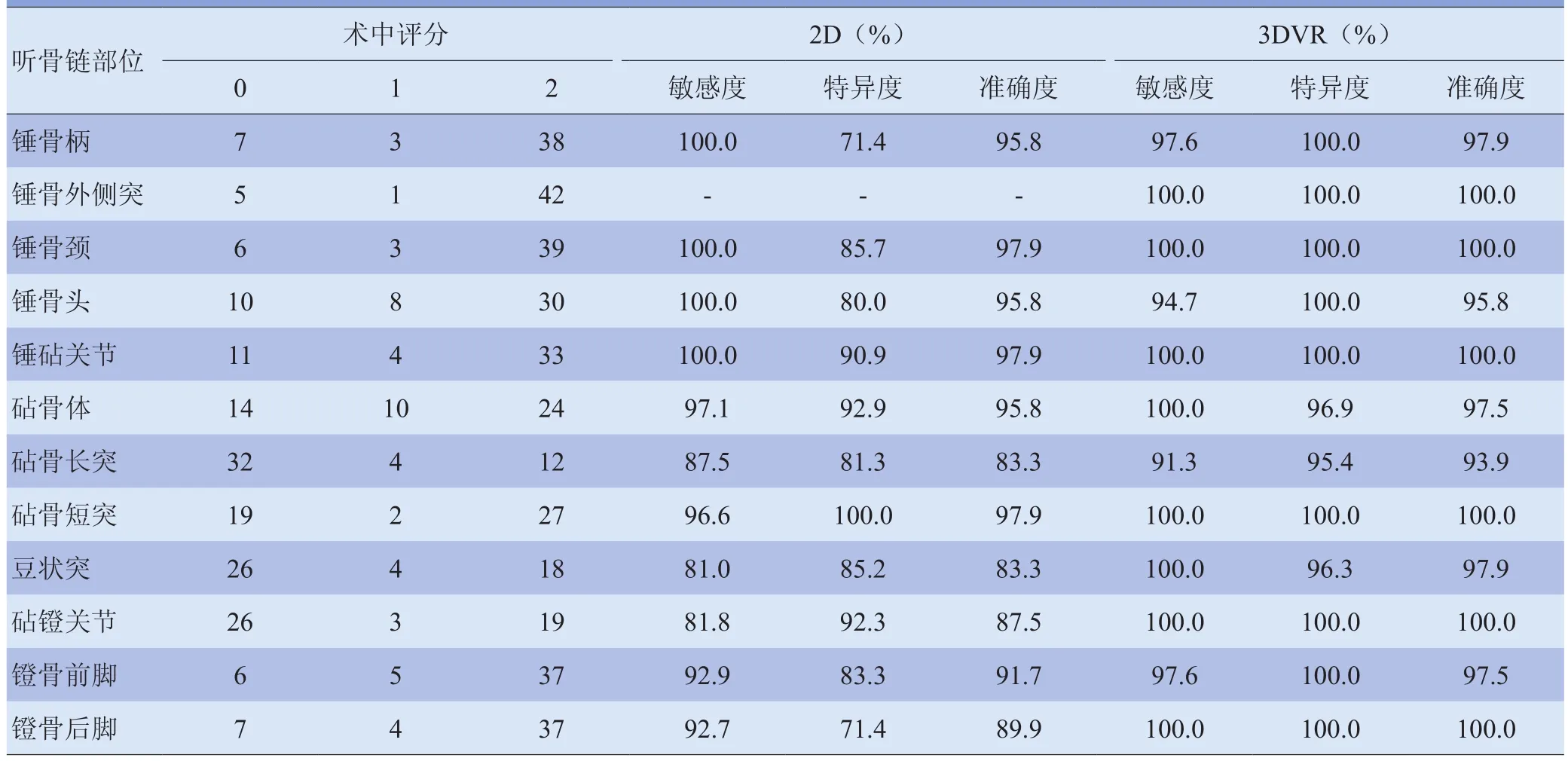
表1 慢性化脓性中耳炎患者听骨链12个部位术中评分及2D、3DVR评估结果(n=48)
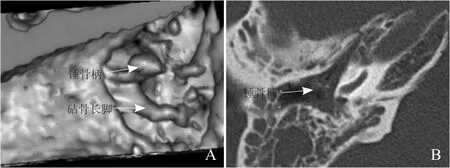
图1 患者女,52岁。A. 3DVR(由下鼓室向上观察)示锤骨柄中部破坏;B.轴位2D示锤骨柄破坏,但在术前评估中,破坏残存的锤骨柄远端无法与钙化鉴别,未能准确诊断

图3 患者男,48岁。A. 3DVR(由上鼓室向下观察)示锤砧关节部位砧骨体部分吸收;B.轴位2D可见砧骨体部分吸收,所见与3DVR一致
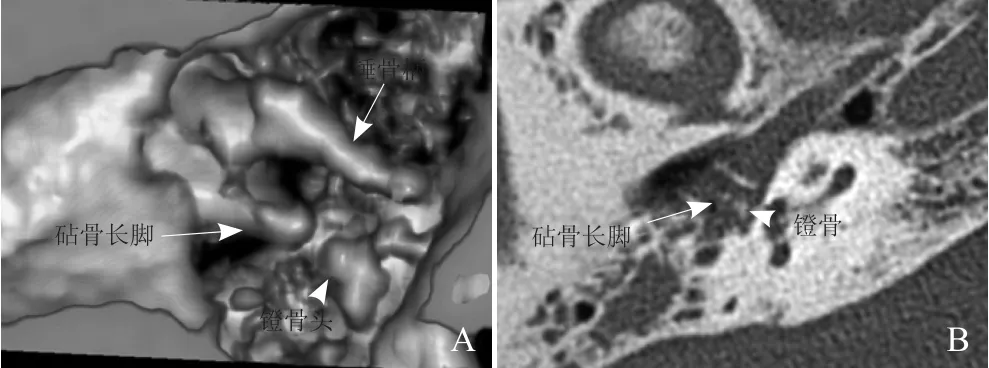
图5 患者女,58岁。A. 3DVR(由下鼓室向上观察)示砧骨长脚远端的豆状突吸收,砧镫关节分离;B.轴位2D图像无法诊断豆状突吸收,砧镫关节分离
3 讨论
既往CTVE在耳部的研究多侧重于其在中耳的运用,CTVE能清楚地显示听小骨链的三维结构,有助于诊断病变,但不能清楚地显示中耳鼓室内的软组织病变及镫骨结构[9-15],当中耳鼓室内充满炎症液体及黏膜增厚时,很难清楚地显示听骨链结构,而本组病例中耳鼓室内均被软组织充填。3DVR与CTVE相比图像更有真实感,图像可以根据需要任意切割,通过旋转可以从不同的角度观察。既往3DVR的主要局限性在于从复杂的颞骨中切割出独立的听小骨链耗费时间长,最小的听骨-镫骨显示不佳[4,12,13]。由于以往重建软件功能的限制及重建方法的不足,关于3DVR评价听骨链的研究较少,该技术也未能广泛应用于临床。
本研究采用的定义6条边线的3DVR方法简单快捷,2 min内均可完成,并且利用上下两个观察视野能完全覆盖听骨链12个解剖部位。通过旋转观察类似内镜,便于耳科及放射科医师理解图像。重建方法简单、速度快,使3DVR技术广泛应用于临床成为可能。

图2 患者女,18岁。A. 3DVR(由下鼓室向上观察)示锤骨头、颈完全吸收破坏,砧骨体部分吸收;B.轴位2D图像可见砧骨体,与之相关节的锤骨头消失,所见与3DVR一致
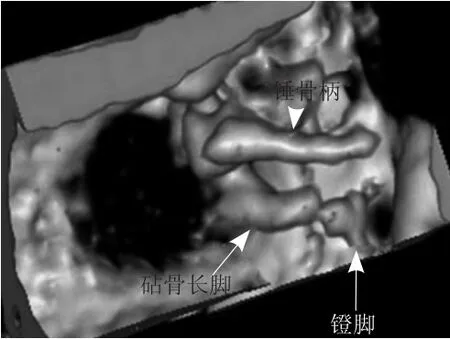
图4 患者男,16岁。3DVR(由下鼓室向上观察)示砧骨体、砧骨短脚完全吸收破坏

图6 患者男,43岁。3DVR(由下鼓室向上观察)示镫骨后脚吸收消失,镫骨前脚部分吸收呈明显粗细不均匀
Pandey等[10]的研究表明,高分辨2D及CTVE评价CSOM听骨链破坏的准确度与被评价部位的大小相关,2D图像评价的准确性为:锤骨100%,砧骨85.29%,镫骨76.97%;CTVE评价的准确性为:锤骨100%,砧骨88.24%,镫骨85.29%。本研究结果显示,高分辨2D诊断CSOM听骨链破坏的准确度主要与受累部位的发生率相关,即破坏发生率高的部位(如砧骨长突、豆状突、砧镫关节)的诊断准确度低于其他破坏发生率低的部位;而3DVR诊断CSOM听骨链破坏的准确度明显高于2D,且诊断不受被评价部位大小及破坏发生率的影响。由于2D图像为局部断面图像,不能在一幅图像上全面显示形态各异的听骨结构,病变的显示受扫描层面与解剖结构长轴是否平行的影响,特别是当骨质破坏较小时,如砧骨长脚、豆状突的破坏,在轴位及冠状位图像上很难显示。解剖结构越小(如镫骨),可能评价越困难,评价的准确度会降低。然而,本研究结果显示破坏发生率高的部位诊断准确度下降,而并非解剖结构越小的部位诊断准确度越低,表明2D图像对听骨破坏的诊断存在一定的不准确性。3DVR图像能够三维立体全面地显示听骨链结构,因此更容易显示听骨破坏,特别是显示病变范围较小的破坏,因此其诊断准确度更高。
3DVR能清楚地显示听骨链12个解剖结构,包括最小的镫骨。本组病例中耳鼓室均见软组织充填,通过对3DVR图像阈值的调整,均能清楚地显示正常解剖及听骨链的破坏。3DVR的主要局限性是不能评价镫骨底板。
总之,听骨链CT 3DVR快速、简单,图像生动逼真,类似耳科内镜,对CSOM听骨链破坏的诊断准确度高于高分辨2D图像,可以作为颞骨2D图像的有效补充。
[1] 黄云海, 梁碧玲. 颞骨CT多平面重建标准化探讨. 中国CT和MRI杂志, 2009, 7(2): 14-17.
[2] 刘兆会, 鲜军舫, 王振常, 等. 慢性化脓性中耳炎HRCT研究. 医学影像学杂志, 2007, 17(2): 123-127.
[3] 王筱容, 翟冰, 刘文华, 等. 慢性化脓性胆脂瘤型中耳炎的高分辨CT诊断. 中华耳科学杂志, 2005, 3(2): 107-109.
[4] 邱丽芹, 黄越, 徐学权, 等. 中耳胆脂瘤的64层螺旋CT听小骨VR重组及其临床意义. 中国CT和MRI杂志, 2009,7(5): 24-26.
[5] 周兵, 靳兆军, 赵娜, 等. 螺旋CT三维成像对听骨链解剖结构的观察. 中国医学影像学杂志, 2003, 11(3): 235-236.
[6] 王东, 张挽时, 熊明辉. 听骨链的螺旋CT三维重建技术及其临床初步应用. 中国医学影像学杂志, 2000, 8(4): 268-270.
[7] Fatterpekar GM, Doshi AH, Dugar M, et al. Role of 3D CT in the evaluation of the temporal bone. Radiographics, 2006,(Suppl 1): S117-S132.
[8] Chuang MT, Chiang IC, Liu GC, et al. Multidetector row CT demonstration of inner and middle ear structures. Clin Anat,2006, 19(4): 337-344.
[9] Wang D, Zhang W, Xiong M, et al. CT virtual endoscopy of the auditory ossicular chain: clinical applications. Clin Med J(Engl), 2001, 114(10): 1015-1018.
[10] Pandey AK, Bapuraj JR, Gupta AK, et al. Is there a role for virtual otoscopy in the preoperative assessment of the ossicular chain in chronic suppurative otitis media? Comparison of HRCT and virtual otoscopy with surgical f i ndings. Eur Radiol,2009, 19(6): 1408-1416.
[11] Park K, Moon SK, Cho MJ, et al. 3D micro-CT images of ossicles destroyed by middle ear cholesteatoma. Acta Otolaryngol, 2004, 124(4): 403-407.
[12] Nakasato T, Sasaki M, Ehara S, et al. Virtual CT endoscopy of ossicles in the middle ear. Clin Imaging, 2001, 25(3): 171-177.
[13] Neri E, Caramella D, Panconi M, et al. Virtual endoscopy of the middle ear. Eur Radiol, 2001, 11(1): 41-49.
[14] Pauriol-Lacaze S, Pouget JF, Michel F, et al. Advantage of virtual endoscopy in the evaluation of the ossicular chain. J Radiol, 2003, 84(12 Pt 1): 1961-1968.
[15] Rodt T, Bartling S, Schmidt AM, et al. Virtual endoscopy of the middle ear: experimental and clinical results of a standarised approach using multi-slice helical computed tomography. Eur Radiol, 2002, 12(7): 1684-1692.
