影响腐乳结晶物产生的因素*
2013-10-30代来鑫卢红梅张丽平张百发姜晓琳
代来鑫,卢红梅,张丽平,张百发,姜晓琳
1(贵州大学贵州省发酵工程与生物制药重点实验室,贵州 贵阳,550025)
2(贵州大学化学与化工学院,贵州 贵阳,550025)
腐乳是一种人们喜爱的调味品,不仅具有大豆所具有的营养价值,还因为经微生物发酵后,蛋白质分解成氨基酸和多肽,淀粉转化为单糖和低聚糖,极易被人体吸收,使其生物利用度最大化[1]。另外,通过微生物发酵,大豆的苦腥味、含有的胀气因子、抗营养因子等不良因素被克服,同时产生了多种具有香味的有机酸、醇、酯和氨基酸[2]。但腐乳在后酵期和货架期容易出现多种影响产品外观的质量问题,如腐乳白点和结晶物,不仅会在食用过程中给消费者带来不便,同时也严重影响了企业的销售和声誉。研究人员对腐乳白点问题的研究比较深入[3-5],而对腐乳结晶物的相关报道则较少。
袁振远等[6]定性腐乳结晶物的成分为磷酸铵镁和磷酸镁的混合物。黄永涛等[7]经过研究分析确定贵阳某腐乳生产厂腐乳结晶物的主要成分为磷酸铵镁(MgNH4PO4·6H2O),不含磷酸镁。通过对后酵车间中不同批次后酵青方腐乳样品进行观察对比,发现青方腐乳后酵前5 个月几乎没有结晶物现象,结晶物开始出现的时间段为后酵期6 ~7 个月,一般青方腐乳的后期发酵不少于6 个月[8]。本实验分别取不同后酵时间(后酵8、9、10、13、14、15 个月,包括在工厂或商店的储藏期)的有结晶物的青方腐乳样品,测定其中相关成分含量,分析了不同后酵时间段有结晶物青方腐乳样品相关成分与结晶物产生的关系,通过实验模拟了不同影响因素对结晶物产生的影响。
1 实验材料与方法
1.1 实验材料
青方腐乳,来源于贵阳某腐乳生产厂。
1.2 实验方法
1.2.1 腐乳卤汤中氨氮、磷、镁的分析方法
1.2.1.1 样品处理
取每批次腐乳实验样品5 瓶,每瓶吸取5 mL 卤汤共25 mL,定容到250 mL 容量瓶中,加滤纸过滤,制得样品腐乳卤汤10 倍稀释液。
1.2.1.2 磷含量的测定
取制备好的腐乳卤汤10 倍稀释液,再稀释10倍,即得腐乳卤汤100 倍稀释液,摇匀取3 mL 置于25 mL 容量瓶中依次加入2 mL 浓度为25 g/L 钼酸铵溶液、1 mL 浓度为5 g/L 对苯二酚溶液、1 mL 浓度为200 g/L Na2SO3溶液,定容,静置显色30 min。以蒸馏水为空白,波长为660 nm 比色分析测定P 含量。3 组平行实验,测定结果取平均值。
1.2.1.3 氨氮含量的测定
取腐乳卤汤100 倍稀释液1 mL,置于50 mL 容量瓶中,加水定容至刻度后加入1 mL 浓度为500 g/L酒石酸钾钠溶液,摇匀,再加入纳试剂1 mL 摇匀,室温下放置10 min,波长420 nm 下,1 cm 比色皿,测定吸光度,计算氨氮含量。3 组平行实验,测定结果取平均值。
1.2.1.4 镁含量的测定
取10 mL 样品腐乳卤汤10 倍稀释液,按络合滴定法[9]测定其中Mg2+含量。乙二胺四乙酸二钠标液的浓度为0.01062 mol/L。
1.2.2 腐乳( 坯体) 中氨基酸态氮、总酸、盐含量的分析方法
1.2.2.1 样液制备
将腐乳坯从瓶中直接取出,置于漏斗中,静置30 min,以除去卤汤。取约150 g 左右不含卤汤的腐乳样品,放入洁净干燥的研钵中研磨成糊状,备用。称取约20 g 研磨好的腐乳样品置于150 mL 烧杯中,加入60 ℃水80 mL,搅拌均匀并置于电炉上加热,煮沸后即取下,冷却至室温(每隔0.5 h 搅拌1 次),然后移入200 mL 容量瓶中,用少量水多次洗涤烧杯,洗液并入容量瓶中,加水定容,混匀,用干燥滤纸滤入250 mL 磨口瓶中备用。
1.2.2.2 测定方法[10]
(1)总酸、氨基酸态氮含量的测定
吸取10.0 mL 制备好的样液,置于250 mL 广口锥形瓶中,加水50 mL,开动磁力搅拌器,用NaOH(CNaOH=0.05 mol/L)滴定至pH8.2(酸度计),记下消耗NaOH 的体积,计算总酸含量。再加入10 mL 甲醛溶液,混匀,用NaOH 继续滴定至pH9.2,记录消耗的NaOH 的体积,计算氨基酸态氮含量。同时取50 mL 蒸馏水做空白试验。
(2)食盐含量的测定
取制备好的样液2.0 mL,置于250 mL 广口锥形瓶中,加50 mL 水及1 mL 铬酸钾指示剂,混匀。用AgNO3标准溶液(0.100 mol/L)滴定至初显砖红色。同时取50 mL 蒸馏水做空白试验。
1.2.2.3 计算方法
(1)总酸计算

式中:X1—试样中总酸含量(以乳酸计)(g/100g);C— NaOH 标准溶液浓度(mol/L);V1—测定试样消耗的NaOH 标准溶液体积(mL);V2—测定空白消耗的NaOH 标准溶液体积(mL);m—称取腐乳质量(g);0.090—与1.00 mL NaOH 标准溶液[CNaOH=1.000 mol/L)相当的乳酸的质量(g)。
计算结果保留3 位有效数字。
(2)氨基酸态氮的计算

式中:X2—试样中氨基态氮的含量(g/100g);C—NaOH 标准滴定溶液的浓度(mol/L);V1—测定试样稀释液加入甲醛后,消耗0.05 mol/L NaOH 标准溶液体积(mL);V2—试剂空白试验加入甲醛后,消耗0.05 mol/L NaOH 标准溶液的体积(mL);m—称取腐乳质量(g);0.014—与1 mL NaOH 标准溶液(CNaOH=1.000 mol/L)相当的氮的质量(g)。
计算结果保留2 位有效数字。
(3)食盐计算

式中:X3—试样中食盐(以NaCl 计)的含量(g/100g);C—AgNO3标准溶液浓度(mol/L);V1—测定试样消耗的AgNO3标准溶液体积(mL);V2—空白样消耗的AgNO3标准溶液体积(mL);0.0585—与1 mL AgNO3标准溶液(CAgNO3=1.000 mol/L)相当的NaCl 的质量(g)。
计算结果保留2 位有效数字。
1.2.3 模拟研究不同因素对磷酸铵镁结晶产生的影响
1.2.3.1 N、P、Mg 储备液的配制
选择MgCl2·6H2O、Na2HPO4·12H2O、NH4Cl 为反应药剂[11-12],设定Mg2+的基准物质浓度为0.041 118 mol/L(1 000 μg/mL),称取29.452 3 g Na2HPO4·12H2O 和4.398 8 g NH4Cl 溶解并定容到1 000 mL,配制成浓度为0.082 24 mol/L 的N、P 储备液。另外称取16.718 7 g MgCl2·6H2O 溶解并定容到1 000 mL,配制成浓度为0.082 24 mol/L 的Mg 储备液。
1.2.3.2 pH 值对磷酸铵镁结晶反应的影响
取5 个洁净干燥的250 mL 三角瓶,先分别加入50 mL N、P 储备液,分别以6 mol/L HCl 调节其pH为5.0、5.5、6.0、6.5、7.0,最后于每个三角瓶中依次加入50 mL Mg 储备液混合,摇匀静置24 h。离心取上清液稀释相应倍数,测定氮、磷去除效率,探究pH对磷酸铵镁结晶的影响。
1.2.3.3 氨氮浓度对磷酸铵镁结晶反应的影响
取4 个洁净干燥的250 mL 三角瓶,先分别加入50 mL N、P 储备液,1 瓶不添加NH4Cl,另外3 瓶添加适量NH4Cl,使N∶P 摩尔比分别为1∶1、4∶l、8∶l、16∶l。然后于每个三角瓶中依次加入50 mL Mg 储备液混合,摇匀静置24 h。离心取上清液稀释相应倍数,测定反应后溶液中磷的去除效率,探究氨氮浓度对磷酸铵镁结晶的影响。
1.2.3.4 盐含量对磷酸铵镁结晶反应的影响
取5 个洁净干燥的250 mL 三角瓶,分别加入50 mL N、P 储备液,再分别添加适量NaCl,使溶液中NaCl 质量浓度为8%、10%、12%、14%、16%。最后于每个三角瓶中依次加入50 mL Mg 储备液混合,摇匀静置24 h 进行磷酸铵镁结晶反应。离心取上清液稀释相应倍数,测定反应后溶液中氨氮和磷的去除效率,探究盐含量对磷酸铵镁结晶的影响。
1.2.3.5 酒精含量对磷酸铵镁结晶反应的影响
无水乙醇分别配制0、5°、10°、15°的酒液,取对应储备液模拟磷酸铵镁结晶反应。静置24 h 取上清液稀释相应倍数,测定反应后溶液中氨氮和磷的去除效率,探究酒精含量对磷酸铵镁结晶的影响。
2 实验结果与分析
2.1 不同后酵时间有结晶物青方腐乳相关成分差异分析
2.1.1 腐乳卤汤中氨氮、磷、镁含量变化
对不同后酵时间含结晶物的腐乳卤汤中氨氮含量、磷含量、镁含量、pH 值的测定结果如图1 所示。

图1 不同后酵时间腐乳样品中氨氮浓度、磷、镁含量及pH 值变化Fig.1 Changes of NH4+,Mg2+,PO43- and pH in Sufu samples in different period of fermentation
从图1 中,可以看出:
①随着后酵时间的延长,腐乳卤汤中氨氮浓度持续增加,后酵1 年后青方腐乳卤汤中氨氮浓度达到9 780.5 μg/mL。
②磷含量随着后酵时间的延长,呈现先增加后减少的趋势,卤汤中磷含量最大值为1 198.3 μg/mL(后酵9 个月左右),磷含量最低值为261.2 μg/mL。镁含量呈持续降低趋势,后酵1 年左右卤汤中镁含量最低(38.74 μg/mL)。同时对比磷、镁的摩尔去除比(磷、镁减少量与其相对原子质量的比值),根据磷酸铵镁(MgNH4PO4·6H2O)分子式其摩尔去除比应为1∶1,而实际测得磷、镁摩尔去除比约为30∶7,远高于理论值,说明腐乳卤汤中磷的去除不只是由于生成磷酸铵镁造成的。腐乳中含有较多Ca2+[13],后酵过程中也可能结合PO43-生成磷酸钙沉淀,对磷造成消耗,使其含量降低[14]。
③后酵8 个月以后,腐乳pH 值逐渐升高,在8 ~13 个月之间升高速率较小,13 ~15 个月的升高速率更大。关于腐乳pH 值升高的原因,付春等认为青方腐乳发酵彻底,氨基酸生成量多,氨基酸脱氨基产生氨溶于水成为NH3·H2O,使汤料pH 值升高[14]。
2.1.2 腐乳( 坯体) 中氨基酸态氮、总酸、盐含量的含量变化
对不同后酵时间含结晶物的腐乳(坯体)氨基酸态氮、总酸、盐含量的测定结果如图2 所示。

图2 不同后酵时间腐乳样品中氨基酸态氮、总酸及食盐含量变化Fig.2 Changes of NH4+,total acid and salt in Sufu samples in different period of fermentation
从图2 中可以看出,青方腐乳中氨基酸态氮含量后酵半年后都能达到1 g/100 g 以上。总酸含量持续减少,与样品腐乳中pH 值的变化一致。坯体中食盐含量逐渐下降,可能是由于坯体中食盐浸出到卤汤中所致[15]。同时后酵8 个月时,氨基酸态氮(≥0.60)、总酸(≤1.30)、食盐(≥6.5)都已达到行业要求(SB/T 10170 -2007)。
2.2 模拟研究不同因素对磷酸铵镁结晶产生的影响
前期研究结果表明,不同后酵时间含结晶物的腐乳卤汤及坯体中氨氮浓度、总酸(pH 值)差异明显。同时生产上后酵过程中主要控制的工艺参数是酒精含量和盐含量,不同种类腐乳中酒精含量和盐含量差异很大。主要选取pH 值、氨氮浓度、酒精含量、盐含量等因素为研究对象,在去离子水中模拟磷酸铵镁反应,探究其对磷酸铵镁结晶的影响。
2.2.1 pH 值对磷酸铵镁结晶反应的影响
根据不同后酵时间含结晶物的腐乳卤汤pH 值变化(见图3),在模拟实验中设置pH 范围为5.0 ~7.0。
图3 表明,在实验pH 值范围内,pH 对于磷酸铵镁生成有非常强的依存性,随着pH 值的降低,磷和氨氮的去除率均减小,P 的去除率由30%降为5%,N的去除率由22%降为0.81%。当pH 值从6.5 降至6.0 时,氨氮和磷的去除率急剧降低,当pH5.0 时氨氮的去除率仅为0.81%。同时观察对比模拟反应后三角瓶中结晶物生成现象,发现pH≤6.0 时三角瓶底部无结晶物生成,可以考虑通过用降低腐乳卤汤中的pH 值的方法来控制腐乳结晶物的生成。此外,王凤翼[16]在研究金枪鱼罐头中鸟粪石结晶时,指出当pH 值为5.9 到6.1 或更低时,不易看到磷酸铵镁结晶生成。这也与我们得到的结论一致。

图3 pH 值对氨氮和磷去除率的影响Fig.3 Effect of pH on removal rate of NH4+ and P
前期研究表明,青方腐乳后酵6 个月,pH 值上升到6.0 以上并随着后酵时间的延长持续升高,说明青方腐乳中磷酸铵镁结晶的产生可能与pH 值升高有关。
2.2.2 氨氮浓度对磷酸铵镁结晶反应的影响
设定溶液中P 的浓度为0.082 24 mol/L,Mg∶P=1∶1(摩尔比),N∶P 的摩尔比为1∶1、4∶1、8∶1、16∶1,模拟磷酸铵镁结晶反应,测定磷的去除率结果如图4所示。

图4 氨氮浓度对磷去除率的影响Fig.4 Effect of NH4+ on removal rate of P
从图4 中可以看出随着N∶P 摩尔比的增大,磷的去除率从25%上升到75%,大幅增加,证明氨氮浓度对磷酸铵镁结晶反应影响很大。
氨氮浓度对磷酸铵镁结晶反应的影响相关文献报道较多,王建森等[17]指出氨氮浓度增大能够有效控制反应程度和反应速度。对于NH4+浓度对磷酸铵镁结晶反应所致的影响,目前还不清楚其作用机理。
青方腐乳发酵较为彻底,腐乳卤汤中氨氮浓度很高,有利于反应获得较多的磷酸铵镁结晶,这可能是青方腐乳结晶物增多的主要原因。
2.2.3 盐含量对磷酸铵镁结晶反应的影响
根据不同后酵时间腐乳样品中食盐含量的变化(图5),设定盐含量分别为8 g/100 mL、10 g/100 mL、12 g/100 mL、14 g/100 mL、16 g/100 mL 进行模拟实验。
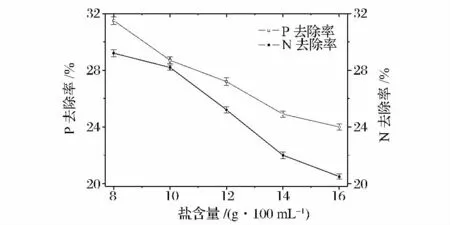
图5 盐含量对氨氮和磷去除率的影响Fig.5 Effect of salt content on removal rate of NH 4+ and P
由图5 可以看出,盐含量对磷酸铵镁结晶反应有一定影响,在实验盐含量范围内,随着盐含量的升高磷和氨氮的去除率均减小,减少幅度不是很大,盐含量增加1 倍,氨氮和磷的去除率约降低8%。NaCl含量增加主要改变溶液中离子强度,姚涛、王建森也都通过各自的研究证明溶液离子强度对磷酸铵镁结晶有影响[17-18]。此外Kabdasli 等人[19]实验研究了溶液中Na+、Cl-、SO2-4 等对磷酸铵镁结晶反应的影响,发现Na+浓度高于50 mmo1/L 时,磷酸铵镁结晶反应受到明显的抑制。
2.2.4 酒精含量对磷酸铵镁结晶反应的影响
在青方腐乳生产中,会把酒精含量作为一个主要的控制参数,加酒可以抑制微生物的生长,同时能使腐乳具有特殊的香味,加酒量一般控制在卤汤的12%左右,因此选取酒精含量0、5°、10°、15°,进行磷酸铵镁结晶反应的模拟实验。
图6 表明,在实验酒精含量范围内,随着酒精含量升高氨氮和磷去除率有增大趋势,但氨氮和磷去除率变化幅度不大,氨氮去除率由37%增大到41%,磷去除率由47.5%增大到52%,说明酒精含量对磷酸铵镁结晶反应虽有影响但其影响程度较小。
实际生产中白方腐乳酒精含量远大于青方腐乳酒精含量,只考虑酒精含量因素,白方腐乳结晶物现象理论上应该要比青方更严重,但是实际情况却是白方腐乳几乎不出现结晶物现象,可能与白方腐乳的发酵时间短有关。

图6 乙醇含量对氨氮和磷去除率的影响Fig.6 Effect of alcohol content on removal rate of NH4+ and P
3 结论
(1)分析对比了不同后酵时间腐乳样品的相关成分差异,证明了随着后酵时间的延长青方腐乳发酵程度高,其卤汤中氨氮浓度及pH 值显著升高,磷含量先增加后减少,镁含量持续降低;腐乳坯体中总酸含量、食盐含量持续下降,氨氮含量初期增加随后减少。初步推测结晶物的形成与否主要与腐乳样品中氨氮和总酸含量有关,腐乳发酵彻底与否(发酵程度)可能是影响结晶物产生的决定性因素。
(2)探究了pH 值、氨氮浓度、酒度、盐度等因素对磷酸铵镁结晶反应的影响。实验结果表明,pH 对于磷酸铵镁生成有非常强的依存性,pH≤6.0 时氨氮和磷的去除率降到较低值,同时无结晶物生成,通过调节pH 值可以控制磷酸铵镁结晶的产生;氨氮浓度对磷酸铵镁结晶反应的影响程度很大,发酵彻底氨氮浓度增大可能是青方腐乳结晶物产生量大的主要原因;盐度和酒度对磷酸铵镁结晶反应影响效果不显著,低盐度高酒度有利于磷酸铵镁结晶的生成。
[1] 李幼筠. 中国腐乳的现代研究[J]. 中国酿造,2006(1):4 -7.
[2] 鲁绯. 腐乳发酵机理、品质改进和模式识别研究[D].北京:中国农业大学,2005:23 -25.
[3] 林影,卢荣德. 腐乳产品的氨基酸分析与白点研究[J]. 中国调味品,1999(9):13 -14.
[4] 鲍松林,丁霄霖. 腐乳白点成分鉴定[J]. 无锡轻工业学院学报,1993,12(4):270 -275.
[5] 汪景泉,毛霉驯化及微波对腐乳白点抑制效果的研究[D]. 重庆:西南大学,2009:17 -20.
[6] 袁振远,凌希利,张水华. 腐乳汁液中的结晶物[J]. 调味副食品科技,1982(01). 3 -6.
[7] 黄永涛,卢红梅. 腐乳中结晶物的研究[J]. 中国酿造,2012,31(2):59 -62.
[8] 马勇. 青方腐乳酿造技术研究[J]. 中国调味品,1996,(4):21 -23.
[9] 王福荣. 生物工程分析与检测[M]. 北京:中国轻工业出版社,2005:89 -93.
[10] SB/T10170 -2007. 腐乳[S].
[11] 邹安华,孙体昌,邢奕,等. pH 对MAP 沉淀法去除废水中氨氮的影响[J]. 环境科学动态,2005 (4):4 -6.
[12] 袁鹏,宋永会,袁芳,等. 磷酸铵镁结晶法去除和回收养猪废水中营养元素的实验研究[J].环境科学学报,2007,27(7):1127 -1134.
[13] 王瑞芝. 中国腐乳酿造[M]. 北京:中国轻工业出版社,1998:135 -140.
[14] Wild D,Kisliakova A,Siegrist H.P - fixation by Mg,Ca and zeolite A during stabilization of excess sludge from enhanced biological P - removal[J].Water Science and Technology,1996,34:391 -398.
[15] 付春. 青方腐乳汤料的配制技术中国酿造[J].2005(3):39 -41.
[16] 王凤翼. 缩合磷酸盐对罐头食品质量的影响[J]. 食品工业科技,1983(5):47 -54.
[17] 王建森,宋永会,袁鹏,等. 基于PHREEQC 程序的磷酸铵镁结晶法污水处理工艺模型化研究[J]. 环境科学学报,2006,26(02):208 -213.
[18] 姚涛,蔡伟民,李龙海. 磷酸胺镁法处理含氮磷废水的研究进展[J]. 中国给水排水,2005,21 (2):31 - 33.
[19] Kabdasli I,Parsons S A,Tünay O. Effect of major ions on struvite crystallization[A]. International Conference for struvite:Its Role in Phosphorus Recovery and Recuse[C].Cranfield university,UK. 2004.
