氮掺杂C20富勒烯的几何结构和稳定性
2013-10-28顾娇娇李宝兴马志伟
顾娇娇,李宝兴,马志伟
(杭州师范大学理学院,浙江 杭州 310036)
氮掺杂C20富勒烯的几何结构和稳定性
顾娇娇,李宝兴,马志伟
(杭州师范大学理学院,浙江 杭州 310036)
应用密度泛函理论,对氮掺杂富勒烯C20的几何结构和稳定性进行系统研究.研究结果表明:C20富勒烯的结构随着掺杂氮原子个数的增多,结构畸变越来越严重;氮原子的掺杂使团簇失去电子变得不容易,氧化能力降低,还原能力增强;氮原子的掺杂在一定程度上增强了团簇的稳定性.
C20富勒烯;氮掺杂;几何结构;氧化性
0 引 言
富勒烯分子有许多奇异的性质,在化学、物理及材料科学等多个领域中受到广泛关注.在富勒烯的大家族中,C20分子是其中最小的一个[1].
2000年,Prinzbach等[2]成功地合成了C20富勒烯分子,开辟了C20富勒烯研究的新领域.但是,由于C20富勒烯由12个五边形构成,具有非常大的张力,不是很稳定.因此,寻找稳定的C20类似物,即C20的异质富勒烯具有重要意义.虽然氮和碳在元素周期表中相邻,氮的最外层电子数比碳的只多了一个,但是它们的物化性质相差很大.在很多碳化合物中,碳通常显负电性,但在碳氮化合物中,碳一般又显正电性.这主要是由氮的电负性比碳的电负性大的性质造成的[3-5].正是氮的这种性质使它掺杂富勒烯的研究受到广泛关注.Huo等[6]在对nN@C20(n=2,4,6)进行电子传输特性研究时发现:N原子的掺入有利于提高分子的传输性能,并且掺入的N原子数越多,传输性能就越好.科技工作者同样研究了部分碳原子被替代后的特性.Ewels等[7]提出富勒烯分子中氮原子的替代违背IPR规则,即稳定的富勒烯应该满足:一个五边形被5个六边形包围,和其他五边形不相邻.而Jiang[8]等提出富勒烯中的碳原子被杂质原子取代服从所谓TCS规则,即掺杂电负性的杂环原子可以使由于五边形造成的不稳定结构变得稳定.Keremu[7]等人用TRE方法对C20-2xN2x(x=1-4)的磁性研究结果支持了TCS规则.同时,Keremu[7]等人的研究还表明:原本具有反磁性的C20,在掺N杂质后,C18N2仍表现为反磁性,而C16N4、C12N6、C12N8则表现为顺磁性.越来越多的研究结果表明,氮原子的掺入可以调控富勒烯的物理和化学性质,这些异质富勒烯可望在超导、光电子器件和有机铁磁体等方面得到广泛应用.但是,目前C20富勒烯中掺杂质N原子的个数只局限于偶数[9-16].为全面探究C20富勒烯掺杂质氮原子后的特性,笔者首次系统地对富勒烯C20进行掺连续个氮杂质原子的研究,得到了一系列C20-xNx(x=1-9)的结构,并探讨了它们的物性.
1 计算方法
应用基于第一性原理的阿姆斯特丹密度泛函程序(Amsterdam Density Functional, 简称ADF),对最小的碳富勒烯C20进行掺氮杂质原子的研究,得到了一系列C20-xNx(x=1-9)的结构,并进一步讨论了它们的特性.ADF计算程序是目前国际上公认用于团簇研究的一种先进程序.在计算过程中,考虑到原子或者分子的电子并不是均匀体系,建立在均匀电子气模型上的LDA 近似得不到精确的结果,所以采用了在LDA近似基础上依赖于电荷密度梯度的广义梯度近似(GGA)和Becke-Perdew(B-P)交换关联泛函.
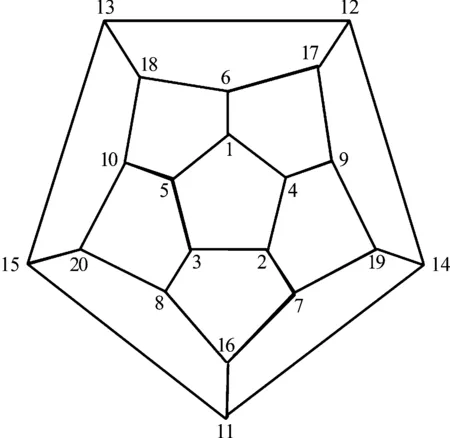
图1 C20的原子编号Fig. 1 Atom number of C20 fullerene
2 结果与讨论
2.1 模 型
C20富勒烯分子由12个五边形构成,分子中共有120个电子,共占据60个分子轨道.在此以C20的Ih构型为基础,通过替代方式来构造C20-nNn(n=1-9)的各种初始结构.
C20结构的原子编号如图1所示,两个原子间的位置关系只有5种.A关系:相邻 (如图1中的1-5,1-4等).B关系:相间(如图1中的1-3,1-17等).C关系:如图1中的1-7,1-8等.D关系:如图1中的1-16,1-14等.E关系:如图1中的1-11.这5种不同位置替代的排列组合构成了C20-nNn(n=1-9)的各种异构体.
2.2 几何结构

图2 C20-nNn (n=1-9)的各种异构体中最稳定的结构Fig.2 The most stable structure of C20-nNn (n=1-9) ismoers
图2给出了C20-nNn(n=1-9)各种异构体的最稳定结构.从图中可以看出,一个氮原子替换C20中碳原子所得到的结构保持原有完整的笼型,没有明显畸变.C18N2各异构体的最稳定结构由2个氮原子替换C20中D类位置的碳原子获得,这与梁等用B3LYP /6-31G*方法得到的结果相符[17].当掺入的氮原子个数为3个时,得到了14个异构体,其中优化后的最稳定结构如图2 中的C17N3所示.该结构出现了氮氮键,笼型发生畸变,但仍闭合.当氮原子个数增加到4个时,得到的最稳定结构如图2中的C16N4所示,它的结合能为-156.03eV.该结构仍为笼型,4个氮原子分别相邻、相隔1个、2个、或3个碳原子.而对于梁等用B3LYP/6-31G*方法在C18N2的基础上构造获得的最稳定结构[17],笔者用ADF程序计算其结构,其结合能为-154.96eV.这说明文中得到的C16N4最稳定结构比梁等得到最稳定结构还要稳定.图2中的C15N5是5个碳原子被氮原子替代得到的最稳定结构.它是一个开口的笼子,开口处有2个氮原子相邻,另外2个氮原子和第5个氮原子相隔1个碳原子.C20中6个碳原子被氮原子替代时,生成了128种异构体.这些异构体优化后的最稳定结构如图2中的C14N6所示.从图2中可以明显看出笼子打开,存在多处畸变,但是还保留着7个五边形.图2中的C13N7是C20中7个碳原子被氮原子替代得到的最稳定结构.该结构开口处,伸出2个支链,其中1条支链由2个相邻的氮原子连着1个碳原子组成,另1条支链由2个氮原子间隔着1个碳原子组成.该结构中剩余3个氮原子都分散在笼型最外圈上.图2中的C12N8是C20中8个碳原子被氮原子替代得到的最稳定结构.该结构开口处,伸出1条支链,它由2个氮原子间隔着1个碳原子组成.笼型开口处分散着各相隔1个碳原子的4个氮原子.当掺入的氮原子个数达到9个时,得到的异构体中最稳定的结构如图2中的C11N9所示.这时笼型结构基本不存在,它由4个五边形和3条支链组成,存在2个氮氮键,1个在支链上,另1个在五边形内.
根据以上的描述、分析,可以得出:C20富勒烯随着氮原子替换碳原子数目的增多,笼型结构逐步破坏,替代原子越多,破坏越严重.由于氮原子的3个键是呈三角锥形,超过2个氮原子无法共面是造成笼型结构破坏的主要原因.当氮原子替换碳原子数目达到9个时,笼型结构几乎完全被破坏.由此,可以预测当氮原子替换碳原子数目超过9个时,笼形结构也是不存在的.所以在此没有继续研究氮原子替换碳原子个数超过9个的情况.
2.3 稳定性
为研究C20-nNn(n=1- 9)团簇结构的稳定性,从团簇的结合能、能量的二阶差分和能隙对团簇进行详细的研究.相应的数据如表1所示,相应的曲线图如图3所示.
表1C20-nNn(n=1-9)的最稳定结构的结合能、能量二阶差分和能隙
Tab.1Thebindingenergy,second-orderenergydifferenceandbandgapofthemoststablestructureofC20-nNn(n=1-9)ismoers
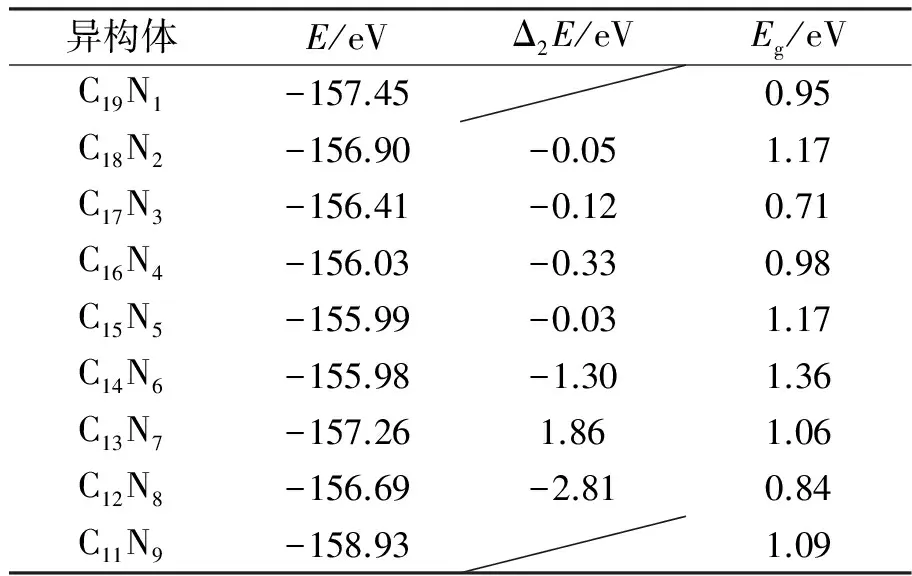
异构体E/eVΔ2E/eVEg/eVC19N1-157.450.95C18N2-156.90-0.051.17C17N3-156.41-0.120.71C16N4-156.03-0.330.98C15N5-155.99-0.031.17C14N6-155.98-1.301.36C13N7-157.261.861.06C12N8-156.69-2.810.84C11N9-158.931.09
图3(a)给出C20-nNn(n=1-9)最稳定结构的结合能,图中虚线为C20团簇和N20团簇基态结构结合能的连接线.从中可以看出当氮原子替换碳原子个数不超过6个时,团簇结合能比理论值要高.但当氮原子替换碳原子的个数是7、8、9个时,团簇结合能比理论值要低,团簇更稳定.究其原因,可以从键能的角度找到答案.当有1个氮原子替换碳原子时,断裂的是2个碳碳单键,形成的是1个碳氮单键和碳氮双键.根据原子半径判断,碳碳之间的距离大于碳氮间的距离,碳碳单键的键能小于碳氮键的键能.当氮原子替换碳原子的个数不超过6个时,团簇受笼形张力的影响,增加的键能被张力作用抵消,结合能比理论值要高.但当氮原子替换碳原子的个数是7、8、9个时,笼形打开,张力左右减弱,增加的键能使团簇结合能比理论值要低,团簇更稳定.团簇结合能的二阶差分Δ2E也可以很好地反映团簇的稳定性.定义C20-nNn(n=1-9)团簇的能量二阶差分Δ2E为:


图3 C20-nNn(n=1-9)的最稳定结构的结合能、能量二阶差分和能隙Fig. 3 The binding energy,second-order energy difference and bandgap of the most stable structure of C20-nNn(n=1-9) isomers
Δ2E(C20-nNn)=E(C20-(n-1)N(n-1))+E(C20-(n+1)N(n+1))-2E(C20-nNn)
图3(b)给出了C20-nNn(n=1-9)基态结构的二阶能量差分,从中可以得出当氮原子替换碳原子的个数是7个时,团簇的稳定性最好.结合图2可以发现,C13N7团簇的几何结构中出现了两条支链,这两条支链不受笼形结构张力的影响,原子间结合能高.这可能是7个碳原子被替换时稳定性增加的原因之一.
能隙Eg与团簇结构的稳定性有关,它的大小反映了电子从占据轨道向空轨道发生跃迁的能力,在一定程度上代表分子的化学动力学反应活性.能隙越大,反应活性越低,团簇越稳定.C20-nNn(n=1-9)团簇的能隙Eg为最高占据轨道(HOMO)和最低未占据轨道(LUMO)之差.
图3(c)给出C20-nNn(n=1-9)的最稳定结构的能隙.总的来看,掺杂团簇的能隙要比C20团簇能隙大,说明掺杂使团簇化学动力学反应活性降低.从局部去分析,掺入的氮原子个数为3、8个时,能隙与C20团簇能隙相比变化不大,团簇化学动力学反应活性降低不明显;替换的氮原子个数为2、5、6、7、9个时,能隙值比C20团簇能隙值至少提高了50%,团簇的化学动力学反应活性明显降低.究其原因,可以从团簇的电子云图找到答案.如图4所示,以C19N1为例.基态C原子的外层电子结构为2s22p2,合成C20时C原子发生了sp2杂化.每个C原子只用去了3个键,还有1个p轨道剩余,分布在外围和腔内形成离域π键.需要指出的是,C20中的sp2杂化轨道不是严格的120°,因为形成笼形三锥结构,存在张力,有变形,实际键角为106°27′.
当掺杂1个N原子时,由于基态N原子的外层电子结构为2s22p3,成键时4个价电子轨道发生sp3杂化,得到4个sp3杂化轨道,其中3个sp3杂化轨道与相邻的3个C原子形成σ键.受其影响,与这3个C原子相邻的6个C原子也由原来π键变为σ键,大大降低了团簇的化学动力学反应活性.N原子的第4个sp3杂化轨道被弧对电子所占有,该弧对电子未参与σ键成键,电子云密集于N原子周围,使碳原子的电子云密度降低,在化学性质上表现为氧化反应变难,还原反应变易.

图4 团簇的电子云图Fig. 4 The electronic cloud of clusters
3 结 论
应用基于第一性原理的阿姆斯特丹密度泛函程序(ADF),对氮原子掺杂富勒烯C20的几何结构和稳定性进行了系统研究.结果发现:(1)当氮原子替换碳原子的个数小于等于6个时,团簇结合能比理论值要高.但当氮原子替换碳原子的个数是7、8、9个时,团簇结合能比理论值要低,团簇更稳定;(2)当氮原子替换碳原子的个数是7个时,团簇出现了2条支链,结合能和二阶能量差分都出现了突变;(3)当氮原子替换碳原子的个数为2、5、6、7、9个时,团簇能隙值比C20团簇的明显要高,失去电子变得不容易,氧化能力降低,还原能力增强;(4) 当氮原子替换碳原子的个数是9个时,团簇的笼型结构基本被破坏.
[1] Xie Suyuan, Gao Fei, Lu Xin. Capturing the Labile Fullerene[50] as C50Cl10[J]. Science,2004,304(30):699.
[2] Prinzbach H, Weller A, Landenberger P,etal. Gas-phase production and photoelectron spectroscopy of the smallest fullerene C20[J]. Nature,2000,407:60-63.
[3] Devos A, Lannoo M. Electron-phonon coupling for aromatic molecular crystals: Possible consequences for their superconductivity[J]. Physical Review B,1998,58:8236-8239.
[4] Chen Zhongfang, Jiao Haijun, Michael B,etal. Theroretical investigation into structures and magnetic properties of smaller fullerenes and their heteroanalogues[J]. Theoretical Chemistry Accounts,2001,106(5):352-363.
[6] Huo Xinxia, Wang Chang, Zhang Xiumei,etal. Impact of electronic structure and transmission characteristic based on N-doping in the C20fullerene molecule[J]. Journal of natural science of heilongjiang university,2009,26(3):402-406.
[7] Christopher P E. Nitrogen Violation of the Isolated Pentagon Rule[J]. Nano Lett,2006,6(5):890-895.
[8] Xu Jiannong, Jiang Yuansheng. Topological Stabilization of Fullerenes[J]. Journal of Chemical Information and Computer Sciences,1995,35:214-216.
[9] Knapp C, Dinse K P, Pietzak B. Fourier transform EPR study of N@C60in solution[J]. Chemical Physics Letters,1997,272(5-6):433-437.
[10] Mauser H, Eikema H, Clark T. Stabilization of Atomic Nitrogen Inside C60[J]. Angew Chem Int Ed Engl, 1997,36(24): 2835-2838.
[11] Suzuki T, Li Q, Khemani K C. Systematic Inflation of Buckminsterfillerene C60: Synthesis of Diphenyl Fulleroids C61to C66[J]. Science,1991,254(5035):1186-1188.
[12] Pattanyak J, Kar T, Scheiner S. Substitution in mono-BN-fullerenes:Cn(n=20, 24, 28,32,36 and 40 )[J]. J Physics Chemical A,2004,108(38):7681-7685.
[13] Xu Shuhong, Zhang Mingyu, Zhao Yuanyuan. Super-valence phenomenon of carbon atoms in C20molecule[J]. Journal of Molecular Structure Theochem,2006,760:87-90.
[14] Pattanyak J, Kar T, Scheiner S. Boron-nitrogen(BN) substitution of fullerenes: C60to C12B24N24CBN ball[J]. J Physics Chemical A,2002,106(12):2970-2978.
[15] Chen Z, Ma K, Pan Y,etal.Therpretical studies on the BN substituted fullerenes C70-2x(BN)x(x=1-3)-isoelectronic equivalents of C70[J]. Journal of Molecular Structure Theochem,1999,490(1/3):61-68.
[16] Andreas H, Berthold N. Nitrogen Heterofullerenes[J]. Accounts of Chemical Research,1999,32,795-804.
[17] 梁云霄,水淼,李榕生.硼/氮掺杂富勒烯C20的结构和稳定性[J].物理化学学报,2007,23(10):1647-1651.
GeometricalStructuresandStabilityofNitrogen-dopedC20Fullerene
GU Jiaojiao, LI Baoxing, MA Zhiwei
(College of Science, Hangzhou Normal University, Hangzhou 310036, China)
The paper investigated the geometry structures and stability of nitrogen-doped C20fullerene by using density functional theory. It is found that the more numbers of nitrogen atoms, the more serious distortion of the structure. The clusters, the oxidation capacity of nitrogen-doped clusters reduces while the reducing capacity of nitrogen-doped clusters enhancements. In certain extent,nitrogen doping enhances the stability of clusters.
C20fullerene; Nitrogen-doped; geometrical structure; oxidation capacity
2012-10-19
浙江省自然科学基金项目(Y6100098).
李宝兴(1960—),男,教授,博士,主要从事团簇物理性质方面研究.E-mail:phybxli01@yahoo.com.cn
10.3969/j.issn.1674-232X.2013.02.011
O469
A
1674-232X(2013)02-0140-05
