胶质瘤大鼠模型射频热疗的最佳作用时间及最适温度初步研究
2013-09-23张正雄
张正雄, 游 洋
目前,胶质瘤的治疗仍以手术为主,但有部分患者不能耐受或不愿手术。射频热疗是近些年发展起来的治疗胶质瘤的新方法,其创伤小,患者耐受性好,目前临床已开始应用。然而,在射频热疗过程中存在治疗时间及温度控制随意性大,主观性强,尚没有严格的标准,患者易产生脑水肿等严重并发症等问题。本研究通过建立胶质瘤大鼠模型,使用不同的温度和作用时间对荷瘤大鼠进行处理,以期探明胶质瘤大鼠射频热疗的最佳作用时间及最适作用温度,为临床应用提供参考依据。
1 材料和方法
1.1 材料 SD大鼠156只,4周龄,雄性,体重(245±10)g,由东南大学实验动物中心提供[SYXK(苏)2007-0011]。C6细胞株购自中科院上海细胞库;胎牛血清购自杭州四季青公司;马血清、F12-K培养基、胰蛋白酶、PBS均购自GIBCO公司。江湾I型C动物立体定向仪、leksell射频仪(东南大学附属中大医院神经外科),牙科磨钻(东南大学附属中大医院口腔科),7.0T德国bruker公司生产实验小动物专用磁共振(东南大学医学院医学影像系),电子分析天平、恒温烘箱(东南大学医学院中心实验室)。
1.2 胶质瘤细胞培养 C6胶质瘤细胞培养于5%CO2气体浓度,37℃培养箱,培养液为加入15%马血清及2.5%胎牛血清的F-12K培养液。于细胞指数生长期胰酶消化并收集细胞,制成105个/μL细胞悬液以供种植肿瘤(悬液不含血清)。
1.3 胶质瘤模型建立 所有大鼠术前禁食禁水,麻醉前30 min肌肉注射阿托品0.05 mg抑制呼吸道分泌,并在实验的过程中每小时肌肉注射阿托品0.05 mg维持。腹腔注射戊巴比妥(40 mL·kg-1)进行麻醉,体温控制在37.5℃。麻醉后将大鼠固定于江湾Ⅰ型立体定位仪上,头部正中1 cm切口切开头皮,暴露前囟,以前囟为原点,向后1.5 mm,向右旁开3.0 mm用牙科磨钻打一直径为1 mm的小孔。微量进样针将10 μL细胞悬液缓慢注入硬脑膜下5 mm(进6mm,退1mm)处的脑组织中,停针5 min后退针,骨蜡封闭骨孔,清洗切口后缝合。
1.4 建模判定 大鼠出现活动减少,进水饮食进行性减少等情况,体重亦在术后10 d减少,再经MRI及病理验证,判定建模是否成功。
1.5 分组及处理 建模成功大鼠随机分成4组:44℃组、58℃组、72℃组、86℃组,每组36只。各组的36只大鼠再随机分成6个小组,每组6只,射频持续时间分别为 50 s、70 s、90 s、110 s、130 s、150 s。
1.6 射频热疗方法 按以上分组对荷瘤大鼠进行射频热凝:腹腔注射4%戊巴比妥钠(40 mg·kg-1),将荷瘤大鼠麻醉后,固定于立体定向仪框架,将三维坐标调零。常规消毒后切开头皮约1 cm,剥离骨膜,用牙科磨钻将原建模时的骨孔扩大为直径3 mm的骨孔,沿此孔将射频电极缓慢步进至预定坐标,开启射频仪,按以上分组条件分别给予射频热凝,结束后缓慢退出射频电极,钻孔使用骨蜡覆盖,常规缝合伤口。整个过程在超净工作台内进行,术后无需抗生素防治感染。
1.7 大鼠脑水含量测定 大鼠术后12小时行磁共振扫描,测量肿瘤毁损灶直径。术后24小时后,以颈椎离断法处死大鼠,立即完整摘取整个脑组织,称湿重,记为WW水肿,再将标本切碎放于90℃烘箱48 h,至恒重后测干重(DW水肿)。脑组织含水量(S水肿)按公式:S水肿= [(WW水肿- DW水肿)/WW水肿] ×100%计算。
1.8 统计学方法 使用SPSS11.5对数据进行统计分析,结果以均数±标准差(x±s)表示,各组间比较使用方差分析,两两比较使用q检验,以P<0.05为差异有统计学意义。
2 结果
2.1 建模结果 因感染、手术操作等因素,术后有3只大鼠死亡,15天后所有剩余153只建模大鼠给予磁共振检查,其中4只大鼠磁共振未见异常表现,余149只大鼠磁共振异常(图1)。随机选取3只断头处死后解剖了解C6胶质瘤成瘤情况,见脑接种处均已成瘤。建模成功率为95.5%。
2.2 各组肿瘤毁损灶直径的比较(表1) 各组毁损灶直径随热疗持续时间增长呈增大趋势,44℃组、58℃组呈持续增大(P<0.05),72℃组、86℃组在90 s后增大趋于平缓(P>0.05)。
2.3 各组脑水含量的比较(表2) 同一热疗时间下,各组间脑水含量无统计学差异(均P>0.05)。脑水含量随热疗持续时间增长呈增加趋势,90 s后各组均增加较剧烈,130 s以后趋于平缓。
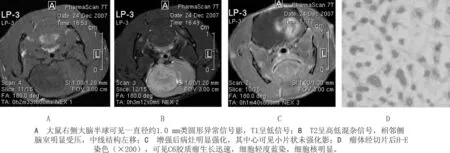
图1 建模成功大鼠影像学及病理学表现

表1 不同温度和作用时间下各组毁损灶最大直径(单位:mm)

表2 不同温度和作用时间下各组脑水含量表(单位:g)
3 讨论
目前,胶质瘤的治疗仍以手术治疗为主,但由于肿瘤呈浸润性生长,与脑组织无明确分界,难以彻底切除,术后进行放射治疗、化学治疗、免疫治疗极为必要,但各种疗法均难以达到根治目的,这已成为神经科学最富挑战性又亟待解决的问题[1]。
利用射频治疗肿瘤是肿瘤局部透热治疗的一种,以影像学引导或直接将电极针导入肿瘤组织,通过射频在电极针周围产生极性分子震荡而发热,从而使细胞内蛋白质变性、细胞膜脂质双层溶解,产生细胞凝固性坏死,达到治疗肿瘤的目的[2]。肿瘤组织具有微血管发育不良和其呈缺氧、低营养、低pH的特点,使瘤细胞对热的耐受性低,比正常细胞更易被杀伤,对热更具有敏感性[3]。
目前微创射频热凝治疗脑肿瘤在临床上已见使用,但仍存在诸如温度点的选择、术后并发症防治等问题[4]。本实验针对肿瘤射频热凝治疗的具体加热温度、加热时间进行大鼠模型研究。对C6胶质瘤模型大鼠分别行44℃,58℃,72℃,86℃ 4个温度条件下 50 s、70 s、90 s、110 s、130 s 及 150 s 6 种时间的射频加热。结果表明:各组毁损灶直径随热疗持续时间增长呈增大趋势,44℃组、58℃组呈持续增大,72℃组、86℃组在90 s以后增长趋于平缓。且同一热疗时间下,各组间脑水含量差异无统计学意义(均P>0.05)。脑水含量随热疗持续时间增长呈增加趋势,90 s以后各组均增加较剧烈,130 s以后趋于平缓。因此认为,(1)脑水肿的发生与热疗持续时间关系密切,而与温度改变关系不大。(2)要获得最佳热疗效果同时尽量减少脑水肿发生,建议提高热疗温度而减少热疗持续时间。
射频热凝疗法增加了脑转移瘤和脑胶质瘤治疗的方法,该疗法创伤小,疗效确切。但是,射频热凝疗法治疗脑转移瘤和脑胶质瘤仍有并发脑水肿等许多不足之处,需要不断总结经验加以改进。对此我们还将进一步深入研究,以逐步探求人脑胶质瘤及转移瘤射频热凝的最佳作用温度及作用时间。以便术者尽可能排除影响手术安全的因素,保证手术质量,减少手术并发症。
[1] 周洪语,罗其中,沈建康.恶性脑肿瘤治疗新进展[J].中华神经外科杂志,2001,17(5):332-334.
[2] 张智坚,吴孟超,陈汉,等.经皮肝穿刺射频热凝治疗肝脏肿瘤[J].中华外科杂志,2001,39(10):749-752.
[3] Gerweck LE.Modification of cell lethality at elevated temperatures:the pH effect[J].Radiat Res,1977,70(1):224-235.
[4] 王东成,李广玉,侯宽省,等.微创射频热凝治疗脑转移瘤和脑胶质瘤6例分析[J].临床医学,2004,24(11):34-35.
