腰舒胶囊质量标准研究*
2013-09-14郭剑华刘渝松马善治彭文忠廖兴隆
郭 亮 ,郭剑华 ,刘渝松 ,马善治 ,林 於 ,刘 新,彭文忠 ,王 健 ,廖兴隆 ,胡 晓
(1.重庆市中医骨科医院,重庆 400010;2.重庆医科大学,重庆 400016)
腰舒胶囊由丹参、党参、当归、川牛膝、狗脊、槲寄生、制川乌、全蝎、熟地黄9味药材组方,为中药复方医院制剂,具补肝肾、益气血、祛风湿、通经络之功效,临床用于腰椎间盘突出症祛风通络、舒筋活血,疗效显著。采用薄层色谱(TLC)法对制剂中的川牛膝、当归、狗脊、党参、槲寄生、丹参进行定性鉴别,采用高效液相色谱(HPLC)法测定制剂中有效成分丹参酮ⅡA的含量,旨在为该制剂的质量控制和评价奠定基础。现报道如下。
1 仪器与试药
SY-810型高效液相色谱仪(瑞利分析仪器公司);AG135型1/10万天平(Mettler Toledo公司)。腰舒胶囊及各阴性样品(重庆市中医骨科医院制备);川牛膝对照药材(批号为121066-200203)、当归对照药材(批号为120927-200512)、狗脊对照药材(批号为121071-200502)、党参对照药材(批号为121057-200303)、槲寄生对照药材(批号为121075-200402)、丹参酮ⅡA对照品(批号为20041207),均由中国药品生物制品检定所提供;乙腈为色谱纯,水为重蒸水,其余试剂均为分析纯。
2 方法与结果
2.1 薄层色谱鉴别
川牛膝:取胶囊内容物20 g,加乙醇100 mL,加热回流1 h,放冷,滤过,滤液蒸干,残渣加水50 mL使溶解,用乙酸乙酯30 mL萃取,弃去乙酸乙酯液,水液继续用水饱和的正丁醇30 mL萃取,分取正丁醇液,蒸干,残渣加乙醇2 mL使溶解,作为供试品溶液。取不含川牛膝的阴性样品,同法制备阴性对照品溶液。取川牛膝对照药材2 g,加乙醇50 mL,加热回流1 h,放冷,滤过,滤液蒸干,残渣加乙醇2 mL使溶解,作为对照药材溶液。照薄层色谱法试验,吸取供试品溶液、阴性对照品溶液、对照药材溶液各5~10 μL,分别点于同一以0.3%羧甲基纤维素钠为黏合剂的硅胶G薄层板上,以石油醚(60~90℃)-乙酸乙酯-甲醇-浓氨(12∶6∶3∶0.5)为展开剂,浓氨水预平衡20 min,展开至12~14 cm,取出,晾干,喷以香草醛硫酸试液,在105℃加热至斑点清晰。供试品溶液色谱中,在与对照药材溶液色谱相应位置上显相同颜色的斑点,置紫外光灯(365 nm)下检视显相同颜色的荧光斑点,阴性对照品溶液色谱则无此斑点(图A1-A2)。
当归:取胶囊内容物20 g,加乙醇100 mL,加热回流1 h,放冷,滤过,滤液蒸干,残渣加水50 mL使分散,用石油醚(60~90℃)50 mL萃取,分取石油醚液,蒸干,残渣加乙醇2 mL使溶解,作为供试品溶液。取不含当归的阴性样品,同法制备阴性对照品溶液。取当归对照药材2 g,加乙醇50 mL,加热回流1 h,放冷,滤过,滤液蒸干,残渣加乙醇2 mL使溶解,作为对照药材溶液。照薄层色谱法试验,吸取供试品溶液及阴性对照品溶液各10~15 μL、对照药材溶液5~10 μL,分别点于同一以0.3%羧甲基纤维素钠为黏合剂的硅胶G薄层板上,以环己烷-乙酸乙酯(10∶1)为展开剂,展开至10~12 cm,取出,晾干,再喷以香草醛硫酸试液,在105℃加热至斑点清晰。供试品溶液色谱中,在与对照药材溶液色谱相应位置上显相同颜色的斑点,置紫外光灯(365 nm)下检视显相同颜色的荧光斑点,阴性对照品溶液色谱则无此斑点(图B1-B2)。
狗脊[1]:取胶囊内容物20 g,加乙醇100 mL,加热回流1 h,放冷,滤过,滤液蒸干,残渣加水50 mL使分散,用石油醚30 mL萃取,弃去石油醚液,分取水液,加乙酸乙酯50 mL萃取,分取乙酸乙酯液,蒸干,残渣加乙醇2 mL使溶解,作为供试品溶液。取不含狗脊的阴性样品,同法制备阴性对照品溶液。取狗脊对照药材2 g,加乙醇50 mL,加热回流1 h,放冷,滤过,滤液蒸干,残渣加乙醇2 mL使溶解,作为对照药材溶液。照薄层色谱法[1]试验,吸取供试品溶液、阴性对照品溶液、对照药材溶液各10~15 μL,分别点于同一以0.3%羧甲基纤维素钠为黏合剂的硅胶G薄层板上,以环己烷-乙酸乙酯(20∶2)为展开剂,展开至10~12 cm,取出,晾干,喷以香草醛硫酸试液,在105℃加热至斑点清晰。供试品溶液色谱中,在与对照药材溶液色谱相应位置上显相同颜色的斑点,置紫外光灯(365 nm)下检视显相同颜色的荧光斑点,阴性对照品溶液色谱则无此斑点(图C1-C2)。
党参:取胶囊内容物6 g,加正丁醇40 mL,超声处理30 min,滤过,滤液水浴浓缩至约1 mL,作为供试品溶液。取不含党参的阴性样品,同法制成阴性对照品溶液。另取党参对照药材2 g,加正丁醇20 mL,超声处理30 min,滤过,滤液水浴浓缩至1 mL,作为对照药材溶液。照薄层色谱法[1]试验,吸取供试品溶液及阴性对照品溶液 10~20 μL、对照药材溶液 10~15 μL,分别点于同一以0.3%羧甲基纤维素钠为黏合剂的硅胶G薄层板上,以正丁醇-乙醇-水(15∶3∶2)为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液,在105℃加热至斑点显色清晰。供试品溶液色谱中,在与对照药材溶液色谱相应位置上显相同颜色的斑点,阴性对照品溶液色谱则无此斑点(图D)。
槲寄生:取胶囊内容物5 g,加乙醇50 mL,加热回流1 h,滤过,取滤液,加盐酸3 mL,加热回流1 h后浓缩至约10 mL,加水20 mL,用石油醚(60~90℃)萃取3次,每次20 mL,石油醚萃取液蒸干,残渣加乙醇1 mL使溶解,作为供试品溶液。取不含槲寄生的阴性样品,同法制备阴性对照品溶液。取槲寄生对照药材1.5 g,加乙醇30 mL,加热回流1 h,滤过,滤液蒸干,残渣加乙醇1 mL使溶解,作为对照药材溶液。照薄层色谱法[1]试验,吸取供试品溶液及阴性对照品溶液各10 μL、对照药材溶液5 μL,分别点于同一以0.3%羧甲基纤维素钠为黏合剂的硅胶G薄层板上,以氯仿-甲醇(40∶1)为展开剂,展开,取出,晾干,喷以5%磷钼酸乙醇溶液,在110℃加热至斑点显色清晰。供试品溶液色谱中,在与对照药材溶液色谱相应位置上显相同颜色的斑点,阴性对照品溶液色谱则无此斑点(图E)。
丹参[2]:取胶囊内容物6 g,加乙醇30 mL,加热回流1 h,放冷,滤过,滤液蒸干,残渣加水20 mL使分散,用乙醚30 mL萃取,分取乙醚层,低温蒸干,残渣加乙醇2 mL使溶解,作为供试品溶液。取不含丹参的阴性样品,同法制备阴性对照品溶液。取丹参酮ⅡA对照品,加乙酸乙酯制成每1 mL含2 mg的溶液,作为对照品溶液。照薄层色谱法[1]试验,吸取供试品溶液及阴性对照品溶液各10 ~15 μL、对照品溶液 10 μL,分别点于同一以 0.3%羧甲基纤维素钠为黏合剂的硅胶G薄层板上,以苯-乙酸乙酯(19∶1)为展开剂,展开,取出,晾干。供试品溶液色谱中,在与对照品溶液色谱相应位置上显相同颜色的斑点,阴性对照品溶液则无此斑点(图F)。
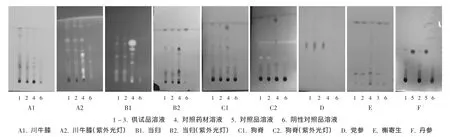
图1 薄层色谱鉴别图
2.2 丹参酮ⅡA含量测定
2.2.1 色谱条件与系统适用性试验
色谱柱:Amethyst C18柱(250 mm ×4.6 mm,5 μm);流动相:甲醇 - 水(9 ∶1);流速:1 mL/min;检测波长:270 nm;进样量:20 μL。该色谱条件下,理论板数按丹参酮ⅡA峰计算应不低于8 000,葛根素峰分离良好,阴性无干扰(见图2)。

图2 高效液相色谱图
2.2.2 溶液制备
取胶囊内容物7 g,碾细,精密称定,用乙醇50 mL回流提取30 min,滤过,残渣再用50 mL乙醇超声处理5 min,滤过,合并滤液,置蒸发皿中蒸干,残渣加水30 mL使分散,转入分液漏斗中,蒸发皿用30 mL乙醚反复洗涤,洗涤液并入分液漏斗中,再用60 mL乙醚分两次萃取,合并乙醚萃取液,蒸干,残渣用甲醇分次使溶解并转移至25 mL容量瓶中,加甲醇至刻度,摇匀,滤过,取续滤液,即得供试品溶液。精密称取丹参酮ⅡA对照品适量,用甲醇制成每1 mL含4 μg的溶液,即得对照品溶液。
2.2.3 方法学考察
线性关系考察:精密称取丹参酮ⅡA对照品适量,用甲醇制成每 1 mL 含 1.0,3.0,4.0,5.0,10.0 μg/mL 的系列对照品溶液,在选订的色谱条件下分别进样20 μL,记录色谱图。以丹参酮ⅡA吸收峰面积积分值为纵坐标 Y、进样质量浓度 X为横坐标绘制标准曲线,线性回归方程为 Y=127 210.6 X,r=0.999 6结果表明,丹参酮ⅡA质量浓度在 1.0 ~10.0 μg/mL 范围内与其峰面积积分值线性关系良好。
精密度试验:吸取同一丹参酮ⅡA对照品溶液,重复进样5次,记录丹参酮ⅡA的峰面积积分值。结果的 RSD为 0.27%(n=5),表明仪器的精密度良好。
稳定性试验:取同一刚制备的供试品溶液,分别于0,4,8,12,24 h在选订的色谱条件下进样20 μL,记录丹参酮ⅡA的峰面积积分值。结果的 RSD为1.3%(n=5),表明供试品溶液在24 h内保持稳定。
重复性试验:取同一批样品,精密称定,依法制备5份供试品溶液,在选订的色谱条件下分别进样20 μL,记录丹参酮ⅡA的峰面积积分值。结果的 RSD为1.0%(n=5),表明方法重现性良好。
加样回收试验:取已知丹参酮ⅡA含量的样品6份,精密称定,分别精密加入丹参酮ⅡA对照品的甲醇稀释液,依法制备6份供试品溶液并测定,记录丹参酮ⅡA的峰面积积分值。结果平均回收率为92.8%。
2.3 样品含量测定[3]
取中试样品3批,依法测定丹参酮ⅡA含量。结果见表1。

表1 中试样品含量测定结果
3 讨论
本制剂当中川牛膝、当归、狗脊、党参、槲寄生、丹参的薄层色谱鉴别方法学考察表明,薄层色谱斑点分离良好,斑点圆整清晰,阴性无干扰,同时试验样品均能检出相应色谱斑点,表明选订的方法具有专属性和重现性,可作为腰舒胶囊制剂质量控制的定性检测方法。
测定丹参酮ⅡA含量采用的是高效液相色谱法。供试品甲醇提取后离心取上清液,再用石油醚萃取,溶液澄清,且用此方法制备供试品溶液简单、快速,测定结果准确,供试品溶液中目标峰与相邻色谱峰分离度大于1.5。因此,该方法可用于本制剂质量控制的含量测定方法。
本试验中建立了鉴别制剂中川牛膝、当归、狗脊、党参、槲寄生、丹参的薄层色谱鉴别方法,能鉴别出其特征性斑点;建立了测定丹参酮ⅡA含量的高效液相色谱法,精密度、稳定性、重现性均符合要求。因此,上述两种方法为制订腰舒胶囊的质量标准提供了理论依据。
[2]周 玲,李桂芳.宁心通痹胶囊丹参和川芎的薄层色谱鉴别[J].中华医药杂志,2009,9(8):56 -58.
[3]国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2010:70.
