中央型肺癌应用IMRT和3-DCRT 实现SBRT的剂量学比较
2013-09-11李腊枚黄高明周光华
李腊枚,黄高明,周光华
(湖南师范大学第二附属医院,解放军第163 医院肿瘤科,湖南 长沙 410003)
在中国每年约有600,000 位患者死于肺癌[1]。很多患者因为心肺功能不全无法手术治疗[2]。随着科技的发展,很多不能手术切除的患者也能通过新兴的非手术方法治愈。在这些新兴的方法中,立体定向放射治疗(Stereotactic Body Radiation Therapy,SBRT)取得了最大的成绩。本研究通过比较同一个体在IMRT 与3-DCRT 技术下的SBRT 计划的优缺点,为临床SBRT 治疗个体化放疗方案的选择提供剂量学方面的依据。
1 材料与方法
1.1 临床资料
选择2011年12月至2012年10月在湖南师范大学第二附属医院肿瘤科收治的30例中央型肺癌患者(30 个病灶)。男性13例,女性17例;年龄45-76 岁。所有患者均经纤维支气管镜病理学诊断确诊为肺癌,腺癌9例,鳞癌21例。肿瘤体积为25.68-103.63cm3,平均65.61 cm3,肿瘤直径3cm 以下的9例,3-5cm的15例,5-7cm的6例。
1.2 仪器设备
Siemens 公司KD-ⅡMevatron 型医用直线加速器;GAMMEXA3000A 型可移动激光定位系统;拓能公司的venus 三维治疗计划系统;瓦里安Eclipse 逆向治疗计划系统;西门子16 排螺旋扫描螺旋CT 机;配套三维固定架,真空袋固定装置。
1.3 靶区和周围危及器官的勾画
所有患者均在CT 定位下扫描,图像资料刻录光盘传至TPS 治疗计划系统,由放疗医师参考ICRU50、62、83 号报告,在计划系统内逐层勾画出大体肿瘤体积(gross tumor volume,GTV)、临床靶体积(clinical target volume,CTV)、计划靶体积(planning target volume,PTV)和周围危及器官(organ at risk,OAR)包括脊髓,两侧肺、心脏和食管。CTV 为在GTV 边缘腺癌病灶外扩8mm,鳞癌外扩6mm。CTV 边缘外扩10mm 为计划靶区PTV。
1.4 治疗计划设计
每一套图像分别7 野、9 野IMRT 计划和6 野3-DCRT 计划。各计划PTV 均给予处方剂量60Gy/12 次,隔日照射1 次。PTV 及各危及器官的优化限制条件为处方剂量至少覆盖95%的PTV;PTV 接受>110%的处方剂量的体积应<20%;PTV 接受<93%的处方剂量的体积应<3%;PTV 外的任何地方不能出现>110%的处方剂量;肺接受>20Gy的体积数<30%;脊髓的最大剂量<40Gy;全食管的受量<30Gy,食管接受>50Gy的体积数<50%;心脏1/3的体积≤60Gy。计划经本科物理师和两位主治以上医师认可。
1.5 治疗计划评价参数
(1)靶区剂量的比较:①评估PTV的最大和最小剂量D2%、D98%(D2%和D98%分别为2%和98%的PTV 体积的受照剂量[8]以及D50% 。②比较三种计划的靶区剂量体积参数VX%(代表X%处方剂量所包绕的靶区体积)。③适形指数(CI)和不均匀指数(HI)。
适形指数(conformity index,CI):用以评价靶区与参考等剂量曲面的适形程度(公式1)。VPTV-REF/VPTV ×VPTV-REF/VREF (1) 式中VPTV 为靶体积,VPTV-REF 为参考等剂量线50Gy 所包绕的靶区体积,VREF 为参考等剂量线50Gy 包绕的所有区域体积。CI的取值在0~1 之间,等于1 时表示等剂量线面所包绕的区域与靶区完全一致,等于0 时表示等剂量线所包绕的区域与靶区没有重叠。CI 越接近1,适形度越高。
不均匀指数(homogeneity index,HI):用以评价PTV 内剂量分布均匀性(公式2)。
HI=D2%-D98%/D50%(2)式中D2% 、D98%分别为2%、8%PTV 所受到的照射剂量,D50%为中位剂量,HI 值越大说明超过处方剂量越大,PTV 内剂量分布也越不均匀。
(3)重要器官受照剂量的比较:①观察全肺平均剂量(mean lung dose,MLD)以及接受大于V5、V10、V20、V30、V40、V50 分别为接受5、10、20、30、40、50Gy 剂量照射的正常肺体积占全肺总体积的百分比。②观察食管平均剂量(Dmean)、V50、V60、D2%用于评价各计划的食管受照射情况。③观察心脏接受大于35Gy的照射体积占全心脏体积的百分比(V35),D1/3 为心脏1/3的体积所接受的照射剂量。④观察脊髓的平均剂量(Dmean)以及1cc 体积的受照射剂量(D1cc)。
1.6 统计学方法
所有结果均以mean±SD表示,对结果采用SPSS13.0 统计软件进行方差分析,SNK-Q 检验进行组间两两比较。P<0.05 为差别有统计学意义。
2 结果
2.1 PTV 各参数、CI、HI的比较
三组计划均能满足剂量学要求,IMRT 计划与3-DCRT 计划比较,前者的PTV 最大剂量、平均剂量均较后者提高[表1];IMRT 计划靶区的CI 平均值高于3-DCRT 计划,而靶区HI 平均值正相反[表1]。
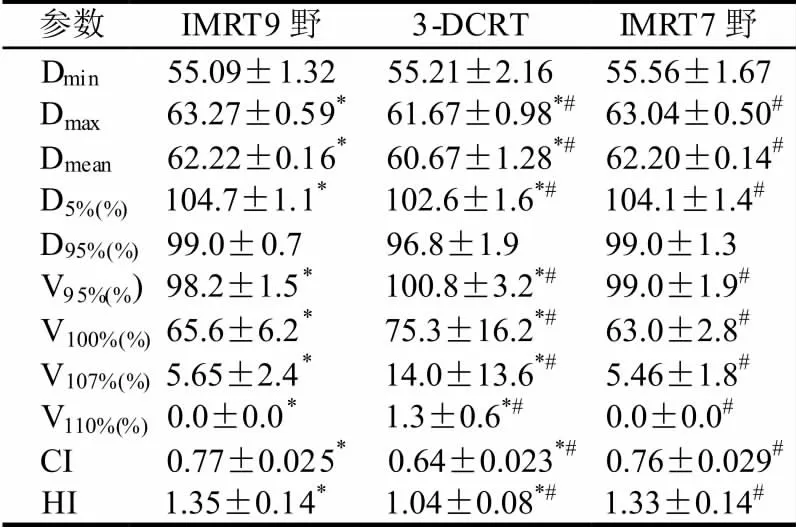
表1 三种放疗计划PTV 剂量比较(mean±SD)
2.2 全肺、食管、脊髓、心脏各参数的比较
三种治疗计划对全肺的照射情况,IMRT 计划对正常肺组织的照射剂量和照射体积均较3-DCRT 小,而7 野IMRT 计 划 比9 野IMRT 计 划V5、V10 值小[表2];食管受照射情况比较显示,IMRT 计划较3-DCRT 计划对食管的照射剂量低,照射体积小[表3];脊髓受照射情况比较显示,IMRT 计划较3-DCRT 计划对脊髓的照射剂量低,照射体积小[表4];心脏受照射情况比较显示,9 野IMRT 计划较3-DCRT和7 野IMRT 计划对心脏的照射剂量高,照射体积大[表5];各项计划均能满足SBRT 在中央型肺癌中应用的剂量学要求,7 野IMRT 计划较其他两项计划在剂量学方面更有优势,对周围组织的保护更好。
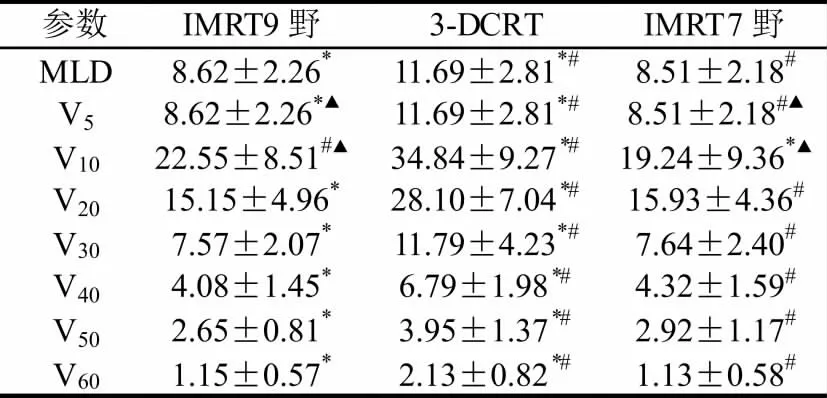
表2 三种治疗计划全肺剂量比较(mean±SD)
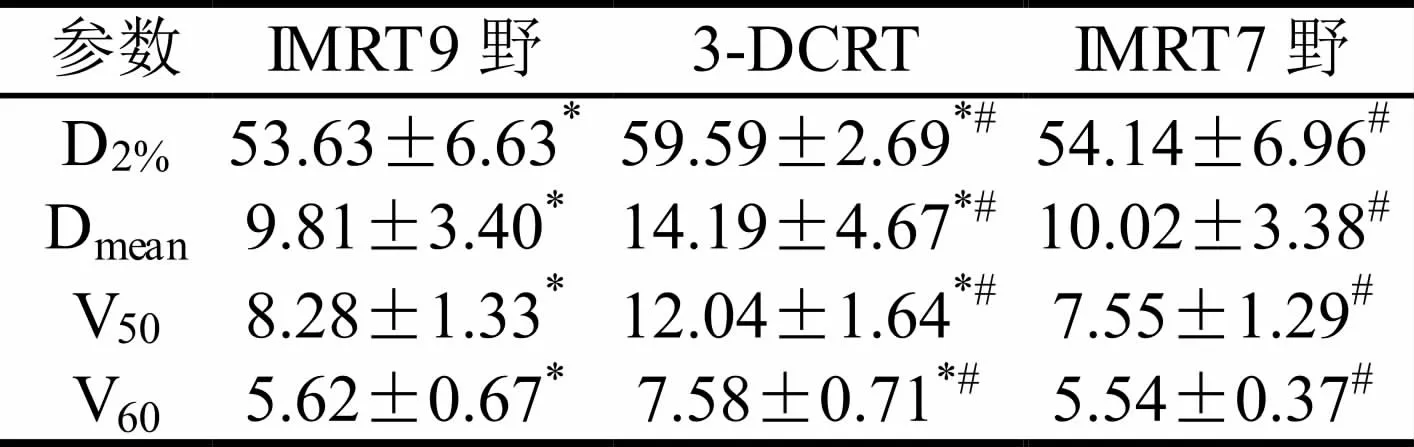
表3 三种治疗计划食管剂量比较(mean±SD)
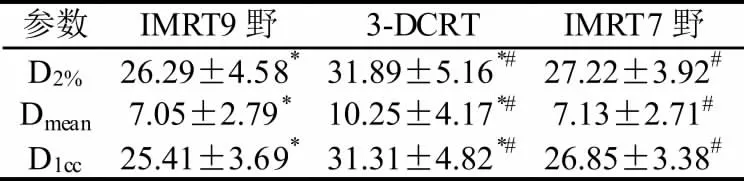
表4 三种治疗计划脊髓剂量比较(mean±SD)
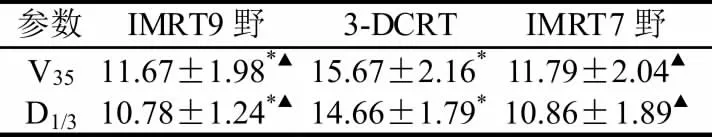
表5 三种治疗计划心脏剂量比较(mean±SD)
3 讨论
SBRT 是以采用现代影像学技术正确发现靶区,通过立体定位及验证技术精确瞄准靶区,通过计算机控制驱动特殊射线装置高剂量摧毁靶区,将放疗副作用及放射损伤降到最低为技术特征的现代放疗过程。采用高分次剂量治疗模式是SBRT的最大特征。在本研究中,三组计划均能满足超过95%的PTV 满足处方剂量要求。9 野IMRT、3-DCRT和7 野IMRT 计 划的 靶 区Dmax、Dmin、Dmean 均能满足剂量学要求。而周围危及器官的受照射剂量和体积均小于研究所设定的阈值,9 野IMRT、3-DCRT和7 野IMRT 计划的肺V20 值、脊髓D2%、食管V50 值、心脏D1/3 值均小于实验所设定的肺V20<30%、脊髓D2%<40Gy、食管V50<50%、心脏D1/3≤60Gy 等剂量学要求,故从剂量学角度来分析SBRT 可以应用于中央型肺癌。
SBRT 采用高分次剂量模式主要从以下几方面提高疗效:首先,SBRT 可以提高放疗的BED(生物等效剂量)值,达到根治的目的,取得与手术治疗相当的疗效;其次,SBRT 可以缩短治疗时间,有对抗常规分割放疗肿瘤细胞加速增殖的生物学优势;再次,SBRT 或许存在一种新的克服乏氧细胞放射耐受机制[1];最后,大分割放疗在促进肿瘤免疫应答方面也发挥着作用[2]。研究证实,常规分割放疗采用与SBRT 放疗相同的设备和技术时,前者也不能取得与后者一致的满意疗效[3]。SBRT 放疗(SBRT 放疗是每次放疗的剂量大于常规分割的剂量,间隔2天以上照射1 次)分割方式可以提高肿瘤的LC和完全缓解率(CR),其值分别达85%-100%[4-5]和62.5%[3]。产生这一差距的原因是,在放疗总剂量相同的情况下,SBRT 所对应的BED 值更高[4]。有三方面依据可以解释这一现象:第一种支持这一结论的理论依据是肿瘤倍增时间理论,SBRT 放疗可以缩短治疗时间,有对抗常规分割放疗肿瘤细胞加速增殖的生物学优势。第二种理论依据是线性二次模型的估计误差理论,Brown[1]认为SBRT 放疗时或许存在一种新的克服乏氧细胞放射耐受机制。第三种理论依据是免疫应答增强机制理论,Michael[2]认为SBRT 放疗在促进肿瘤免疫应答方面也发挥着作用。但是,在放疗毒副反应相关研究中显示:中央型和周围型肺癌放疗后3年内2 或3 级放射性肺炎的累积发病率分别为25%和13%[6],因此,SBRT 应用与中央型肺癌时技术的选择应该更加慎重。
在本研究中,各组计划均能满足处方要求,处方剂量至少覆盖95%的PTV;PTV 接受>110%的处方剂量的体积<20%;PTV 接受<93%的处方剂量的体积<3%;PTV 外的任何地方均没有出现>110%的处方剂量。IMRT组高剂量曲线包绕PTV 较3-DCRT 更为紧密,边缘形成的剂量梯度更陡。这中现象量化的表达就是HI和CI 值,以往的研究均采用ICRU 第62 号报告来确定靶区的适形指数(CI)和均匀性指数(HI),但在ICRU 第83 号[7]报告指出,在精确放射治疗如:3-DCRT、IMRT 等放疗技术中,不再报告PTV的最大剂量和最小剂量,而用接近二者的D2%和D98%来代替。故HI 计算为HI=D2%-D98%/D50%,我们的研究中9 野IMRT,3-DCRT,7 野IMRT 计划的适形指数(CI)分别为0.77±0.025,0.64±0.023,0.76±0.029,IMRT 各组的靶区适形度较3-DCRT 计划高,说明IMRT 计划在三维方向上高剂量分布的形状与靶区的吻合度优于3-DCRT 计划,在这种高度适形的基础上,IMRT技术下增加靶区的剂量更为安全有效,有利于肿瘤的局部控制。9 野IMRT,3-DCRT,7 野IMRT 计划的HI 值分别为1.35±0.14,1.04±0.08,1.33±0.14,IMRT 较3-DCRT 技术靶区剂量的均匀性下降,即在IMRT 计划中靶区内的剂量线分布更为紧密,而接近靶区边缘时,剂量梯度突然增加,剂量线的分布突然减少,IMRT 计划中靶区的剂量曲线均较3-DCRT 包绕靶区更加紧密,接近靶区周围时梯度更大,在靶区部分剂量分布更集中,剂量率也越高,故正常肺组织的受照剂量和体积也更少。
虽然我们的研究在剂量学上证实了SBRT 可以应用于中央型肺癌,但是,我们的研究目前仅限于剂量学方面的研究,SBRT 技术的开展对设备、技术、人员的要求很高,在临床上广泛开展的条件还不是很成熟,需要开展大规模的临床观察研究来证实其临床上的实用性和安全性,相信随着设备、技术的进步,人才的培养,SBRT 在NSCLC中的应用会取得突破。
[1]Brown JM,Koong AC.High-dose single-fraction radiotherapy:exploiting a new biology [J].Int J Radiat Oncol Biol Phys,2008,71(2):324-325.
[2]Milano MT,Constine LS,Okunieff P,et al.Normal tissue toxicity after small field hypofractionated stereotactic body radiation[J].Radiat Oncol,2008,3:36.
[3]Shen Y,Zhang H,Wang J,et al .Hypofractionated radiotherapy for lung tumors with online cone beam CT guidance and active breathing control[J].Radiat Oncol,2010,5:19.
[4]Onishi H,Araki T,Shirato H,et al.Stereotactic hypofractionated high-dose irradiation for stage I nonsmall cell lung carcinoma:clinical outcomes in 245 subjects in a Japanese multiinstitutional study [J].Cancer,2004,101 (7):1623-1631.
[5]Chang JY,Balter PA,Dong L,et al.Stereotactic body radiation therapy in centrally and superiorly located stage I or isolated recurrent non-small-cell lung cancer[J].Int J Radiat Oncol Biol Phys,2008,72(4):967-971.
[6]Baba F,Shibamoto Y,Oqino H,et al.Clinical outcomes of stereotactic body radiotherapy for stage I non-small cell lung cancer using different doses depending on tumor size[J].Radiat Oncol,2010,5:81.
[7]Journal of the ICRU Report 83.[M]Oxford University Pressd,2010:(10) 1:1-106.
