浅谈摩尔教学中的五步教学法
2013-09-01丁宇
丁 宇
(鞍山师范学院附属卫生学校,辽宁 鞍山 114001)
摩尔是联系宏观物质质量与微观粒子个数之间关系的重要的桥梁和纽带,是中职卫校学生在化学第一课所要学习的内容。物质的量、摩尔、摩尔质量、阿伏伽德罗常数、气体摩尔体积、摩尔浓度等一系列抽象概念的出现,往往会使这些原本化学基础不扎实的学生感到茫然,继而对化学的学习丧失信心。因此,如何循序渐进地引导学生理解这部分内容,是笔者在教学中不断思考的问题。在教学中笔者采取逐层导入式五步教学法,收到较好的效果,课后卷面考核成绩显示,学生掌握情况较好。
在20世纪80年代之前近30年的时间里,有这样一个难题长期困扰着科学家:我们具体做实验的单质或化合物宏观上大多都是肉眼可见并可称其质量或量其体积的,而事实上化学反应是微观的原子、分子或离子按照一定的数目比进行的,这些粒子又是肉眼看不见且难以称量的,如何知道一定质量的物质中到底含有多少数量的微粒,或者一定数量的某种微粒其对应质量有多少,以便宏观上予以称量。换句话说,宏观上可称量的物质质量和微观上微粒数量之间到底存在什么关系?

1 导入物质的量和摩尔的概念
物质的量就是联系宏观和微观的一个物理量,它是微观世界中的一个计数单位,不同于物质的质量、物质的数量。它的符号为n,单位为摩尔(简称摩,mol)。学生可通过例举(见表1)对比,对这个新接触到的物理量有基本的了解。

表1 基本物理量及其单位名称
表1显示,通过与熟悉的物理量进行对比,使学生对这个新学的物理量不再感到抽象。同时通过例举让学生熟悉有关物质的量的符号、单位及表达方式。
2 导入阿伏伽德罗常数
根据教材[1]中关于摩尔的定义,已知12C的原子量为12,一个12C原子的真实质量为1.9993×10-23g,则12g12C所含原子数为:12/1.9993×10-23=6.02×1023个。
为纪念意大利科学家阿伏伽德罗,把此数记为:NA=6.02×1023/mol。表示1mol任何物质含6.02×1023个微粒,从而可得出微粒个数N的计算公式:N=n·NA。
物质的量就是以集团的方式对微观粒子进行计数的单位,一个微粒集团的数量就等于阿伏伽德罗常数,记为1mol。这种计数方法与宏观世界里某些计数单位,如“打”、“令”、“箱”等有着相似的地方。
3 导入摩尔质量的概念
以氢气和氧气在点燃的条件下反应生成水为例(见表2),从初中所学的微观粒子的知识过渡到物质的量。

表2 微观粒子数与物质的量的关系推导
探寻表2中物质的质量和物质的量之间的关系,不难发现,物质的质量与物质的量之比为该物质的相对原子量或分子量。即1mol物质的质量当以克为单位时在数值上等于其粒子的相对质量,定义该物理量为摩尔质量,符号M,单位为g/mol(或kg/mol)。计算式为:M=m/n。事实上,只要研究对象明确,物质的量(M)是一个已知量,所以上式可整理为:n=m/M。
总结前3步的内容,可整理如下:
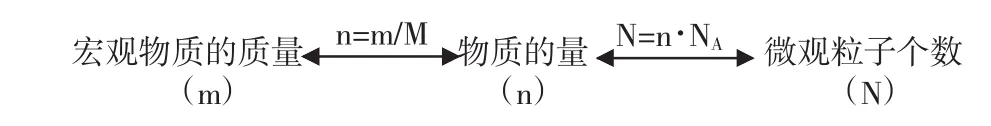
通过物质的量这一纽带,沟通了宏观物质的质量和微观粒子个数之间的关系,解决了理论与实际联系中的一个难题。
4 导入气体摩尔体积的概念
物质的摩尔体积由3方面因素决定:(1)物质所含微粒个数;(2)微粒本身的大小;(3)微粒之间的间距。以100个篮球和排球分别密集排列和间隔10m分散排列为例,说明为什么相同物质的量的不同固体和液体体积千差万别,而不同气体的体积却相差不大。3个因素中,由于气体的微粒间距远大于微粒本身,从而可以忽略微粒自身体积,因此不同气体体积类似。而固体和液体由于微粒间比较密集,自身体积不能忽略,导致体积也各不相同。
研究表明,在标准状况下(0℃,101.3kPa),各种气体体积都约为 22.4L,习惯上称为气体的摩尔体积,记为:Vm,0=22.4L/mol。由此在标准状况下,气体的体积可用公式计算,即V=n·Vm,0。在非标准状况下,只要在相同温度和相同压力下,相同体积的任何气体都含有相同数目的分子,这就是阿伏伽德罗定律[1]。
5 导入液体摩尔浓度的概念
物质的量浓度又称为摩尔浓度,经过以上4个步骤的学习学生理解摩儿浓度就比较简单了。其计算公式为:c=n/V。n为溶质的物质的量,单位为mol;V指溶液的总体积,单位为升(L),因此,摩尔浓度的单位为mol/L。
根据上述五步知识的分层导入,不难发现物质的质量、微观粒子数、标准状况下气体的体积,以及液体的摩尔浓度,这些物理量无不与物质的量(n)有着千丝万缕的关系(见图1)。
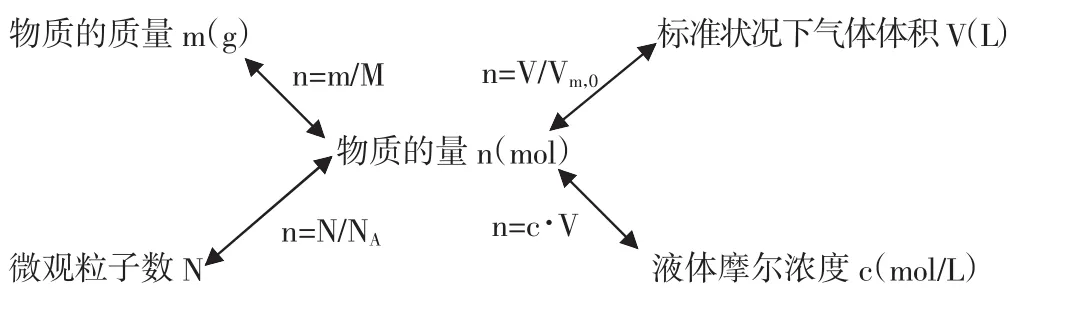
图1 有关物质的量的各物理量关系
由图1可知,物质的量是紧密联系其他物理量的重要纽带,从宏观到微观,从气体到液体,相关的计算中无不出现它的身影,其重要性可见一斑。学生在熟练掌握5个概念的同时,只要牢牢记住这一关系网,就可以通过物质的量这座桥梁,利用4个计算公式去计算所需要的物理量。
需要说明的是,上述物理量在使用时必须标明基本单元数,即研究对象的名称,把其化学式写在各符号的右下标处(或在符号后加括号,在括号内标明物质名称)。在用五步法讲课时,必须同步引入大量的例题,由简到繁,带领学生逐步理解消化,切不可光讲概念和提纲。这种循序渐进的五步教学法,使摩尔这一单元的难点得以分解,提高了教学效果,也激发了学生学习化学的兴趣。
[1]张锦楠.化学[M].北京:人民卫生出版社,2002.
