红花清肝十三味丸质量标准研究
2013-08-28史文凤
刘 颖, 胡 琴*, 史文凤
(1.北京市药品检验所,北京 100035;2.长治医学院,山西长治 046000)
红花清肝十三味丸来源于《蒙医验方》,1984年收载入《内蒙古蒙成药标准》,2001年收载入《中华人民共和国卫生部药品标准》(蒙药分册)。原标准收载了显微鉴别以及两个理化鉴别[1]。为控制药品的内在质量,对处方中红花、丁香、木香、诃子、栀子、紫檀香、人工牛黄进行了薄层色谱鉴别,并采用高效液相色谱法测定了制剂中栀子苷、羟基红花黄色素A、丁香酚。所建立的方法具有操作简便、分离效果好、重复性好,专属性强,准确等优点,可以有效地控制本品的质量。
1 仪器与试药
岛津LC—20A高效液相色谱仪,配备二极管阵列检测器 (PDA)型;聚酰胺薄膜 (浙江省台州路桥四甲生化塑料厂);硅胶G预制板 (烟台市化学工业研究所);硅胶G预制板 (青岛海洋化工厂分厂)。
对照品:羟基红花黄色素A(批号111637-200502)、丁香酚 (批号725-200209)、去氢木香内酯 (批号:111525-200706)、木香烃内酯 (批号:111524-200503)、没食子酸 (批号:110831-200803)、栀子苷 (批号:110749-200714)、胆酸(批号:100078-200414)、猪去氧胆酸 (批号100087-200610)。对照药材:红花 (批号120907-200609)、丁香 (批号121039-200503),木香 (批号120921-200607)、诃子 (批号121015-200503)。对照品与对照药材均购于中国食品药品检定研究院。
红花清肝十三味丸样品共11批:A(批号:20120203);B(批号:110525 071,110526 027);C(批 号:10455001,10455002);D(批 号:110825,110420,110419);E(批 号:110925,111056,110946)。
甲醇为色谱纯,水为超纯水,其他试剂均为分析纯。
2 薄层色谱鉴别
2.1 红花及羟基红花黄色素A的薄层鉴别
取本品3 g,研细,加甲醇10 mL,超声处理30 min,静置,取上清液作为供试品溶液。另取不含红花的阴性制剂,同法制成红花阴性溶液。另取红花对照药材1 g,加甲醇5 mL,超声处理10 min素A对照品,加甲醇制成每1 mL含1 mg的溶液,作为对照品溶液。吸取供试品溶液及红花阴性溶液5 μL,对照药材溶液 2 μL,对照品溶液 1 μL,点于聚酰胺薄膜上,以醋酸展开,喷以3%三氯化铝乙醇溶液,在105℃加热至斑点显色清晰,置紫外光灯 (365 nm)下检视。供试品在与对照药材及对照品色谱相应的位置上,显相同颜色的荧光斑点。缺红花阴性样品无相应斑点。见图1。

图1 红花清肝十三味丸中红花及羟基红花黄色素A的TLC图谱Fig.1 TLC chromatogram of Carthami Flos and hydroxysafflor yellow A
2.2 丁香及丁香酚、木香及去氢木香内酯的薄层色谱鉴别[2-4]
分别取不含丁香、木香的阴性制剂各3 g,研细,加甲醇10 mL,超声处理30 min,静置,取上清液,分别作为丁香阴性溶液及木香阴性溶液。另取丁香对照药材、木香对照药材各1 g,分别加甲醇5 mL,超声处理10 min,静置,取上清液作为对照药材溶液。再取丁香酚对照品、去氢木香内酯对照品,分别加甲醇制成每1 mL含1 mg的溶液,作为对照品溶液。吸取2.1项下供试品溶液,丁香阴性溶液、木香阴性溶液及两种对照药材溶液各10 μL,两种对照品溶液各5 μL,点于硅胶 G板上,以环己烷-甲酸乙酯-甲酸 (15∶5∶1)展开,喷以5%香草醛硫酸溶液,在105℃加热至斑点显色清晰。供试品在与对照药材及对照品色谱相应的位置上,显相同颜色的斑点。缺丁香及缺木香阴性样品无相应斑点。见图2。
2.3 诃子及没食子酸的薄层色谱鉴别

图2 红花清肝十三味丸中丁香、丁香酚、木香、去氢木香内酯的TLC图谱Fig.2 TLC chromatogram of Caryophylli Flos,eugenol,Aucklandiae Radix,dehydrocostuslactone
取不含诃子的阴性制剂3 g,研细,加甲醇10 mL,超声处理30 min,静置,取上清液,作为诃子阴性溶液。另取诃子对照药材1 g,加甲醇5 mL,超声处理10 min,静置,取上清液作为对照药材溶液。再取没食子酸对照品1 mg,用1 mL甲醇溶解,作为对照品溶液。吸取2.1项下供试品溶液、诃子阴性溶液及对照药材溶液各10 μL,对照品溶液3 μL,点于硅胶G板上,以甲苯-乙酸乙酯-甲酸 (5∶4∶1)展开,喷以2%三氯化铁乙醇液,在105℃加热至斑点显色清晰。供试品在与对照药材和对照品色谱相应的位置上,显相同颜色的斑点。缺诃子阴性样品无相应斑点。见图3。
2.4 栀子苷的薄层色谱鉴别
取不含栀子的阴性制剂3 g,研细,加甲醇10 mL,超声处理30 min,静置,取上清液,作为栀子阴性溶液。另取栀子苷对照品,加甲醇制成每1 mL含1 mg的溶液,作为对照品溶液。吸取2.1项下供试品溶液、栀子阴性溶液各10 μL,对照品溶液2 μL,点于硅胶G板上,以乙酸乙酯-丙酮-水(6∶6∶1)展开,喷以10%硫酸乙醇溶液,在105℃加热至斑点显色清晰。供试品在与对照品色谱相应的位置上,显相同颜色的斑点。缺栀子阴性样品无相应斑点。见图4。
2.5 紫檀香的薄层色谱鉴别[5-7]

图3 红花清肝十三味丸中诃子及没食子酸的TLC图谱Fig.3 TLC chromatogram of Chebulae Fructus and gallic acid

图4 红花清肝十三味丸中栀子苷的TLC图谱Fig.4 TLC chromatogram of geniposide
取不含紫檀香的阴性制剂3 g,研细,加甲醇10 mL,超声处理30 min,静置,取上清液,作为紫檀香阴性溶液。另取紫檀香对照药材1 g,加甲醇5 mL,超声处理10 min,静置,取上清液作为对照药材溶液。吸取2.1项下供试品溶液、紫檀香阴性溶液各10 μL,对照药材溶液3 μL,点于硅胶G板上,以甲苯-丙酮 (7∶3)展开,喷以5%香草醛硫酸溶液,在105℃加热至斑点显色清晰。供试品在与对照药材色谱相应的位置上,显相同颜色的斑点。缺紫檀香阴性样品无相应斑点。见图5。
2.6 胆酸、猪去氧胆酸的薄层鉴别
取不含人工牛黄的阴性制剂3 g,研细,加甲醇10 mL,超声处理30 min,静置,取上清液,作为人工牛黄阴性溶液。另取胆酸对照品、猪去氧胆酸对照品,加甲醇制成每1 mL各含1 mg的混合溶液,作为对照品溶液。吸取2.1项下供试品溶液、人工牛黄阴性溶液各10 μL,对照品溶液2 μL,点于硅胶 G板上,以异辛烷-乙酸乙酯-冰醋酸(15∶7∶5)展开,喷以10%硫酸乙醇溶液,在105℃加热至斑点显色清晰,置紫外灯 (365 nm)下检视。供试品在与对照品色谱相应的位置上,显相同颜色的荧光斑点。缺人工牛黄阴性样品无相应斑点。见图6。

图5 红花清肝十三味丸中紫檀香的TLC图谱Fig.5 TLC chromatogram of Pterocarpi indici Lignum
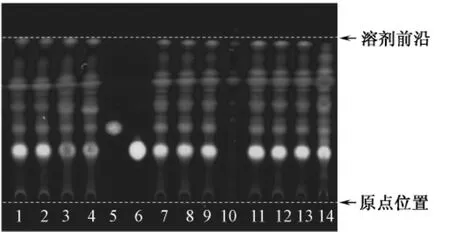
图6 红花清肝十三味丸中胆酸、猪去氧胆酸的TLC图谱Fig.6 TLC chromatogram of cholic acid and hyodeoxycholic acid
3 HPLC法测定栀子中栀子苷、红花中羟基红花黄色素A、丁香中丁香酚[8-9]
3.1 色谱条件 Phenomenex Luna C18色谱柱(5 μm,4.6 mm×250 mm);以甲醇为流动相A,以0.1%磷酸溶液为流动相B,按表1进行梯度洗脱。柱温为30℃,检测波长分别为栀子苷238 nm,羟基红花黄色素A 403 nm,丁香酚280 nm。理论板数按理论板数按栀子苷峰、羟基红花黄色素A峰、丁香酚峰计算均应不低于3 000。

表1 梯度洗脱流动相比例Tab.1 Gradient elution ratio using methanol-H2O
3.2 对照品溶液的制备 取栀子苷对照品、羟基红花黄色素A对照品和丁香酚对照品适量,精密称定,分别加70%甲醇制成每1 mL含栀子苷20 μg,羟基红花黄色素 A 25 μg,丁香酚40 μg的溶液,即得。
3.3 供试品溶液的制备 取本品,研细,取约1 g,精密称定,置具塞锥形瓶中,精密加入70%甲醇50 mL,密塞,称定质量,加热回流60 min,放冷,再称定质量,用70%甲醇补足减失的质量,摇匀,滤过,取续滤液,即得。
3.4 阴性样品溶液的制备 分别按处方比例及制剂制备工艺制备不含栀子、红花、丁香的阴性样品,再按3.3项下方法制备,即得。
3.5 专属性试验 取对照品溶液、供试品溶液和阴性样品溶液各10 μL,分别注入液相色谱仪测定,结果红花、丁香、栀子阴性样品分别在羟基红花黄色素A、丁香酚、栀子苷相应保留时间处未见色谱峰,表明阴性样品对检测无干扰。见图7~9。
3.6 线性关系考察 分别精密吸取栀子苷对照品溶液 (质量浓度为 0.106 5 mg/mL)1、6、12、15、18、21 μL;羟基红花黄色素 A对照品溶液(质量浓度为 0.064 66 mg/mL)1、3、5、6、8、9、12 μL;丁香酚对照品溶液 (质量浓度为0.227 8 mg/mL)1、5、9、15、18、21 μL,注入高效液相色谱仪,以进样量为横坐标,峰面积为纵坐标,其回归方程:栀子苷为y=1 444 967.883 12x-8 515.467 88(r=1.000 0),表明其在0.106 5~2.236 5 μg范围内线性关系良好;羟基红花黄色素A为y=2 913 887.269 01x-25 106.472 60(r=0.999 8),表明其在0.064 66 ~0.775 92 μg范围内线性关系良好;丁香酚为y=973 750.233 23x+5 538.847 34(r=1.000 0),表明其在0.227 8~4.783 8 μg范围内线性关系良好。
3.7 稳定性试验 取同一份供试品溶液 (批号:20120203),按3.1项,分别在制备后0、4、8、16、20、24 h进样测定。结果峰面积RSD栀子苷为0.54%,羟基红花黄色素A为2.2%,丁香酚为0.73%,表明供试品溶液在24 h内基本稳定。
3.8 重复性试验 取本品,研细,取约1 g,精密称定,依法测定。结果栀子苷RSD为0.73%;羟基红花黄色素A RSD为1.95%;丁香酚RSD为1.2%,方法重复性良好。
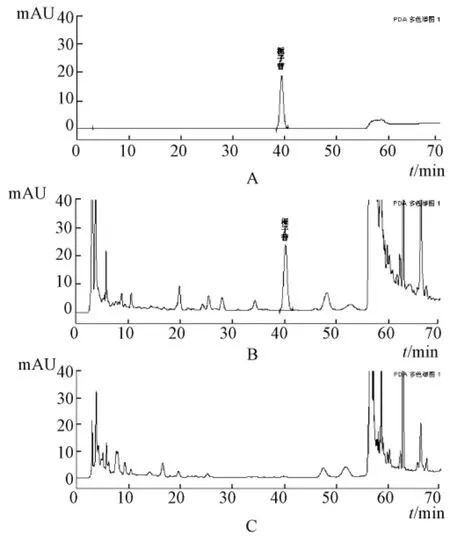
图7 栀子苷测定HPLC图谱Tab.7 HPLC chromatograms of geniposide

图8 羟基红花黄色素A测定HPLC图谱Fig.8 HPLC chromatogramsofhydroxysafflor yellow A

图9 丁香酚测定HPLC图谱Fig.9 HPLC chromatograms of eugenol
3.9 加样回收率试验 精密称取已知含有量的同一批样品 (批号20120203,栀子苷含有量为3.881 8 mg/g,羟基红花黄色素A含有量为3.026 4 mg/g,丁香酚含有量为7.857 0 mg/g)。①低浓度:取约0.25 g精密加入对照品混合溶液 (含栀子苷0.019 915 mg/mL,羟基红花黄色素A 0.01056mg/mL,丁香酚0.02380 mg/mL)50 mL;②中浓度:取约0.5 g精密加入对照品混合溶液 (含栀子苷0.039 83 mg/mL,羟基红花黄色素 A 0.021 12 mg/mL,丁香酚0.047 60 mg/mL)50 mL;③高浓度:取约1 g精密加入对照品混合溶液 (含栀子苷0.079 66 mg/mL,羟基红花黄色素 A 0.042 24 mg/mL,丁香酚0.095 20 mg/mL)50 mL,按供试品溶液同法制备,测定。结果栀子苷平均回收率97.24%,RSD为1.2%;羟基红花黄色素A平均回收率96.75%,RSD为2.0%;丁香酚平均回收率98.56%,RSD为1.8%。见表2~4。
3.10 样品测定 按上述测定方法,测定11批红花清肝十三味丸样品,结果见表5。

表2 栀子苷加样回收试验Tab.2 Results of recovety tests of geniposide

表3 羟基红花黄色素A加样回收试验Tab.3 Results of recovery tests of hydroxysafflor yellow A

表4 丁香酚加样回收试验Tab.4 Results of recovery tests of eugenol
4 讨论
丁香、丁香酚、木香、去氢木香内酯的薄层鉴别中,曾对木香烃内酯薄层色谱进行了研究,但在其色谱相应位置上,有时空白会有干扰,故仅以木香药材及去氢木香内酯作为对照。
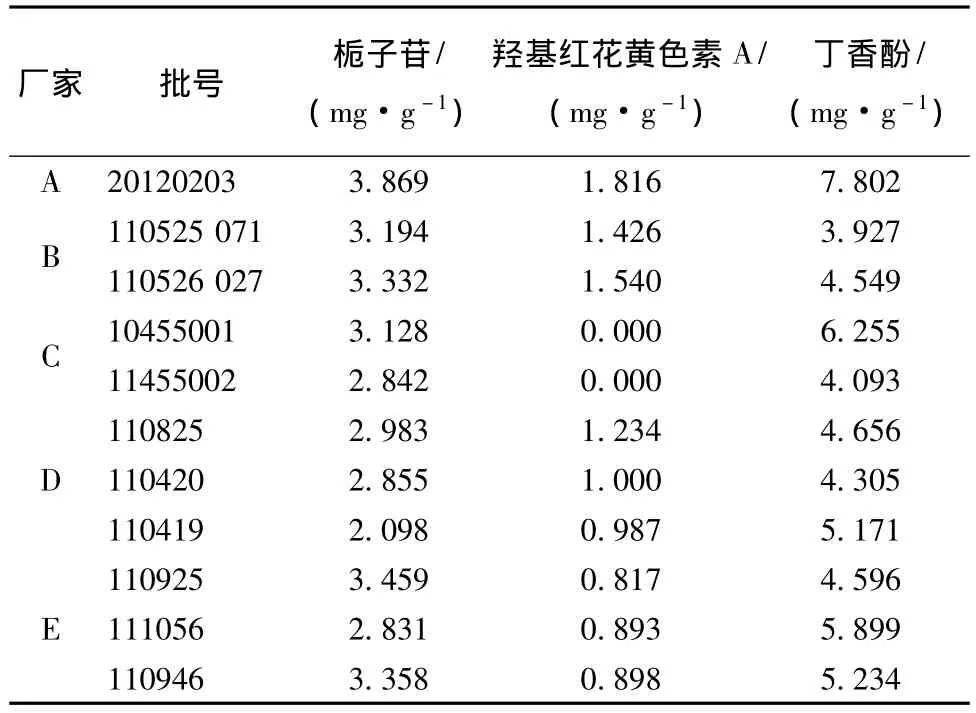
表5 栀子苷、羟基红花黄色素A、丁香酚测定结果(n=3)Tab.5 Determination results of geniposide,hydroxysafflor yellow A,eugenol(n=3)
栀子苷的薄层鉴别中,曾对栀子对照药材薄层色谱进行了研究,通过样品、栀子苷对照品、栀子对照药材及空白各色谱的比较,认为栀子的主要鉴别成分为栀子苷,故仅以栀子苷作为对照。
丁香中丁香酚的定量测定采用《中国药典》2010年版GC的方法,本研究为达到在操作简便的基础上得到更多可靠数据的目的,采用了HPLC方法测定丁香酚的量,其最大吸收波长除参考文献[10-12]外,还采用了PDA检测器扫描验证,确定其最大吸收波长为280 nm。
本实验分别采用不同品牌色谱柱Phenomenex luna C18(5 μm,250 mm ×4.6 mm),TechMate C18(5 μm,250 mm ×4.6 mm),Kromasil 100-5C18(5 μm,250 mm×4.6 mm)进行测定,结果羟基红花黄色素A、丁香酚、栀子苷峰分别在各种色谱柱均分离良好,空白无干扰,不同色谱柱间测定羟基红花黄色素A的RSD为1.2%,丁香酚的RSD为2.3%,栀子苷的RSD为2.3%,表明本HPLC方法有较好的耐用性。
根据表5的数据分析,栀子苷含有量数据各厂家、各批次及RSD值差异均较小;羟基红花黄色素A的含有量测定数据,各厂家之间相差较大,其中厂家C未测出羟基红花黄色素A,经与企业联系,认为与其灭菌方法有关,该成分不稳定,不宜采用加热灭菌的方法;丁香酚含有量测定数据,各厂家、各批次均有一定差异,由于丁香酚为易挥发性成分,有可能与原料、生产、贮藏、运输等环节有关。除栀子苷、羟基红花黄色素A、丁香酚3成分外,还对没食子酸、木香烃内酯、去氢木香内酯进行了研究。但在与没食子酸相应保留时间处诃子阴性对照有干扰,木香中木香烃内酯、去氢木香内酯峰形均欠佳,故未对这3种成分进一步进行定量测定研究。
[1]国家药典委员会.中华人民共和国卫生部药品标准:蒙药分册[S].1998.
[2]周 军,张 晶,金兆祥,等.济坤丸质量标准研究[J].天津药学,2010,22(1):28-30.
[3]李冬梅,刘永利.中国药典品种参苏丸中木香鉴别的商榷[J].时珍国医国药,2010,21(7):1820.
[4]姚令文,郑笑为,刘 燕,等.治痢片的质量标准研究[J].中国药品标准,2009,10(5):342-346.
[5]侯世海.檀香、紫檀香、降香及苏木的紫外光谱和薄层色谱鉴别[J].青海医药杂志,1999,29(10):54-55.
[6]国家药典委员会.中华人民共和国卫生部药品标准:藏药第一册[S].1995.
[7]国家药典委员会.中华人民共和国药典:2010年版一部[S].北京:中国医药科技出版社,2010:7.
[8]王焕芸,冯 欣,董立森.反相高效液相色谱法测定红花清肝十三味丸中羟基红花黄色素A的含量[J].中国新药杂志,2008,17(11):952-954.
[9]刘月庆,王 睿,毕开顺.HPLC法测定红花黄色素A的含量[J].药物分析杂志,2004,24(4):356-358.
[10]Liu Shujuan,Li Zongtao,Wang Hong,et al.Quantification of eugenol and bancroftione inCaryophylli Fructususing high-performance liquid chromatography[J].J Chin Pharm Sci,2010,19(10):459-463.
[11]刘 刚,李勉珊,谢雅君,等.变换波长HPLC测定七味广枣丸中丁香酚、木香烃内酯和去氢木香内酯的含量[J].中国药学杂志,2011,46(1):64-66.
[12]王 静,岳秀峰,王 晋,等.蒙药红花清肝十三味丸中丁香酚含量的测定方法研究[J].内蒙古医学院学报,2012,34(1):65-68.
