河毒素药理活性和热性质密度泛函研究
2013-07-31秦文杰钟爱国
秦文杰,钟爱国
(浙江省台州学院医药化工学院, 浙江 台州 316000)
1970 年Tamura 等报道了TTX-氢溴酸盐的晶体结构[1,2],潘心富等于1979 年首次由河豚卵巢中分离提取出 TTX[3]。在理论计算方面, 陈常英等[4]利用DPCILO 程序,采用半经验方法(INDO)优化了 TTX及其 5 个衍生物的结构及分子轨道, 并与化学结构不同但药理作用相同的石房蛤毒素(STX)进行了比较;赵永明等[5]探讨了TTX 及其23 种类似物的红外光谱和核磁共振图谱。TTX 是迄今为止人类在自然界中发现的最为奇特的小分子天然产物之一,不仅结构新颖而且性质独特,即使长时间高温加热亦不会破坏其化学结构或降低其毒性,但遇碱不稳定,易被破坏。TTX 的分子结构和原子编号如图1 所示。由于原料来源稀有,纯品昂贵,限制了它的实验研究。本文选用密度泛函方法在优化结构的基础上,得到其热力学函数并利用Fukui 指数和前线轨道理论,对其易发生的反应部位进行了理论预测,取得了有意义的结果。
1 计算方法
本文对河豚毒素分子采用 DFT 理论的 B3LYP方法在 6-311+G(d,p)基组水平上进行了优化计算。在优化得到的稳定构型基础上,采用Freq 方法进行了频率分析,结果表明所有简谐振动频率全部为正值,表明其计算结果是可信的。本项目的全部计算工作通过Gaussian03 程序在PC 机上完成。

图 1 河豚毒素(C11H17O8N3)分子结构和原子编号Fig.1 Tetrodotoxin (C11H17O8N3) molecular structure and atomic number
2 结果与讨论
2.1 几何结构分析
用Gaussian 03程序在B3LYP/6-311+G(d,p)水平上进行优化计算得到了河豚毒素分子的键长, 键角等与晶体实验值的比较示于表1[1,2]。

表1 优化后键长、键角的比较(键长:nm; 键角: °)Table 1 The bond lengths, bond angels, optimized (nm, °)
正常的C=N 双键的键长(0.134~0.138 nm), C-N单键(0.147~0.152 nm),C-C 单键(0.154~0.162 nm),C-O 单键(0.120~0.143 nm), C=O 双键(0.121~0.123 nm), O-H(0.094~1.500 nm)。表1 中列出了优化后分子的部分键长数据表明:除C10-O18的键长稍微大一点外,其他键长均属于正常范围。结合分子结构图1 分析,对应的 C5-N12键(0.144 nm)和 C12-N15键(0.146 nm)的键长稍长于正常的C=N 双键(0.134~0.138 nm),而与之相邻的 C10=N12双键的键长(0.126 nm)稍小于正常的 C-N 单键(0.147~0.152 nm),符合胍基离域结构稳定的要求。表2 中列出的重要键角数据表明,由 C1-C2-C6-C13-C8-C3原子组成的六元环的夹角数据均在 109.0° 附近,而 C1-C2-C7-N15-C12-N5,C1-C2-C6-O14-C10-C5,C1-C4-C10-O17- C8-C3和 C6-O14-C10-O17-C8-C13杂环,夹角均在 107~118.0° 附近, 除C 原子受连接的O 和N 杂原子大的电负性作用使角度变型外,其余角度没有发生明显的扭曲变形。表1 的二面角数据表明:5 个六元环几乎处在椅式结构,这就有利于TTX 分子稳定,使得总能量降低。分子中的支链与环有明显的扭转而没有处在同一平面,这样的结构受位阻效应小有利于发挥官能团优势作用。
2.2 NBO 电荷
优化后TTX 分子中各原子的NBO 电荷分布见表2。

表2 TTX 分子的NBO 净电荷布居值Table 2 NBO net charge population value of TTX e
由于N 和O 原子的电负性比C 和H 原子大。因此, 在 TTX 分子中,3 个 N 原子(- 0.626 ~ -0.781e)和8 个O 原子(- 0.557 ~ -0.705 e)均带有净的负电荷。而且主环上N 和O 原子比氨基上的N 和羟基上的O 原子带有较多的负电荷, 这是因为它们较强烈地吸引相连的C 原子或H 原子上的电荷, 使其自身带上较大负电荷。除 C2原子外,其余C 和H 原子均带有正电荷, 且H 原子带有较大正电荷。 因主环上C 和N 原子正负电荷均不相等, 致使五个六元环主体带有少量的负电荷(0.04~0.05 e), 具有一定的亲水性。在由电荷控制的反应中, 原子的负电荷越多,其受亲电试剂进攻的可能性越大; 反之, 原子的正电荷越多, 则受亲核试剂进攻的可能性也越大. 因此推测胍基上的N19, N5,和N15原子很可能是亲电反应的作用点。
红外吸收光谱对研究分子的结构、化学键、表征和鉴别物质等有十分重要的作用。在结构优化的基础上, 在相同的计算水平上计算了TTX 的振动红外光谱。TTX 属于 C1点群, 有 39 个原子, 对应有94 个振动模式。理论计算所得到的部分特征振动频率(0~4 000 cm-1)及其红外强度列于图2。

图2 理论模拟TTX 的IR 谱Fig.2 IR spectrum of TTX2.3 IR 和 1HNMR 谱
在图2 谱图中,出现了TTX 的特征峰值: 3 502 cm-1(O-H,伸缩); 3 385 cm-1(N-H,伸缩); 1 766 cm-1(C=O 伸缩);1 070~1 000 cm-1(伯醇,C-O 伸缩);(1 120~1 030 cm-1仲醇C-O,伸缩); 1 170~1 100 cm-1(叔醇 C-O,伸缩);1 275~1 020 cm-1(脂肪醚O-C-O,反对称伸缩);1 098 cm-1(六元单氧环,伸缩); 1 640 cm-1(N-H,弯曲振动)和1 600 cm-1(一级酰胺的特征吸收峰); 1 550~1 530 cm-1(N-H,弯曲振动吸收)。在低频率范围内(<400 cm-1)还出现较多吸收峰,这主要由于六元环的 H 原子的特征指纹区[6-7]。理论模拟并指认TTX 核磁共振谱(见图3 所示)的峰特点较好地与其实验值吻合起来,也进一步验证了计算的准确性[8]。

图3 1HNMR 图谱指认Fig. 3 1HNMR spectrum of TXX
2.4 热力学稳定性
式(1)~(5) 显示了 TTX 的热力学函数计算结果与温度在25~1000 K 范围的对应关系。在298.15 K,熵(Sm)、热容(Cp,m)、焓(Hm)和自由能(Gm)的计算结果分别为 361.27, 142.19 J·mol-1·K-1和 343.31, 316.92 kJ·mol-1; 随温度升高, 熵(Sm)、热容(Cp,m)、焓(Hm) 等热力学函数均增大, 而自由能(Gm) 减小, 直到温度接近500 K 出现负值。通过对TTX 的计算热力学函数与温度的关系拟合, 我们得到了TTX 热力学函数与温度的关系式如下:
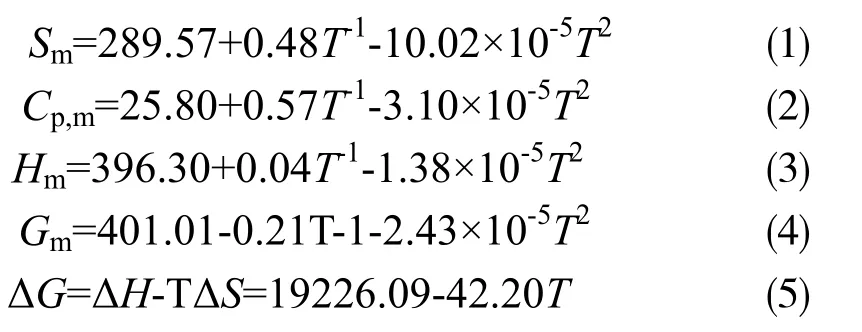
在整个温度范围内(25~1 200 K), T2的系数都很小, 因此其 4 个热力学函数与温度的倒数(1/T)近似呈正的线性关系。现假设TTX 脱水反应的焓变(Δ H)和熵变(ΔS)与温度关系不大为常数,则计算得到分解反应的吉布斯自由能变(ΔG)与温度成线性关系,意味着该脱水反应在高温下(520 K)能自发进行(ΔG<0),为熵变驱动型反应(ΔS>0)。这与热重分析结果基本吻合。
2.5 极性和疏水参数
偶极矩和在正辛醇-水体系的分配系数(P)是用来表示药物亲脂性或疏水性的重要物理参数。我们使用 Gaussian03 程序计算获得 TTX 分子的偶极矩(3.368D),为弱极性。这可能是由于TTX 的6 个醇羟基的存在,增大了TTX 的亲水性的缘故; 脂水分配系数(logP=996.16) 很大,表明其为一亲脂性的分子。另外,使用ACD/Lab 6.0 软件预测的TTX 在pH=7时的水溶解度 S=1.40×10-3mol·L-1,在pH=13 时突然增大。
2.6 反应活性
TTX 的亲电与亲核反应的Fukui 指数值列于图4。从图4 中数据可以看出, 最可能的亲电反应中心(f-)主要集中在3 个N 原子以及与之相连的H35,H32,H26以及 H28原子上, 主环整体不显电性, 尤其胍基N 原子上还含有孤对电子, 可与强酸如盐酸、硫酸、硝酸等都能形成盐; 亲核反应中心(f+)也主要在 N原子以及相连的H 原子上。因此, 遇到强酸或强碱溶液则分子会水解, 逐步被羟基取代, 最后生成开环结构。分子能隙ΔE(ELUMO-EHOMO) 的大小, 反映电子从最高占据轨道向最低空轨道发生电子跃迁的能力, 一定程度上可以代表其参加化学反应的活性。其差值越大, 分子稳定性越强; 反之分子越不稳定,越易参与化学反应。 TTX 的计算结果为EHOMO=-571.233 kJ·mol-1, ELUMO=13.797 kJ·mol-1, Δ E=585.03 kJ·mol-1。比较计算结果可知, 得到电子的能力较弱(ELUMO>0) , 因而生成河豚酸等衍生物的过程中, 胺基被羟基逐步取代; 失去电子的能力相对较弱(因为 EHOMO 很低), 因其胍基(C=NH)上的孤电子对, 能吸引 H+形成稳定的 C=NH2+, 所以它是一种弱碱(pKb=8.3)。能隙较大, 所以参加化学反应活性很弱。

图4 TTX 的Fukui 指数图Fig. 4 The atomic Fukui index of TXX
3 结 论
(1) 几何优化表明, 河豚素的 6 个六元环互成椅式构象,具有稳定的分子构型和良好的疏水参数,在碱性溶液中溶解能力强,红外光谱表征与官能团吻合较准确,核磁共振与其实验值基本符合;
(2) 在25~1 200 K 范围内,相应的热力学函数与温度的倒数呈正的线性关系,温度增加致520 K,脱水分解反应趋势增加,是受熵变驱动型反应;
(3) 通过 NBO 电荷分布, Fukui 指数和前线轨道分析, 我们推测分子活性最强的部位在胍基,胍基 N 原子孤对电子吸引酸的 H+显弱碱性的亲电反应; 与 N 相连接的 H 原子被碱性 OH-逐步取代生成开环衍生物的亲核反应。TTX 将主要通过这2 种方式来发挥其毒理和药理作用。
[1]Tamura C.,Amakasu O.,Sasada Y.,Tsuda K.. The crystal structure of derivatives of tetrodotoxin. I. Tetrodonic acid hydrobomide[J]. Acta Cryst. 1966, 21:219-225.
[2]Tamura C.,Amakasu O.; Sasada Y.,Tsuda K. The crystal structures of derivatives of tetrodotoxin. II. Diaeetylanhydrotetrodotoxin Hydroiodide[J]. Acta Cryst, 1966, 21:226-236 .
[3]潘心富, 黄致强. 河豚毒素研究[J]. 中国海洋药物,1980, 17: 77-91.
[4]陈常英,丁晓琴,潘心富,李玉林. 河豚毒素(TTX)及其衍生物的电子结构和构效关系及与石房蛤毒素(STX)的比较研究[J]. 化学学报, 1998, 56:109-116.
[5]赵永明,苏晓会,史清文,顾玉诚. 河豚毒素及其类似物的研究概况[J]. 河北医科大学学报,2007, 28(6):474-480.
[6]Goto T.,Kishi Y.,Takahashi S.,et a1.Tetrodotoxin XI[J]. Tetrahedron,1965, 21(8):2059-2088.
[7]Brian A. M.,Marco A. C. Approach to Tetrodotoxin via the Oxidative Amidation of a Phenol[J]. Org. Lett., 2009, 11(20): 4736-4739.
[8]Douglass F. T.,Pierre H. S. Synthesis of (-)-Tetrodotoxin: Preparation of an Advanced Cyclohexenone Intermediate[J]. J. Org. Chem., 2003,68:7768-7771.
