邻羟基苯甲醛希夫碱类化合物的合成与表征
2013-07-24周影
周影
(辽宁师范大学化学化工学院,辽宁大连160029)
邻羟基苯甲醛希夫碱类化合物的合成与表征
周影
(辽宁师范大学化学化工学院,辽宁大连160029)
近几年来,随着化工业的发展,希夫碱类化合物及其配合物诸多领域已经有了非常广泛的应用,其应用前景十分广阔.本文以邻羟基苯甲醛为原料,分别与3-氨基苯甲酸和4-氨基苯甲酸通过脱水缩合反应,合成了具有希夫碱结构的羧酸类衍生物1和2,并通过IR和1HNMR等谱图表征了该类化合物的结构,并据此研究了反应机理.
邻羟基苯甲醛;希夫碱;羧酸衍生物
1864年,H.Schiff首先将胺和活性羰基进行缩合,合成具有碳氮双键的一类新物质,并将其命名为Schiffbase(希夫碱).由于该类物质具有碳氮双键,很容易与金属离子配位形成稳定的配合物,因此,在配位化学领域中得到高度重视.随着近代化学研究的开展,有关希夫碱及其配合物的应用和研究报道逐渐丰富起来.1969年,研究者发现过渡金属Co(Ⅱ)的Schiff碱配合物在生物活性方面应用前景很广阔,因而使该研究领域活跃起来.
希夫碱的合成是一种缩合反应,反应物空间立体结构及电子效应很大程度地影响反应的发生.不同结构的取代基,其产生的诱导效应对进攻效果将起着不同的影响,反应过程中其电子效应与空间位阻效应也都起着重要作用,故应慎重地选择取代基.在实际设计反应合成路线和反应条件时,要根据具体体系要求进行选择,因此,了解缩合反应机理及其影响因素对反应的进行会十分有利,具体反应历程如下图所示.
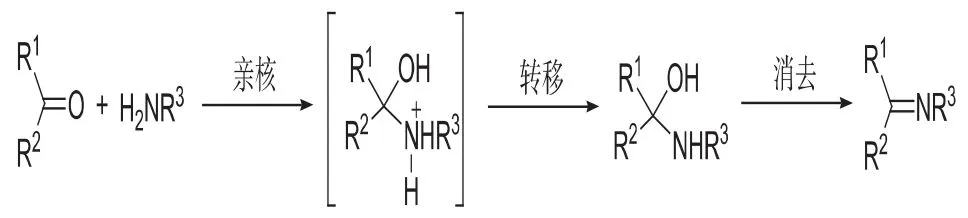
图1 希夫碱类化合物的合成机理
羧酸类希夫碱配合物具有良好的生物活性,近年来得到科学工作者们的普遍重视.羧酸类希夫碱配合物具有多方面的应用,例如,在化学分析领域、催化剂使用方面[6]、农业领域、医学领域[7-8],光致变色领域[9-11],羧酸类席夫碱配合物都发挥着巨大的作用.本文在参阅了大量文献的基础上,选取了邻羟基苯甲醛为原料,与3-氨基苯甲酸和4-氨基苯甲酸通过脱水缩合反应,构筑碳氮双键,形成了一系列具有潜在生物活性的羧酸类希夫碱,力求使该类物质在化学、生物、医药等领域发挥一定的作用.
1 实验部分
1.1 实验仪器
BrukerAvance500型核磁共振仪,RE-52C型旋转蒸发器,CL-4型恒温加热磁力搅拌器,Sartorius电子天平(BL310),SHZ-2000型双配套循环水式多用真空泵,ZF-2型三用紫外分析仪,KQ-500DV型超声波清洗器,KQ-B型气流干燥器.
1.2 实验试剂
邻羟基苯甲醛,3-氨基苯甲酸,4-氨基苯甲酸,无水Na2SO4,高纯氮气,氯化钠,无水甲醇.
1.3 合成路线
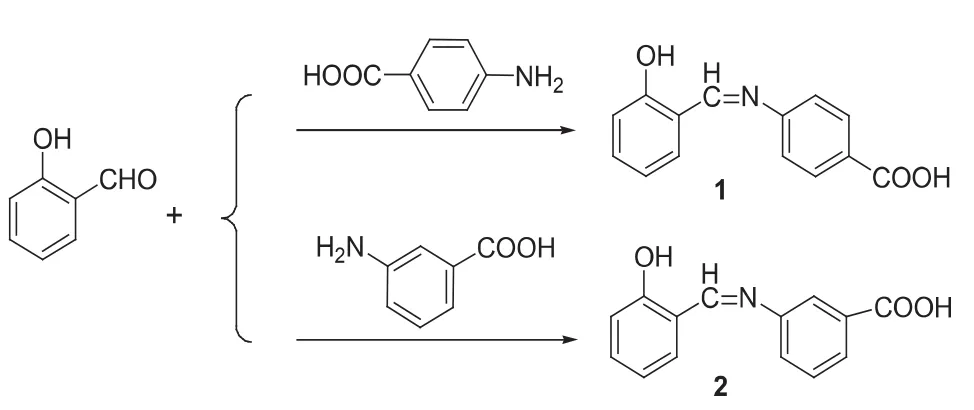
图2 目标产物1和2的合成
1.3.1 对氨基苯甲酸水杨醛希夫碱1的合成
用冰盐浴将体系的温度降至0℃以下,在100 ml的三颈烧瓶中加入0.244g(0.002mol)邻羟基苯甲醛,再加入20mL无水甲醇,使二者均匀混合,待全部溶解后,为无色透明的溶液,将0.274g(0.002mol)的4-氨基苯甲酸溶解于30mL无水甲醇中,通过恒压滴液漏斗滴加到反应体系中,剧烈搅拌,待固体全部溶解后将温度升高至65℃,反应约4h,有大量固体析出,TLC检测反应进程,待反应结束后,减压抽滤,用热的无水甲醇进行充分洗涤,得产品为0.43g,淡黄色固体,产率为90%.IR(KBr)ν/cm-1:3437(ν-OH),3030(ν=C-H),1672(νC=N),1630 (νC=O),1557,1466(νC=C),1380(νC-N), 1160(νC-O);1HNMR(CDCl3,500MHz,ppm), δ:11.04(s,1H,-COOH),δ:10.21(s,1H,-OH), δ:9.17(d,1H,CH=N),δ:7.5~8.1(m,8H,PyH);HRMS(positive-SIMS):m/z:242.0113(M+1)(计算值C14H11NO3:241.0739).
1.3.2 间氨基苯甲酸水杨醛希夫碱2的合成
用冰盐浴将体系的温度降至0℃以下,在100 ml的三颈烧瓶中加入0.244g(0.002mol)邻羟基苯甲醛,再加入20mL无水甲醇,使二者均匀混合,待全部溶解后,为无色透明的溶液,将0.274g(0.002mol)的3-氨基苯甲酸溶解于30mL无水甲醇中,通过恒压滴液漏斗滴加到反应体系中,剧烈搅拌,待固体全部溶解后将温度升高至65℃,反应约4h,有大量固体析出,TLC检测反应进程,待反应结束后,减压抽滤,用热的无水甲醇进行充分洗涤,得产品为0.40g,黄色固体,产率为84%.IR(KBr)ν/cm-1:3330 (ν-OH),3100(ν=C-H),1660(νC=N),1630 (νC=O),1565,1432(νC=C),1350(νC-N), 1142(νC-O);1HNMR(CDCl3,500MHz,ppm), δ:11.22(s,1H,-COOH),δ:9.81(s,1H,-OH), δ:8.90(d,1H,CH=N),δ:7.5~8.1(m,8H,PyH);HRMS(positive-SIMS):m/z:242.0124(M+1)(计算值C14H11NO3:241.0739).
2 结果与讨论
本文以对邻羟基苯甲醛为起始原料,分别与3-氨基苯甲酸和4-氨基苯甲酸反应,构筑了含碳氮双键的羧酸类希夫碱化合物,并通过IR和1H NMR等表征手段确定了化合物1和2的结构,由于希夫碱及其配合物在药物、催化、分析、材料等领域有广泛的应用,本文的合成对研究希夫碱的各种性质奠定了研究基础.
〔1〕Jabri,E,GarrMB,HausingerRP,KarplusP A.Crystalstructureofureasse.Science, 1995,268,998.
〔2〕VolkmerD,HommeriehB,GriesarK.,Haase W,HrebsB.Inorg.Chem.,1996,35(13),3792.
〔3〕ArnoldM,BrownDA,DeegO,Errington W,HaaseW.Inorg.Chem.,1998,37(12),2920.
〔4〕CasellaL,GullottiM.Inorg.Chem., 1986,25,1293.
〔5〕LiZC,LiTS.Chem.J.Chin.Univ.,1993, 14,301.
〔6〕BastosMBR,MoreiraJC,FariasPAM. Analytical.Chimica.Acta.,2000,408,83.
〔7〕叶勇.2-氯代苯甲醛丙氨酸席夫碱及其3d-过渡金属配合物的合成与表征[J].湖北大学学报, 2001,23(1):57-61.
〔8〕DesaiSB,DesaiPB,DesaiK.R.Synthesis ofsomeSchiffbasesthiazolinonerandazetidinonerfrom2,6-di-amnobonzol[1,2-d;4,5-d`] bisthiazoleandtheiranticanceractivities. HetercyclCommun.,2001,7(1):83-90.
〔9〕BASTOSMBR,MOREIRAJC,FARIAS PAM.AdsorptivestrippingvoltammetricbehaviourofUO2(II)complexedwuthehwSchiff baseN,N-prime-ethylenebissalicylidenimine) inaqueous4-(2-hydroxyethyl)-1-iperazine ethanesulfonicacidmedium.AbalyticalChimica Acta.,2000,408:83-88.
〔10〕杜宝石,樊耀亭.镨、钕、钇甘氨酸三元配合物的晶体结构[J].结构化学,1996,15(2):141-146.
O629
A
1673-260X(2013)11-0016-02
