发疹性丘疹型汗孔角化症一例
2013-07-19林尽染陈明华徐金华
林尽染,韩 凌,陈明华,罗 燕,徐金华
临床资料
患者,女,60 岁。主因双下肢皮损2 周,无明显自觉症状,于2010 年8 月就诊。2 周前患者双大腿下段、小腿外侧出现散在分布针尖至粟米大红色丘疹,略隆起于皮肤,表面少许脱屑。发疹前1 个月曾患急性荨麻疹,接受甲泼尼龙40 mg/d 治疗后缓解,2 周前减量至甲泼尼龙8 mg/d 后停用。否认有类似疾病家族史。皮肤科情况:双侧大腿、小腿内侧(图1)为主泛发点滴状红褐色角化性丘疹,表面覆有环状细小鳞屑,面部及掌跖部未见类似皮损。皮损组织病理检查示:表皮角化过度,可见角化不全柱,其下方颗粒层消失,未见角化不良细胞(图2)。诊断:发疹性丘疹型汗孔角化症。治疗:外用0.1%维A 酸软膏治疗0.5 年。1 年后随访,皮损颜色变暗,部分变平,无新发皮损。
讨论
临床所见汗孔角化症主要分型有Mibelli 经典斑块型、浅表播散型、播散性浅表性光线型、单侧线状型、掌跖点状型、掌跖泛发型及疣状斑块型等。发疹性丘疹型为一种少见的亚型,日本Kanzaki 等[1]于1992 年首先报道了3 例发疹性瘙痒性丘疹型汗孔角化症,在发病前已有数年无症状的浅表播散型皮损,认为其为浅表播散型的一种异型。其临床特征为突然起病伴明显瘙痒的丘疹性皮损,消退后遗留褐色斑疹或环状皮损。Kanekura 和Yoshii[2]认为丘疹型汗孔角化症可能是经典型汗孔角化症早期炎症阶段的表现;瘙痒症状可能与表皮棘层肥厚、真皮浅层细血管周围淋巴细胞浸润有关;免疫组化结果显示浸润的炎性细胞主要为CD4+T 细胞夹杂CD8+T 细胞及少量朗格汉斯细胞,而不伴瘙痒的皮损免疫组化结果显示无CD8+T 细胞浸润,推测CD8+T 细胞介导的免疫反应可能与皮损自行消退有关。国内于2003 年由孙建方等[3]报道1 例伴瘙痒的丘疹型汗孔角化症,患者病程长,起病于双前臂,渐累及四肢、颈部、阴囊及胸部,未自行消退,遗留褐色环状皮损。本文报道的病例既往无明确的汗孔角化症病史,皮损表现为多发的角化性丘疹,组织病理表现可见角化不全柱,符合汗孔角化症的典型组织病理特点,结合皮损与组织病理可诊断为发疹性丘疹型汗孔角化症。该例患者与日本学者报道的典型病例不同,其不伴瘙痒,组织病理显示棘层肥厚及真皮浅层细血管周围炎性细胞浸润不明显,可能与该例患者近1 个月因急性荨麻疹接受糖皮质激素治疗有关。临床上该病可与点滴状银屑病、毛周角化症、毛囊和毛囊旁角化过度病等相鉴别。文献报道冷冻、CO2激光、外用氟尿嘧啶、外用维A 酸联合氟尿嘧啶、外用咪喹莫特及手术切除等治疗汗孔角化症有效。本例患者外用维A 酸治疗有效,仍需随访观察皮损是否复发。
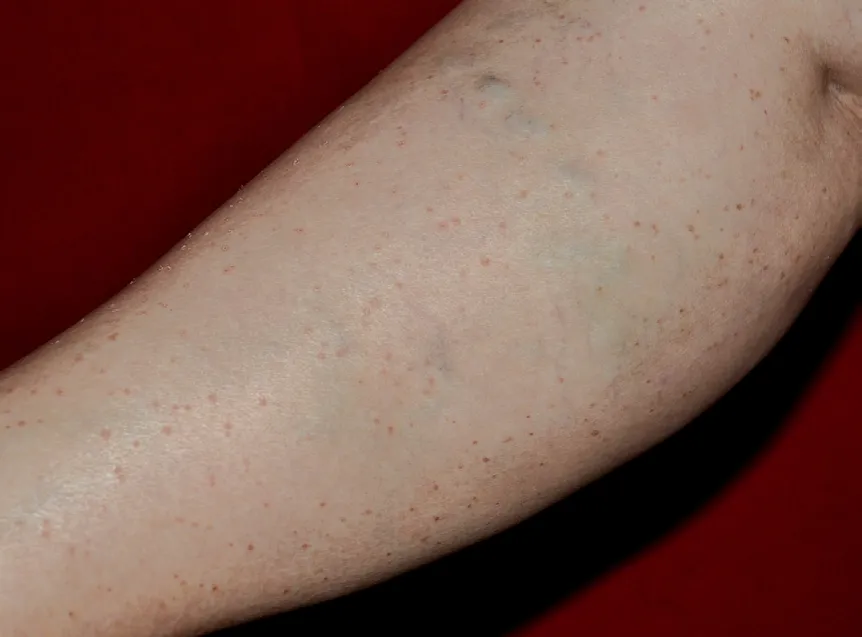
图1 发疹性丘疹型汗孔角化症患者临床皮损

图2 发疹性丘疹型汗孔角化症患者皮损组织病理
[1] Kanzaki T, Miwa N, Kobayashi T, et al. Eruptive pruritic papular porokeratosis [J]. J Dermatol, 1992, 19(2):109-112.
[2] Kanekura T, Yoshii N. Eruptive pruritic papular porokeratosis: a pruritic variant of porokeratosis [J]. J Dermatol, 2006, 33(11):813-816.
[3] 孙建方, 李保强, 胡兹嘉. 丘疹型汗孔角化症1例 [J]. 中华皮肤科杂志, 2003, 36(12):713.
