皮肌炎/多发性肌炎合并肺间质病变的临床特征及预后相关因素
2013-04-17周丽忻霞菲黄华覃文王庭辉赵宝景
周丽 忻霞菲 黄华 覃文 王庭辉 赵宝景
●临床研究
皮肌炎/多发性肌炎合并肺间质病变的临床特征及预后相关因素
周丽 忻霞菲 黄华 覃文 王庭辉 赵宝景
目的 探讨皮肌炎/多发性肌炎(DM/PM)合并肺间质病变(ILD)的临床特征和预后。 方法 回顾住院诊治及门诊长期随访的141例DM/PM患者的临床资料及实验室指标,对PM/DM合并ILD的生存时间、预测因素和预后不良因素进行分析。结果 141例DM/PM患者中合并ILD 42例(29.8%),其1、5、10年生存率分别为76%、66%和57%,中位生存时间为127.3个月。多因素Cox回归分析得出:合并ILD、年龄>50岁、声音嘶哑、低白蛋白血症、低氧血症是DM/PM预后不良的独立危险因素(均P<0.05)。logistic回归显示,低白蛋白血症、技工手和抗Jo-1抗体与ILD呈正相关(均P<0.05),成为ILD相关预测因子。急性/亚急性ILD进展快,病死率高(75%)。丙种球蛋白治疗与病死率呈负相关(P<0.05)。 结论 ILD是DM/PM的常见并发症,也是影响预后的危险因素。技工手、抗Jo-1抗体和低白蛋白血症是DM/PM合并ILD的预测因子,低氧血症是影响ILD预后的不良因素,早期使用丙种球蛋白冲击治疗有助改善预后。
皮肌炎 多发性肌炎 间质性肺病 预后
炎性肌病(inflammatory myopathies,IM)是一种免疫介导的以侵犯骨骼肌为主的系统性自身免疫性疾病,临床上主要为皮肌炎(dermatomyositis,DM)和多发性肌炎(polymyositis,PM)。DM/PM常可累及全身多个脏器,其中肺间质病变(interstitial lung disease,ILD)是DM/PM的主要死亡原因之一,5年病死率0~55%[1-2]。笔者通过对141例DM/PM患者进行回顾,分析DM/PM合并ILD的临床特征,预测DM/PM发生ILD的相关因子,探讨影响ILD患者预后的相关因素,提高对DM/PM合并ILD的认识。
1 资料和方法
1.1 一般资料 收集宁波市第一医院1997-01—2012-08住院诊治及门诊长期随访的患者资料共171例,其诊断均符合1975年Bohan和Peter的DM/PM分类标准[3]。去除合并恶性肿瘤25例(包括鼻咽癌、胃癌、肺癌、淋巴瘤等)、儿童DM/PM 3例、重叠综合征2例(均为重叠系统性红斑狼疮),共收集成人特发性DM/PM 141例,其中典型DM 100例,PM 23例,无肌病性皮肌炎(amyopathic dermatomyositis,ADM)18例。ADM是DM的一种新类型,它具有特征性的DM皮肤改变而无肌炎表现,血清肌酶不升高,肌电图及肌肉病理无显著改变。141例患者中合并ILD 42例(29.8%),男13例,女29例,男∶女为1∶2.2,年龄28~86岁,平均(56.4±13.0)岁。其中DM合并ILD者30例,PM合并ILD者7例,ADM合并ILD者5例。发病到终点随访时间2~228个月,平均(55.2±45.4)个月。采集患者临床表现[发热(T>37.3℃,除感染外)、Gottron征,眶周红斑、技工手、吞咽困难、声音嘶哑、体重减轻、近端肌痛、肌无力、关节炎]、实验室检查[红细胞沉降率(ESR)、肌酸激酶(CK)、天冬氨酸转氨酶(AST)、乳酸脱氢酶(LDH)、抗核抗体(ANA)、抗Jo-1抗体、血气分析]、特殊检查 [肺高分辨率CT(HRCT)、肺功能]、用药情况和预后。对所有患者进行门诊及电话随访(在院死亡者除外),记录转归。
1.2 纳入与排除标准 DM/PM合并ILD的标准:(1)排除其他病因引起的弥漫性间质性肺炎,如感染、心力衰竭、药物反应等;(2)有干咳、进行性呼吸困难,活动后胸闷气促,双肺底部闻及爆裂音;(3)胸部X线或CT(包括HRCT)检查表现为双肺网格状改变、斑片状渗出、毛玻璃样病变、肺实变、蜂窝肺;(4)肺功能检查表现为限制性通气功能障碍或者弥散功能障碍(低于预计值80%);(5)外科肺活检符合间质性肺病。符合第(1)条及另4条中的2条或第(5)条即诊断为DM/PM合并ILD。排除标准:(1)合并其他弥漫性结缔组织病的重叠综合征,继发性干燥综合征除外;(2)合并恶性肿瘤者;(3)儿童DM/PM(发病年龄≤16岁)。
1.3 ILD分型 根据病情急缓分为4个亚型:(1)急性间质性肺炎(acute interstitial pneumonia,AIP):ILD严重,1个月内快速进展为呼吸衰竭。(2)亚急性间质性肺炎(subacute interstitial pneumonia,SIP):ILD进展较 AIP慢,但呼吸困难在3个月内有明显进展。(3)慢性间质性肺炎(chronic interstitial pneumonia,CIP):干咳、劳力性呼吸困难、偶尔出现呼吸衰竭症状超过6个月。(4)无症状型:胸部影像学和肺功能检查提示肺间质病变轻微,没有明显的临床表现及爆裂音等体征。
1.4 统计学处理 采用SPSS17.0统计软件。计量资料以表示,采用寿命表法、多因素Cox回归模型分析预后和危险因素,ILD相关的预测因子采用非条件logistic回归分析,治疗药物和预后的相关性采用Spearman相关分析,组间比较采用Mann-Whitney U检验,计数资料组间比较采用χ2检验。
2 结果
2.1 生存分析 对42例DM/PM合并ILD患者进行生存分析,得出1、5、10年生存率分别为76%、66%和57%,中位生存时间为127.3个月。多因素Cox回归分析得出合并ILD(OR=2.536,95%CI 1.205-5.335,P=0.014)、年龄>50岁(OR=1.074,95%CI 1.040-1.109,P=0.000)、声音嘶哑(OR=5.254,95%CI 1.710-16.142,P=0.004)、低白蛋白血症(OR=7.619,95%CI 2.378-24.410,P=0.004)是DM/PM预后不良的独立危险因素。
2.2 合并与未合并ILD两组患者临床表现的比较 根据患者是否合并ILD分为合并ILD组42例,未合并ILD组99例。
2.2.1 临床表现 141例DM/PM患者中发热53例,眶周红斑102例,Gottron征115例,技工手15例,近端肌痛92例,肌无力111例,关节痛52例,吞咽困难16例,声音嘶哑9例,体重减轻31例。合并ILD组患者中发热、技工手、关节炎的发生率明显高于未合并ILD组,差异有统计学意义,而性别、年龄、眶周红斑、Gottron征、近端肌痛、肌无力、吞咽困难、声音嘶哑、体重减轻两组间的差异均无统计学意义,详见表1。
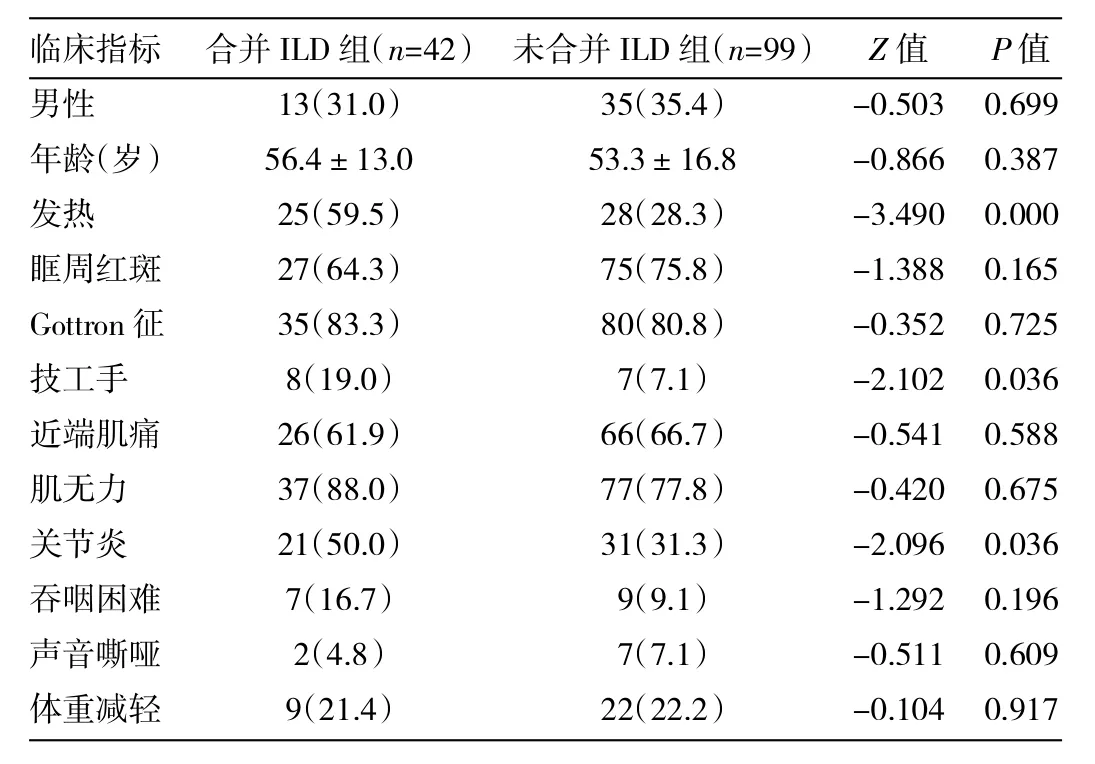
表1 合并与未合并ILD组患者临床表现比较[例(%)]
2.2.2 实验室检查 141例DM/PM患者中ANA阳性38例,抗Jo-1抗体阳性12例。30例患者行血气分析检查,发现低氧血症(PaO2<80mmHg)13例,其中Ⅰ型呼吸衰竭9例,Ⅱ型呼吸衰竭1例。所有患者的HRCT检查结果:条索24例,斑片20例,网格状阴影20例,毛玻璃样变18例,絮状13例,蜂窝状4例,多为混合性改变。29例患者行肺功能检查,其中17例(58.9%)结果异常,主要表现为限制性通气功能障碍和(或)弥散功能障碍、肺活量(VC)和残气量(RV)减少、第1秒用力呼气容积占用力肺活量百分比(FEV1/VVC)正常或增加,一口气弥散量(TLCO/SB)和弥散率(TL-CO/VA)<正常值80%。由于部分重症患者无法耐受肺功能检测,故未对其进一步分析。合并ILD组中的抗Jo-1抗体阳性的发生率明显高于未合并ILD组,而白蛋白、CK水平显著低于未合并ILD组,差异均有统计学意义;但ESR、ALT、AST、球蛋白、LDH、ANA两组间的差异均无统计学意义,详见表2。
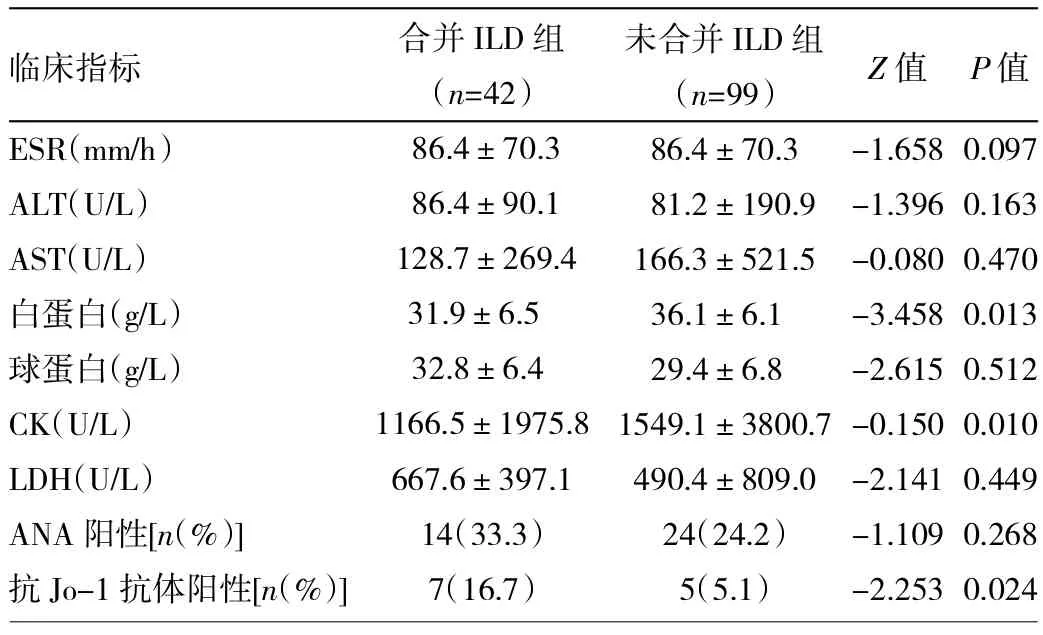
表2 合并与未合并ILD组患者实验室检查结果比较
2.2.3 预测因子 对合并ILD组与未合并ILD组间有明显差异的指标(发热、技工手、关节炎、白蛋白、CK、抗Jo-1抗体)进行非条件logistic回归分析,结果显示技工手(OR=3.888,95%CI 1.084-13.942,P=0.037)、低白蛋白血症(OR=2.958,95%CI 1.233-7.092,P=0.015)和抗Jo-1抗体(OR=4.439,95%CI 1.078-18.272,P=0.039)与ILD呈正相关,是ILD相关预测因子。
2.3 影响ILD的预后因素分析
2.3.1 死亡与非死亡患者临床指标的比较 根据患者是否死亡将DM/PM合并ILD患者分为死亡组15例与非死亡组27例,死亡组患者中低氧血症、抗Jo-1抗体、ANA阳性、低白蛋白血症的发生率显著高于非死亡组,CK水平明显低于非死亡组,差异均有统计学意义,而性别、发热、Gottron征、近端肌痛、肌无力、关节炎、AST、LDH等差异均无统计学意义,详见表3。多因素Cox回归分析显示出现低氧血症是预后不良的独立危险因素(OR=16.572,95%CI 3.238-84.817,P=0.001),13例出现低氧血症的患者中10例死于呼吸衰竭(76.9%),详见表4。
2.3.2 肌病类型与预后 合并ILD患者中DM 30例,死亡14例;PM 7例,无死亡患者;ADM 5例,死亡1例,其中DM合并ILD组预后与PM合并ILD组的差异有统计学意义(P<0.05),ADM合并ILD与DM或PM合并ILD组间的差异均无统计学意义(均P>0.05)。
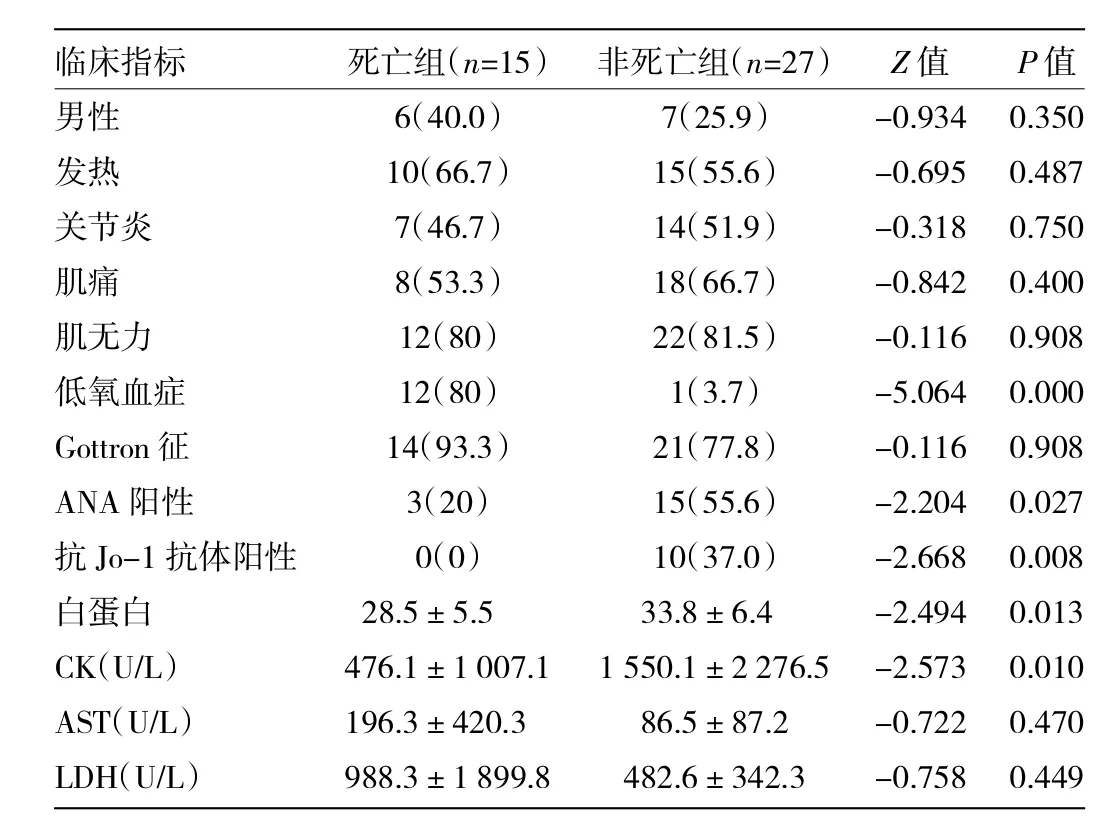
表3 ILD死亡与非死亡组患者临床指标比较[例(%)]
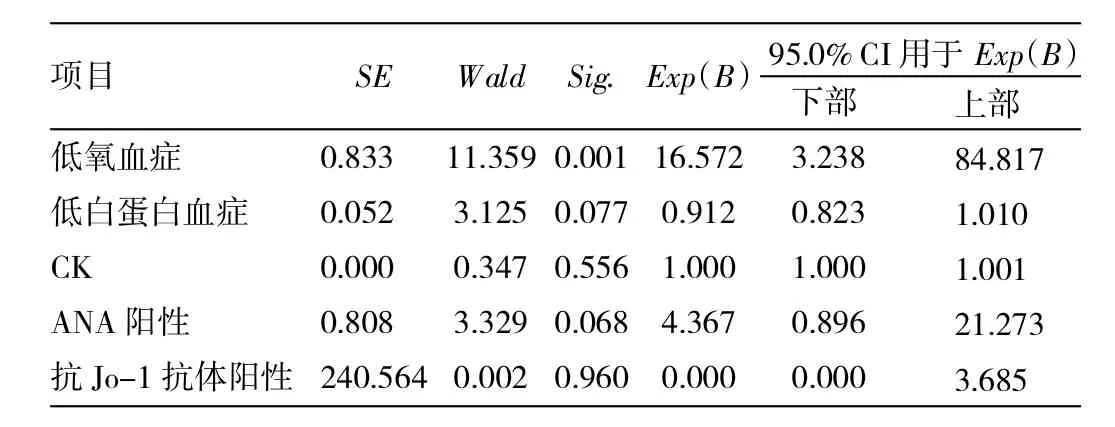
表4 多因素Cox回归模型分析预后不良的独立危险因素
2.3.3 ILD亚型与预后 42例ILD患者中,A/SIP 8例,死亡6例;CIP 20例,死亡8例;无症状型ILD 14例,死亡1例,详见表5。A/SIP中DM 6例,ADM 2例,肺部症状的出现与肺外症状的首发时间一致,均表现为进行性呼吸困难、低氧血症。HRCT检查结果提示,该类患者早期为毛玻璃状、斑片状阴影,伴不同程度的纤维化,后期纤维化程度迅速进展、恶化,呈现弥漫性改变。PM多为CIP和无症状ILD,无A/SIP发生。

表5 ILD亚型与肌病类型(例)
2.3.4 治疗药物与预后 42例DM/PM合并ILD患者中死亡15例(35.7%),其余患者经治疗后临床表现、实验室检查和(或)肺功能均有不同程度改善。死因为合并肺部感染出现呼吸衰竭13例(86.7%),心力衰竭1例(6.7%),中毒性休克1例(6.7%)。给予大剂量甲基强的松龙针(240~500mg/d×3d)冲击5例,包括A/SIP 4例,CIP 1例,其他为泼尼松1~2mg/kg治疗。冲击治疗后死亡4例(80%),3例因肺间质病变进展合并肺部混合感染难以控制死亡,1例因心力衰竭死亡。治疗初期即联合使用静脉注射丙种球蛋白(IVIG)11例,包括A/SIP 5例,CIP 4例,无症状ILD 2例,仅1例AIP死亡(9%)。免疫抑制剂主要为环磷酰胺(共11例,死亡3例)和环孢霉素A(共9例,死亡1例)。有1例SIP患者经阿达木单抗(40mg,2次/周)治疗后肺部病变明显吸收好转。治疗半年后18例复查肺部HRCT,13例病变有好转,5例无明显变化。Spearman相关分析显示大剂量激素冲击与病死率成正相关(r=0.340,P=0.028),IVIG治疗与病死率成负相关(r=-0.331,P=0.032),而环磷酰胺、环孢霉素A与预后无明显相关(r=-0.067、-0.268,均P>0.05)。
3 讨论
DM/PM合并ILD的发生率约26%~64%[4-5],本组PM/DM合并ILD发生率为29.8%,与文献报道一致。ILD是DM/PM重要的系统损害,可以引起呼吸衰竭、继发性肺动脉高压、肺源性心脏病等[6],合并ILD是DM/ PM患者预后不良的独立危险因素,其死亡风险增加2.536倍,故对该合并症要予以重视,笔者建议对DM/ PM的患者及早行肺部影像学检查明确肺部病变情况,有利于早期治疗,改善预后。
本研究提示有技工手、抗Jo-1抗体和低蛋白血症的DM/PM患者合并ILD的风险分别增加3.888、4.439和1.233倍。通常认为抗Jo-1抗体与DM/PM的ILD关系密切,其阳性患者ILD的发生率高达50%~75%[5]。抗Jo-1抗体滴度与ILD的发生和病情严重程度有关[7],动态观察其血清滴度有助于判断ILD的预后。血清白蛋白水平反映(负性)炎症反应的程度和患者一般情况(尤其是营养状况)的好坏[8],低白蛋白血症不仅是DM/PM预后不良的独立危险因素,也是DM/PM合并ILD的预测因子,故对于出现低白蛋白血症患者应予以足够的重视。国内有报道称[9],Gottron征阳性的DM患者伴发ILD的可能性小,且病情轻,但本组资料中未显示Gottron征与ILD的相关性,期间原因仍需进一步探讨。
DM/PM合并ILD患者的肺功能主要表现为限制性通气功能障碍和弥散功能减低,晚期以Ⅰ型呼吸衰竭为主。低氧血症是影响DM/PM合并ILD预后的独立危险因素,存在低氧血症的患者死亡风险增加14.925倍。对于有症状的合并ILD患者建议早期行血气分析,若出现低氧血症则需提高警惕。Takada等[10]曾根据合并ILD的 DM/PM患者对糖皮质激素治疗的反应分为治疗敏感组和抵抗组,发现抵抗组CK降低,AST升高,CK/AST可作为衡量预后的指标,其值低的患者预后不良。本组资料中CK水平在合并ILD组和未合并ILD组间及合并ILD的死亡组和非死亡组间均有统计学差异,但非条件logistic回归分析显示CK水平不能成为ILD的预测因子,也未发现CK/AST与预后的相关性。而Marie等[1]却发现CK水平在合并ILD组和未合并ILD组间的差异无统计学意义,分析可能与样本量及入组人群有关。由于病例数有限,未能进一步按各肌病类型行分层分析,故CK水平与ILD发病和预后的相关性尚待进一步研究。
本研究发现,与PM合并ILD相比,DM合并ILD患者病情重,疗效差,病死率高,与Yamasaki[4]报道一致,可能与DM患者中存在抗CADM-140抗体这一预后不良标记物有关[11]。ILD分型中A/SIP起病急,肺部症状发生早,进展快,低氧血症发生率高,激素治疗效果差,肺部病理主要表现为弥漫性肺泡损害,可于短期内出现肺间质纤维化,病死率高(75%);CIP和无症状ILD相对进展缓慢,以寻常型间质性肺炎(UIP)和非特异性间质性肺炎(NSIP)的病理表现为主,有报道其3年生存率和不合并ILD的DM/PM患者相似[12]。此外,肺部感染也是导致死亡的重要因素,特别是随着病程的延长,长期使用糖皮质激素和免疫抑制剂,极易合并多种病原菌混合感染。多数患者后期处于感染和病情进展的恶性循环中,最终呼吸衰竭,因此预防和治疗肺部感染也是影响预后的重要措施。
DM/PM合并ILD的治疗目前尚无统一确定有效的方法,总体预后不理想。IVIG治疗DM/PM肌炎、皮疹的疗效已受肯定[13],但用于治疗ILD仍以小范围报道为主,病例数较少。近期Suzuki等[14]用IVIG 0.4 mg/kg静脉滴注5d治疗难治性DM/PM合并A/SIP安全有效,建议把IVIG从补救治疗的地位升至为DM/PM合并ILD患者的一线治疗药物。Bakewell等[2]报道1例66岁的DM/PM合并ILD患者,在强的松60mg/d等常规治疗疗效不佳的情况下每月静脉滴注IVIG 2mg/kg,共3个月,得以持续临床缓解2年,一氧化碳弥散量(DLCO)由预计值的35%升至55%。本研究中显示IVIG与DM/PM合并ILD患者的死亡负相关,5例早期应用中等剂量激素联合IVIG的A/SIP患者仅1例死亡,而4例应用大剂量激素冲击的A/SIP患者除1例死于心力衰竭外,其余3例均死于肺部感染、呼吸衰竭。考虑IVIG不仅有对ILD的治疗作用,还有一定的抗感染保护作用,而过度免疫抑制则增加感染风险且不利于感染的控制,故推荐对A/SIP患者尽早使用IVIG治疗,以期改善预后。但由于总体病例数少,IVIG的治疗地位仍需进一步论证。近年来也有研究发现细胞因子TNF-α在DM/PM疾病发病过程中有重要作用,使用TNF-α阻滞剂对这类患者可能有效[15]。本研究中有1例SIP经阿达木单抗治疗后好转,但现阶段对该治疗方案仍存争议,有待进一步循证医学检验。无症状的ILD患者肺部以轻度的小叶间隔增厚、条索状、网格状改变等表现为主,进展慢,预后好,应避免不必要的过度治疗。
综上所述,ILD是DM/PM的常见并发症,也是影响预后的危险因素。前期治疗经验提示不宜对DM/PM合并ILD患者采用大剂量激素冲击等过度免疫抑制治疗,建议选择IVIG等免疫支持,争取帮助患者度过A/SIP阶段,延缓肺间质纤维化的出现,改善预后,提高生存率及生活质量。
[1]Marie I,Hatron P Y,Dominique S,et al.Short-term and long-term outcomes of interstitial lung disease in polymyositis and dermatomyositis:a series of 107 patients[J].Arthritis Rheum,2011,63(11): 3439-3447.
[2]Bakewell C J,Raghu G.Polymyositis associated with severe interstitial lung disease:remission after three doses of IV immunoglobulin[J].Chest,2011,139(2):441-443.
[3]Bohan A,Peter J B.Polymyositis and Dermatomyositis[J].N Engl J Med,1975,292(7):344-347.
[4]Yamasaki Y,Yamada H,Ohkubo M,et al.Longterm survival and associated risk factors in patients with adult-onset idiopathic inflammatory myopathies and amyopathic dermatomyositis:experience in a single institute in Japan[J].J Rheumatol,2011,38(8): 1636-1643.
[5]Connors G R,Christopher-Stine L,Oddis C V,et al.Interstitial lung disease associated with the idiopathic inflammatory myopathies:what progress has been made in the past 35 years[J]? Chest,2010,138(6):1464-1474.
[6]Chen I J,Jan Wu Y J,Lin C W,et al.Interstitial lung disease in polymyositis and dermatomyositis[J].Clin Rheumatol,2009,28(6): 639-646.
[7]Stone K B,Oddis C V,Fertig N,et al.Anti-Jo-1 antibody levels correlate with disease activity in idiopathic inflammatory myopathy [J].Arthritis Rheum,2007,56(9):3125-3131.
[8]叶霜,黄文群,吴美芳,等.以急进性肺间质病变为突出表现的无肌炎的皮肌炎[J].中华风湿病学杂志,2006,10(9):527-533.
[9]阮晨曦,郑捷.皮肌炎患者Gottron皮疹与肺间质病变[J].中华皮肤科杂志,2009,42(1):19-21.
[10]Takada T,Suzuki E,Nakano M,et al.Clinical features of polymyositis/dermatomyositis with steroid-resstant interstitial lung disease[J].Intern Med,1998,37(8):669-673.
[11]Nakashima R,Mimori T.Clinical and pathophysiological significance of myositis-specific and myositis-associated autoantibodies[J].Int J Clin Rheumatol,2010,5(5):523-536.
[12]Won Huh J,Soon Kim D,Keun Lee C,et al.Two distinct clinical types of interstitial lung disease associated with polymyositis-dermatomyositis[J].Respir Med,2007,101(8):1761-1769.
[13]Cherin P,Pelletier S,Teixeira A,et al.Results and long-term followup of intravenous immunoglobulin infusions in chronic,refractory polymyositis:an open study with thirty-five adult patients[J].Arthritis Rheum,2002,46(2):467-474.
[14]Suzuki Y,Hayakawa H,Miwa S,et al.Intravenous immunoglobulin therapy for refractory interstitial lung disease associated with polymyositis/dermatomyositis[J].Lung,2009,187(3):201-206.
[15]Keystone E C.The utility of tumour necrosis factor blockade in orphan disease[J].Ann Rheum Dis,2004,63:79-83.
Clinical features of dermatomyositis/polymyositis complicated with interstitial lung disease
Objective To review the clinical characteristics and prognosis of dermatomyositis(DM)and polymyositis(PM) complicated with interstitial lung disease(ILD). Methods The clinical and laboratory data were collected from 141 patients with DM or PM admitted to Ningbo First Hospital from January 1997 to August 2012.The survival,predicting and prognostic factors of PM/DM patients complicated with ILD were analyzed retrospectively.Results Forty-two out of 141 DM/PM patients were complicated with ILD(29.8%).The 1,5,10-years survival rates were 76%,66%and 57%,respectively,with a median survival time of 127.3 months.The presence of clinical ILD and the hyoxemia were the risk factors for DM/PM (OR=2.536,95%CI 1.205-5.335, P=0.014 and OR=16.572,95%CI 3.238-84.817,P=0.001,respectively).Logistic regression showed that anti-Jo-1 antibody,mechanic's hand and hypoproteinemia were positively correlated with ILD in DM/PM.DM/PM complicated by acute or subacute interstitial pneumonia progressed rapidly with a high mortality(75%).Treatment with intravenous immuuoglobulin was negatively correlated with mortality in DM/PM-ILD patients(r=-0.331,P=0.032).Conclusion ILD is a common complication of DM/PM and is also a prognostic factor.The DM/PM patients with anti-Jo-1 antibody,mechanic's hand and hypoproteinemia tend to complicate with ILD.Hyoxemia is a risk factor of poor prognostic in patients with DM/PM-ILD.Early immuuoglobulin treatment might improve the prognosis of DM/PM-ILD.
Dermatomvositis Polymyositis Interstitial lung disease Prognosis


2013-07-16)
(本文编辑:严玮雯)
(本文由浙江省医学会风湿病学分会推荐)
315010 宁波市第一医院风湿科
忻霞菲,E-mail:xinxiafei0827@163.com
