淋巴免疫治疗过敏性哮喘的临床疗效
2013-04-09高春芳程相铎王俊琦李华信董学文张彩霞
雍 磊,高春芳,程相铎,王俊琦,李华信,董学文,贾 丹,张彩霞,何 静
(中国人民解放军第150中心医院变态反应中心,河南洛阳 471031)
ChinJAllergyClinImmunol,2013,7(2):160-166
过敏原特异性免疫治疗是目前唯一能改变过敏性疾病病程的病因治疗[1]。经典的治疗方法为皮下免疫治疗,虽然其对支气管哮喘、过敏性鼻炎、特应性皮炎及蜂毒过敏等的疗效显著[2-5],但因3~5年的疗程及多达30~70次的皮下注射,以及过敏相关性不良反应,使患者依从性大大降低,仅有约5%的变态反应性疾病患者接受特异性免疫治疗[6]。曾有研究表明,给予花粉及猫毛皮屑过敏患者行淋巴免疫治疗——淋巴结内注射变应原治疗,仅需3次治疗即可引起免疫耐受,且显著疗效[7-8]。然而,检索万方、中国期刊网及PubMed数据库,均未见淋巴免疫治疗过敏性哮喘的相关文献。笔者从2009年开始对屋尘螨致敏的哮喘患者进行淋巴免疫治疗,现总结如下。
对象和方法
对象及分组
选自2009年5月至2012年5月中国人民解放军第150中心医院门诊和住院的患者。
入选标准:(1)符合中华医学会呼吸病学分会哮喘学组2008年制定的《支气管哮喘防治指南》的支气管哮喘诊断标准[9];(2)皮肤点刺试验(skin prick test,SPT)屋尘螨变应原阳性2级以上,血清屋尘螨变应原特异性IgE(specific, sIgE)≥0.70 kUL,无花粉、霉菌及其他常见过敏原过敏者;(3)依从性较强,并签署知情同意书者;(4)年龄18~65岁,无过敏性鼻炎、结膜炎、特应性皮炎、荨麻疹等其他过敏性疾病,无严重心肺疾病及恶性肿瘤者。
排除标准:(1)有过敏原诱发过敏性休克史者;(2)伴有Ⅲ型过敏性疾病的患者;(3)有严重免疫病理改变的疾病和免疫缺陷病者;(4)存在应用肾上腺素禁忌症如高血压及心脏病患者;(5)严重心理障碍,无法配合免疫治疗者;(6)孕妇及儿童;(7)严重哮喘且药物不能控制者。
分组:纳入试验者按1∶1随机分为治疗组和对照组。
本研究经本院伦理委员会批准,所有入选患者均签署知情同意书。
试剂及仪器
屋尘螨过敏原制剂(商品名:安脱达,丹麦ALK-Abello公司),吸入组过敏原点刺液、一次性皮肤点刺针(丹麦ALK-Abello公司),Unicap100全自动变应原检测系统、酶标二抗和终止液(瑞典法玛西亚公司)、麦迪肺功能检测仪(比利时)。
检查方法
血清屋尘螨sIgE检测:用Unicap100全自动变应原检测系统,以荧光酶联免疫法按说明书检测两组患者治疗前后血清屋尘螨sIgE,灵敏度设为0.35 kUL,标准曲线最大值设为100.00 kUL。按照Unicap100系统的标准将检测值分为0~6级,检测值<0.35 kUL为0级,0.35≤检测值<0.70 kUL为1级,0.70≤检测值<3.50 kUL为2级,3.50≤检测值<17.50 kUL为3级,17.50≤检测值<50.00 kUL为4级,50.00≤检测值<100.00 kUL为5级,检测值≥100.00 kUL为6级。
治疗方案
治疗组:在上述药物治疗基础上加用标准化屋尘螨过敏原淋巴免疫治疗。淋巴免疫治疗方案:由专业医师操作,参考文献[7]并加以改进,在超声引导下分别于0、4、8、12、16和20周行腹股沟淋巴结内注射屋尘螨过敏原制剂,除0周用药剂量为100 SQ-U外,其余5次应用剂量均为1000 SQ-U。注射后至少留观30 min,观察并记录患者的不良反应。
哮喘控制测试
两组患者治疗前(0周)及治疗后4、8、12、16和20周分别进行哮喘控制测试(asthma control test, ACT)。向患者及家属详细解释哮喘控制测试(asthma control test, ACT)的方法和注意事项。详实记录ACT 5个问题的答案,即(1)过去4周内,在工作及学习环境或家中,哮喘妨碍进行日常活动的时间;(2)出现呼吸困难的次数;(3)因哮喘症状造成夜间觉醒比平时早醒的次数;(4)使用急救药物(如沙丁胺醇)的次数;(5)哮喘控制情况的评价。每个答案按严重程度分为1~5分,分别评分后得分相加为总分,满分25分为完全控制,20~24分为良好控制,低于20分为未控制[10]。
肺功能检测
两组患者在治疗前后分别用麦迪肺功能检测仪进行检测,主要观察第1秒用力呼吸容积占预计值百分比(percentage of forced expiratory volume in first second to predicted value, FEV1%)、第1秒用力呼吸容积与用力肺活量比值(ratio of forced expiratory volume in first second to forced vital capacity, FEV1FVC)和峰流速占预计值百分比(percentage of peak expiratory flow to predicted value, PEF%)。
药物用量评分
两组患者在治疗前1周每日记录相关药物使用情况,参照文献[11]的记分标准(茶碱缓释片0.1 g片=1分;吸入β2受体激动剂1喷=1分;吸入用糖皮质激素1喷=0.75分,口服激素换算成醋酸泼尼松片后,按照醋酸泼尼松片5 mg=1分计算)记录。将7 d用药评分相加得出总分,然后求平均值作为治疗前药物用量评分;淋巴免疫治疗结束后,按同样方法算出治疗后药物用量评分。
不良反应
参照文献[12]将特异性免疫治疗的不良反应分为小局部不良反应、大局部不良反应及全身不良反应。小局部不良反应:局部红肿区直径<40 mm。大局部不良反应:局部红肿区域≥40 mm。全身不良反应分级:0级为无症状或非特异性症状;Ⅰ级(轻度)为局部荨麻疹、鼻炎或轻度哮喘(峰流速下降<20%);Ⅱ级(中度)为出现缓慢的全身荨麻疹(>15 min)和(或)中度哮喘(峰流速下降<20%);Ⅲ级(重度)为快速发生的全身尊麻疹(<15 min)、血管性水肿或严重哮喘(峰流速下降>40%);Ⅳ级(过敏性休克)为迅速发生皮疹、皮肤潮红、红斑、全身荨麻疹,血管性水肿,哮喘发作,低血压等。
统计学处理
数据应用SPSS19统计软件进行统计分析。ACT评分组内比较用重复测量数值方差分析,组间比较采用多元方差分析进行比较。FEV1%、FEV1FVC、PEF%、血清屋尘螨变应原sIgE值和药物用量评分组间比较用独立样本t检验,组内治疗前后比较用配对样本t检验。P<0.05为差异有统计学意义。
结 果
一般情况
共筛选出72例患者,男30例,女42例;年龄为18~65岁,平均为(38.03±11.24)岁;病程为2~30年,平均(5.95±5.40)年。治疗组及对照组各36例,均为男15例,女21例,其年龄、病程均无统计学差异(均P>0.05)(表1)。
治疗组32例完成了淋巴免疫治疗,2例因怀孕退出,2例失访;对照组32例完成观察,4例失访。
ACT评分
两组治疗前(0周)ACT评分比较,差异无统计学意义(P>0.05)。治疗后4和8周两组间比较,差异均无统计学意义(P>0.05),治疗后12、16和20周,治疗组患者ACT评分明显高于对照组,差异均有统计学意义(P<0.01)。
表1治疗前两组患者的统计数据
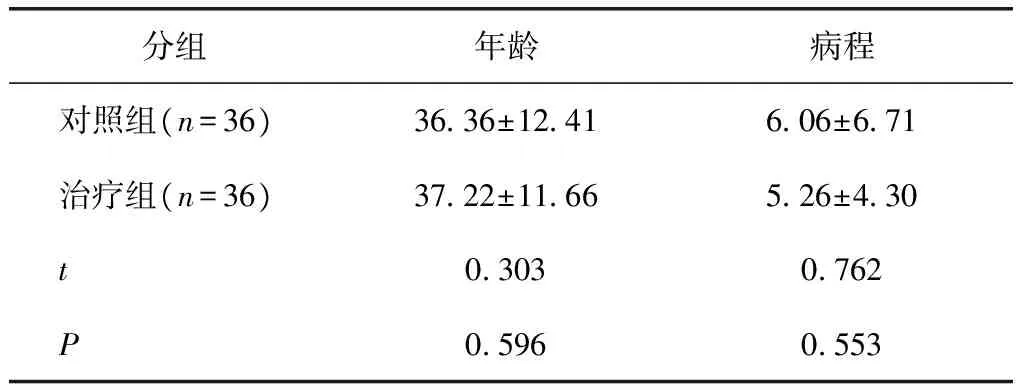
分组年龄病程对照组(n=36)3636±1241606±671治疗组(n=36)3722±1166526±430t03030762P05960553
治疗组组内比较,治疗后4、8、12、16、20周患者ACT评分与治疗前(0周)比较,差异均有统计学意义(P<0.01)。对照组组内比较,治疗后4、8、12、16、20周与治疗前(0周)比较,差异均有统计学意义(P<0.01)。
治疗后两组患者ACT评分均有升高,淋巴免疫治疗组升高程度明显优于对照组(表2、3,图1)。
肺功能检测
FEV1%:两组治疗前FEV1%无显著性差异(P>0.05);治疗后治疗组FEV1%显著高于对照组,差异有统计学意义(P<0.01)治疗组组内比较,治疗后FEV1%明显高于治疗前,差异有统计学意义差异(P<0.01);对照组组内比较,治疗前后FEV1%差异无统计学意义(P>0.05)。(表4)。
PEF%:两组治疗前PEF%无显著性差异(P>0.05);治疗后,治疗组PEF%显著高于对照组,两者差异有统计学意义(P<0.01)。治疗组,治疗后PEF%明显高于治疗前,差异有统计学意义(P<0.01),对照组治疗前后FEV1FVC差异无统计学意义(P>0.05)(表6)。
表2治疗组和对照组不同时相ACT值统计结果
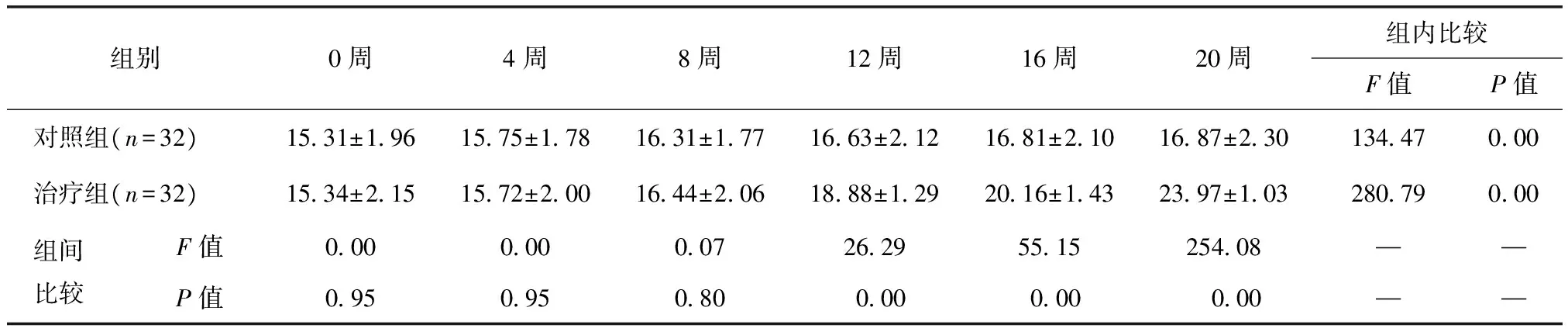
组别0周4周8周12周16周20周组内比较F值P值对照组(n=32)1531±1961575±1781631±1771663±2121681±2101687±23013447000治疗组(n=32)1534±2151572±2001644±2061888±1292016±1432397±10328079000组间比较F值0000000072629551525408——P值095095080000000000——
药物用量评分
两组治疗前药物用量评分无差异(P>0.05);治疗后治疗组药物用量评分明显低于对照组,差异有统计学意义(P<0.01)。治疗组治疗后药物用量评分明显低于治疗前,差异有统计学意义(P<0.01),对照组治疗后药物用量评分比治疗前降低,但差异无统计学意义(P>0.05)(表7)。

表3 治疗组和对照组患者治疗后不同时相ACT值的变异分析
表4两组治疗前后FEV1%值比较
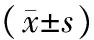

分组治疗前治疗后组内比较tP对照组(n=32)5406±8705491±779115026治疗组(n=32)5706±7497481±5911453000组间比较t1481152——P015000——
表5两组治疗前后FEV1FVC值比较
Table5Comparison of FEV1FVC values between before and after treatment of 2 groups

分组治疗前治疗后组内比较tP对照组(n=32)5813±8025944±877172009治疗组(n=32)6031±7047731±5431334000组间比较t116980——P025000——
血清屋尘螨变应原sIgE
两组治疗前血清屋尘螨变应原sIgE值无显著性差异;治疗后,治疗组血清屋尘螨sIgE较对照组明显降低,差异有统计学意义(P<0.01)。治疗组,治疗后血清屋尘螨变应原sIgE低于治疗前,差异有统计学意义(P<0.01),对照组治疗前后血清屋尘螨变应原sIgE差异无统计学意义(P>0.05)(表8)。
表6两组治疗前后PEF%的比较
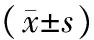

分组治疗前治疗后组内比较tP对照组(n=32)4947±7455038±813175009治疗组(n=32)5081±6577409±4711958000组间比较t0771428——P045000——
表7两组治疗前后药物用量评分比较
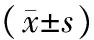

分组治疗前治疗后组内比较tP对照组(n=32)196±076192±077118025治疗组(n=32)219±078066±0431014000组间比较t116809——P025000——
表8两组治疗前后血清屋尘螨sIgE比较(kUL)
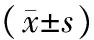
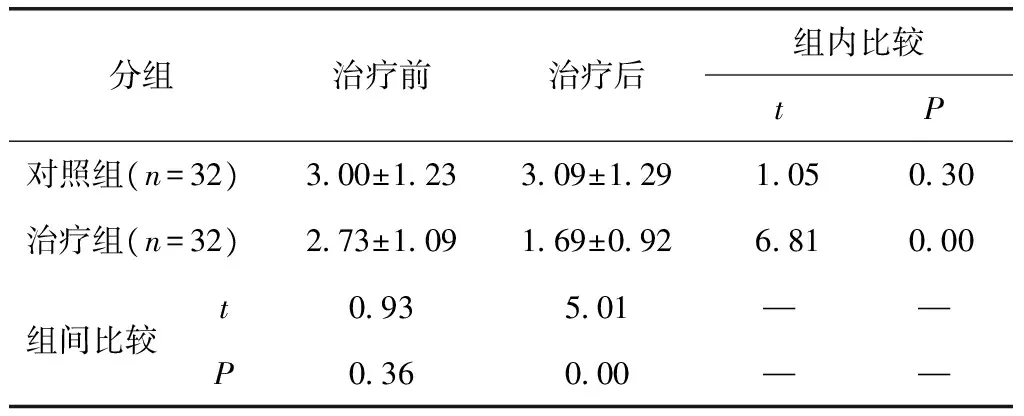
分组治疗前治疗后组内比较tP对照组(n=32)300±123309±129105030治疗组(n=32)273±109169±092681000组间比较t093501——P036000——
不良反应
32例治疗组患者共进行192次腹股沟淋巴结注射,未出现局部不良反应和全身不良反应。
讨 论
过敏原特异性免疫治疗过敏性哮喘不仅可减轻症状,还可预防哮喘发生[13]。但是,常规皮下免疫治疗因疗程长、注射次数多及可能发生不良反应,只有极少数患者能完成。近年来,舌下免疫治疗虽然免除了注射痛苦,但疗程仍未改变[14]。因此,缩短疗程、减少注射次数,以及减少不良反应可提高患者特异性免疫治疗的依从性。本研究采用淋巴免疫治疗方案,仅在半年内注射6次即可完成,缩短了疗程,同时减少了注射次数。
T、B淋巴细胞在发育过程中表面抗体的随机重排形成了众多的受体来识别抗原。尽管受体数目众多,但仅有1107的T淋巴细胞或B淋巴细胞能够识别特异性抗原。所以,激发免疫反应需将抗原呈现在大量淋巴细胞聚集的次级淋巴器官——淋巴结和脾脏中。淋巴结是蛋白质抗原传输、浓缩的主要场所,抗原递呈细胞在淋巴结内将抗原表位递呈给淋巴细胞,激发免疫反应,且T、B淋巴细胞相互作用也在淋巴结内进行[15]。皮下注射、舌下含服、肌肉注射等途径进入体内的过敏原只有很少部分通过淋巴管引流入区域淋巴结,激发免疫反应的效率很低。动物实验证实,将过敏原直接注入浅表淋巴结,与皮下注射和腹腔注射相较,可大大提高过敏原的利用率,免疫效应增强达106倍[16]。Senti等[7]应用标准化花粉过敏原给58例花粉症患者淋巴结内注射免疫治疗3次,并与54例花粉症患者皮下注射免疫治疗进行对照研究,结果显示淋巴免疫治疗产生的免疫耐受性与皮下免疫治疗3年相当。Senti等[8]进行重组猫毛皮屑过敏原淋巴结内注射,2个月内即可产生免疫耐受。本试验应用标准化屋尘螨过敏原,对屋尘螨致敏的哮喘患者在超声引导下行浅表淋巴结内注射,过敏原剂量由常规特异性免疫治疗的约4 000 000 SQ-U减少至5100 SQ-U,疗程缩短为20周,患者临床症状明显改善。
目前,呼吸系统过敏性疾病评价临床疗效的指标主要为症状改善情况和对症治疗药物的剂量[17]。本研究通过临床症状评分和药物用量评分进行淋巴免疫治疗疗效评价,结果表明,经过20周的淋巴免疫治疗,患者哮喘控制评分显著增加,药物评分明显降低,肺功能明显改善。同时,淋巴免疫治疗组可以更快、更早地(第8周)实现症状改善并减少药物使用剂量,这是其较常规皮下特异性免疫治疗方案的一大优势。
机体产生针对过敏原持久的免疫耐受是特异性免疫治疗的目的,通过免疫调节来改变免疫反应,是目前唯一通过免疫调节机制治疗过敏性疾病的方法。在过去的研究中,一般认为在特异性免疫治疗早期,血清过敏原sIgE增高,随着疗程延长,其水平逐渐降低[18]。本研究发现,仅20周即可引起患者血清屋尘螨sIgE显著降低,但机制尚待进一步研究。
免疫治疗过程中可能出现局部或全身不良反应、甚至危及生命的严重不良反应是患者依从性差的主要原因之一。特异性免疫治疗不良反应的发生与患者对过敏原的敏感性、应用剂量、注射方式、时机、医务人员操作失误、患者病情及疫苗是否为缓释载体等因素密切相关[17]。本研究采用国际标准化屋尘螨过敏原,剂量与常规免疫治疗相比减少约800倍,注射次数减少了10倍。32例患者均完成了淋巴免疫治疗,共行浅表淋巴结注射192次,无局部及全身不良反应发生,降低了不良反应的发生率,依从性良好。极少发生不良反应是淋巴免疫治疗的又一大优势。
总之,淋巴免疫治疗缩短了特异性免疫治疗的疗程、减少了过敏原的剂量和注射次数、降低了不良反应的发生率、起效快且临床疗效显著,为快速、安全、有效的病因治疗,值得推广应用。
(本文图1见封3)
[1]Larche M, Akdis CA, Valenta R. Immunological mechanisms of allergen-specific immunotherapy[J]. Nat Rev Immunol, 2006, 6:761-771.
[2]Jacobsen L, Niggemann B, Dreborg S, et al. Specific immunotherapy has long-term preventive effect of seasonal and perennial asthma: 10-year follow-up on the PAT study[J]. Allergy, 2007, 62:943-948.
[3]Varney VA, Tabbah K, Mavroleon G, et al. Usefulness of specific immunotherapy in patients with severe perennial allergic rhinitis induced by house dust mite: a double-blind, randomized, placebo controlled trial[J]. Clin Exp Allergy, 2003, 33:1076-1082.
[4]Bussmann C, Maintz L, Hart J, et al. Clinical improvement and immunological changes in atopic dermatitis patients undergoing subcutaneous immunotherapy with a house dust mite allergoid: a pilot study[J]. Clin Exp Allergy, 2007, 37:1277-1285.

[6]Martínez-Gómez JM, Johansen P, Erdmann I, et al. Intralymphatic injections as a new administration route for aAllergen-specific immunotherapy[J]. Int Arch Allergy Immunol, 2009, 150:59-65.
[7]Senti G, Prinz Vavricka BM, Erdmann I, et al. Intralymphatic allergen administration renders specific immunotherapy faster and safer: A randomized controlled trial[J]. PNAS, 2008, 105:17908-17912.
[8]Senti G, Crameri R, Kuster D, et al. Intralymphatic immunotherapy for cat allergy induces tolerance after only 3 injections[J]. J Allergy Clin Immunol, 2012, 129:1290-1296.
[9]中华医学会呼吸病学分会哮喘学组. 支气管哮喘防治指南(支气管哮喘的定义、诊断、治疗、疗效判断标准及教育和管理方案) [J]. 中华结核和呼吸杂志, 2008, 31:177-185.
[10] 庄少侠, 金珠凤, 王艳萍. 哮喘控制测试在哮喘管理中的应用[J]. 中国医师进修杂志, 2007, 30:20-21.
[11] 张罗, 王成硕, 王向东, 等. 变应性鼻炎集群免疫治疗的疗效和安全性临床分析 [J].中华耳鼻咽喉头颈外科杂志, 2008, 43:187-191.
[12] 郝飞, 宋志强. 特应性皮炎[M]. 北京:人民军医出版社, 2008:458-460.
[13] Maestrelli P, Zanolla L, Pozzan M, et al. Effect of specific immunotherapy added to pharmacologic treatment and allergen avoidance in asthmatic patients allergic to house dust mite[J]. J Allergy Clin Immunol, 2004, 113:643-649.
[14] Han DH, Rhee CS. Sublingual immunotherapy in allergic rhinitis[J]. Asia Pac Allergy, 2011, 1:123-129.
[15] Senti G, Johansen P, Kündig TM. Intralymphatic immunotherapy[J]. Curr Opin Allergy Clin Immunol, 2009, 9:537-543.
[16] Johansen P, Häffner A C, Koch F, et al. Direct intralymphatic injection of peptide vaccines enhances immunogenicity[J]. Eur J Immunol, 2005, 35:568-574.
[17] Cox L, Nelson H, Lockey R, et al. Allergen immunotherapy:apractice parameter third update[J]. J Allergy Clin Immunol, 2011, 127 :1-58.
[18] Akdis CA, Akdis M. Mechanisms of allergen-specific immunotherapy[J]. J Allergy Clin Immunol, 2011, 127:18-27.
