小剂量利妥昔单抗治疗系统性红斑狼疮或干燥综合征合并血小板减少症:长期随访研究
2013-04-09苏金梅吴庆军费允云郑文洁曾小峰张奉春
陈 华,苏金梅,王 迁,吴庆军,费允云,王 立,郑文洁,张 烜,曾小峰,张奉春
(中国医学科学院 北京协和医学院 北京协和医院风湿免疫科,风湿免疫病学教育部重点实验室,北京 100730)
ChinJAllergyClinImmunol, 2013, 7(2):139-145
自身免疫性血小板减少症是系统性红斑狼疮(systemic lupus erythematous,SLE)和干燥综合征(Sjoögren’s syndrome,SS)的常见合并症。目前,针对该合并症的常规治疗方法为应用糖皮质激素、人免疫球蛋白及免疫抑制剂,但对部分病例疗效不佳。利妥昔单抗(rituximab,RTX)为抗CD20单克隆抗体,能特异性杀伤表达CD20的B细胞[1],已应用于多种自身免疫病的治疗,包括类风湿关节炎[2]、原发性血小板减少性紫癜[3-5]和SLE[6-11]。RTX已成为特发性血小板减少性紫癜(idiopathic thrombocytopenic purpura,ITP)的标准二线治疗药物,减少脾脏切除率[12]。早期研究表明,给予SLE合并自身免疫性血小板减少症患者应用标准剂量RTX(375 mg/m2,1次/周,共4次)或小剂量RTX(100 mg,1次/周,共4次)均有良好短期疗效[13-14]。但RTX治疗的长期疗效仍有待明确,本研究对小剂量RTX治疗SLE或SS患者合并自身免疫性血小板减少症进行了长期随访研究,对RTX长期治疗的有效性和安全性进行评价,以期为临床治疗提供参考。
对象和方法
对象
纳入标准:2008年12月至2010年6月就诊于北京协和医院风湿免疫科SLE或SS合并重症难治性血小板减少症患者,诊断均符合相应分类标准[15-16]。重症难治性血小板减少症定义为重症血小板减少(血小板计数<10×109/L,或<30×109/L合并出血倾向)[12],且对甲泼尼龙冲击治疗(1 g/d,共3 d)和(或)人免疫球蛋白(20 g/d,共3~5 d)治疗无效,或大剂量糖皮质激素联合免疫抑制剂(环磷酰胺、长春新碱、环孢菌素等)治疗无效。
排除标准:(1)妊娠;(2)药物相关血小板减少;(3)重要脏器病变;(4)肿瘤;(5)活动性感染(包括乙型病毒性肝炎和丙型病毒性肝炎)。
研究方案获得北京协和医院伦理委员会批准,所有患者均签署书面知情同意书。
治疗方案
RTX 100 mg,1次/周静脉注射,共4次(第1、8、15和22天)[4],静脉注射前预处理均未使用糖皮质激素。口服糖皮质激素维持原始剂量,并在3~6月内逐渐减至最小维持剂量(≤泼尼松等效剂量7.5 mg/d)。在使用RTX前2周内停用免疫抑制剂。首次应用RTX后第2、4、12、24、52、76、104、128和156周随访。
实验室检查
在基线和各次随访时检查全血细胞计数、血生化、补体C3和C4、免疫球蛋白(IgG、IgA和IgM)、抗核抗体、抗双链DNA(double-stranded DNA,dsDNA)抗体、抗可提取性核抗原(extractable nuclear antigen,ENA)抗体、抗磷脂抗体及淋巴细胞亚群(CD19+B细胞、CD3+CD4+T细胞和CD3+CD8+T细胞)。外周血B细胞清除水平定义为:流式细胞检测外周血B细胞计数<5×106/L)。
疗效评价
每次随访进行疗效评价[3]。疗效评价基于主要疗效终点,无次要终点。
主要疗效终点:评价根据首次应用RTX后第12周血小板计数定义为(1)有效(complete response,CR):血小板计数>100×109/L;(2)部分有效(partial response,PR):50×109/L≤血小板计数≤100×109/L;(3)无效(no response,NR):血小板计数<50×109/L;(4)总体有效(overall response,OR):血小板计数>50×109/L。
不良事件
根据患者每次随访时症状、体征、实验室检查及影像学检查评价有无不良事件,并结合临床表现及联合用药情况评价该不良事件与RTX的相关性。
统计学处理
临床资料均使用描述性分析,数值以中位数、四分位数、极值表示,资料分析使用SPSS13.0软件。
结 果
一般情况
纳入13例患者,包括11例SLE和2例SS,均为女性患者。中位年龄为36岁(23~76岁),血小板减少症中位病程2年(0.5~10年),中位随访时间25个月(5~41个月)(表1)。所有病例均完成治疗方案。
主要疗效终点
首次应用RTX后第2周,分别有2例(15%)和1例(8%)达到CR和PR。
第12周OR达53%,其中5例(38%)达到CR,其中4例维持长期缓解,1例于52周后逐渐降至PR,并与128周后降至NR。2例(15%)达到PR,1例在36周后逐渐达到CR并长期维持,另1例逐渐降至NR。
第24周OR达到高峰9例(69%),其中6例(46%)达到CR,3例(23%)达到PR。此后OR呈下降趋势,第52周、104周和156周,分别为6例(46%)、6例(46%)和4例(31%)(图1A)。
有效组、部分有效组和无效组随访血小板计数改变分别见图1B、1C和1D。
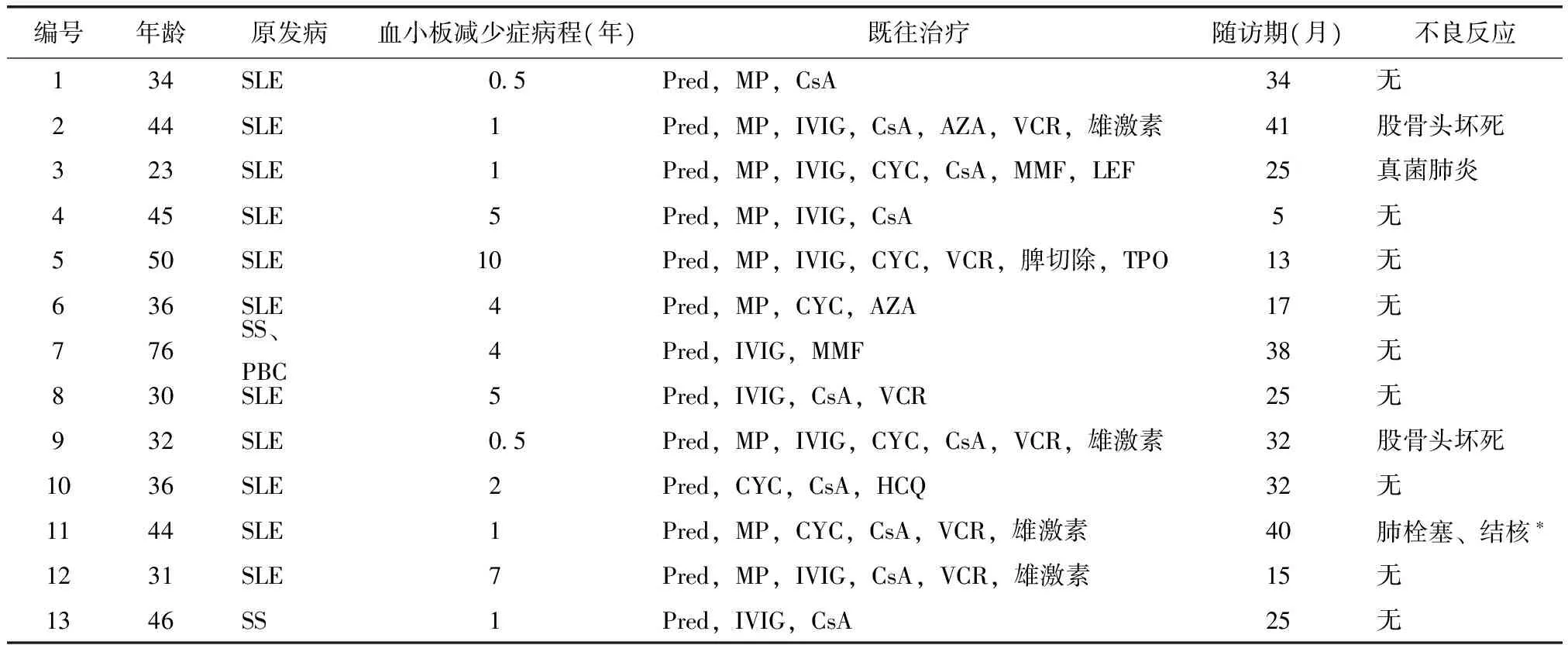
表1 SLE或SS患者合并重症难治性血小板减少症应用利妥昔单抗治疗基本资料
SLE:系统性红斑狼疮;SS:干燥综合征;PBC:原发性胆汁性肝硬化;Pred:泼尼松;MP:甲泼尼龙冲击;IVIG:人免疫球蛋白;CYC:环磷酰胺;CsA:环孢菌素;MMF:吗替麦考酚酸;LEF:来氟米特;VCR:长春新碱;TPO:血小板生成素;AZA:硫唑嘌呤;HCQ:羟基氯喹;*肺结核合并脑结核

图1SLE或SS患者合并重症难治性血小板减少症应用利妥昔单抗治疗效果
Fig1Platelet response of patients with lupus and Sjoögren’s syndrome
A:各随访期临床反应率;B:CR组(n=5)血小板计数变化;C:PR组(n=2)血小板计数变化;D:NR组(n=6)血小板计数变化
SLE:系统性红斑狼疮;SS:干燥综合征;PLT:血小板计数;CR:有效;PR:部分有效;NR:无效;N/A:无相应数据(失访或未到相应随访时间)
实验室指标变化
RTX治疗后,所有患者外周血CD19+B细胞计数均迅速下降。首次应用RTX后第4周,13例患者均达到外周血B细胞清除水平,并维持低水平至第24周,此后逐渐回升,直至第156周仍未恢复到治疗前水平(图2A)。血清免疫球蛋白水平呈轻度下降趋势,但未低于正常范围低限,在第24周后逐渐回升(图2B)。血清补体C3和C4水平在正常范围内,呈轻度上升趋势并在第24周达到高峰(图2C、2D)。
不良反应
轻度输液反应2例,均减慢输液速度后自行缓解,未终止治疗。1例在随访第4月发生肺动脉血栓,在随访第7月发生活动性结核,经抗凝、抗结核治疗后痊愈。2例出现股骨头无菌性坏死,行髋关节置换。1例在随访第25个月因真菌肺炎死亡(表1)。
讨 论
本研究是首个小剂量RTX治疗SLE或SS合并血小板减少的研究,且纳入病例均为难治性血小板减少症,对大剂量糖皮质激素甚至冲击剂量激素及多种免疫抑制剂无明显临床应答。在本研究中,小剂量RTX治疗表现出了良好疗效,在第12周和第24周时有53%和69%的病例分别达到CR和PR,临床疗效与小剂量RTX治疗ITP相仿[4-5]。本研究进一步证实了常规治疗无效的SLE或SS合并血小板减少症,小剂量RTX治疗较具潜力。
小剂量RTX起效较快,在首次应用4周时近50%病例即可达到CR或PR,仅经过半量治疗(2周)后少数病例即达到CR或PR。然而,因浆细胞不表达CD20,尽管RTX治疗迅速达到了B细胞清除水平,血清免疫球蛋白水平仍未发生显著改变。RTX治疗机制未明,推测可能系B细胞清除削弱其抗原呈递和分泌细胞因子等功能,以及影响辅助性T细胞亚群(T helper cell,Th) Th1/Th2转化和相关基因如Bcl-2和Bax的表达[17-18]。
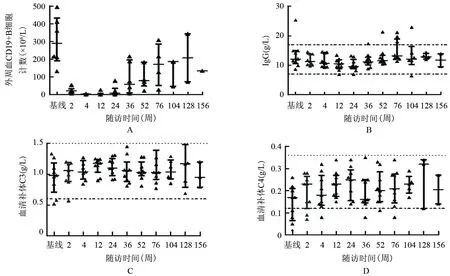
图2 SLE或SS患者合并重症难治性血小板减少症应用利妥昔单抗治疗后免疫学应答Fig 2 Immunological Response of Patients with Lupus and Sjoögren’s syndrome
在长达3年余的随访中,首次应用RTX第12周达到CR的病例多数能维持长期缓解,达到PR的病例中有1例在36周后逐渐达到CR并长期维持。因此,小剂量RTX治疗的长期疗效较稳定,对于第12周有临床应答(CR或PR)的病例,疗效多可长期维持。第12周的临床应答水平可能可作为长期应答的预测因素。鉴于本试验样本量小,还需要进一步研究证实。
RTX治疗后B细胞计数迅速达到清除水平,之后呈逐渐回升趋势,尤其是第24周后明显回升。其机制为原B细胞不表达CD20,在治疗后逐渐发育为成熟B细胞。小剂量和标准剂量RTX治疗的B细胞恢复趋势相仿,提示这两种剂量对外周血B细胞清除程度相近[19]。尽管多数病例B细胞计数呈持续上升趋势,但均未恢复基线水平,可能与复发较少相关。有研究表明,若恢复为纯真B细胞,则病情较少复发;若恢复为记忆B细胞,则病情复发可能性大[20]。此外,有研究报道RTX重复治疗可提高缓解率并延长缓解期[21]。
本研究中,输液反应的发生率较低,可能与RTX应用剂量小导致杀伤B细胞量较小有关。1例出现血栓事件,可能与合并的抗磷脂抗体有关。值得注意的是,尽管有报道RTX治疗可出现抗磷脂抗体综合征[22],但也有治疗后新发血栓事件的报道[23]。2例并发股骨头无菌性坏死的患者在既往治疗中使用了总计5次的甲泼尼龙冲击治疗,考虑糖皮质激素所致不良反应可能性大。严重感染是最严重的并发症,尤其是真菌感染和结核。1例患者因存在长期重度血小板减少,并对常规治疗反应不佳,先后接受多种免疫抑制剂甚至联合治疗,最终因严重免疫抑制并发肺部真菌感染死亡。建议给予患者应用RTX治疗时,应除外感染,且尽量避免免疫抑制剂联合治疗。
总之,本研究表明,对于SLE或SS合并难治性自身免疫性血小板减少症,小剂量RTX疗效较好,起效较快,长期疗效稳定,是一种较有前景的治疗方案。RTX治疗的安全性较好,但需谨慎除外感染。有必要开展RTX治疗的大规模对照研究,以进一步证实其长期疗效和安全性。
[1]Maloney DG, Grillo-Lopez AJ, White CA, et al. IDEC-C2B8 (Rituximab) anti-CD20 monoclonal antibody therapy in patients with relapsed low-grade non-Hodgkin’s Lymphoma[J]. Blood, 1997, 90:2188-2195.
[2]Emery P, Fleischmann R, Filipowicz-Sosnowska A, et al. The efficacy and safety of rituximab in patients with active rheumatoid arthritis despite methotrexate treatment: results of a phase IIB randomized, double-blind, placebo-controlled, dose-ranging trial[J]. Arthritis Rheum, 2006, 54:1390-1400.
[3]Garcia-Chavez J, Majluf-Cruz A, Montiel-Cervantes L, et al. Rituximab therapy for chronic and refractory immune thrombocytopenic purpura: a long-term follow-up analysis[J]. Ann Hematol, 2007, 86:871-877.
[4]Zaja F, Battista ML, Pirrotta MT, et al. Lower dose rituximab is active in adults patients with idiopathic thrombocytopenic purpura[J]. Haematologica, 2008, 93:930-933.
[5]Zaja F, Vianelli N, Volpetti S, et al. Low-dose rituximab in adult patients with primary immune thrombocytopenia[J]. Eur J Haematol, 2010, 85:329-334.
[6]Galarza-Maldonado C, Kourilovitch MR, Molineros JE, et al. The administration of low doses of rituximab followed by hydroxychloroquine, prednisone and low doses of mycophenolate mofetil is an effective therapy in Latin American patients with active systemic lupus erythematosus[J]. Autoimmun Rev, 2010, 10:108-111.
[7]Jónsdóttir T, Gunnarsson I, Risselada A, et al. Treatment of refractory SLE with rituximab plus cyclophosphamide: clinical effects, serological changes, and predictors of response[J]. Ann Rheum Dis, 2008, 67:330-334.
[8]Looney RJ, Anolik JH, Campbell D, et al. B cell depletion as a novel treatment for systemic lupus erythematosus: a phase I/II dose-escalation trial of rituximab[J]. Arthritis Rheum, 2004, 50:2580-2589.
[9]Sanz I, Lee FE-H. B cells as therapeutic targets in SLE[J]. Nat Rev Rheumatol, 2010, 6:326-337.
[10] Smith KGC, Jones RB, Burns SM, et al. Long-term comparison of rituximab treatment for refractory systemic lupus erythematosus and vasculitis: Remission, relapse, and re-treatment[J]. Arthritis Rheum, 2006, 54:2970-2982.
[11] Terrier B, Amoura Z, Ravaud P, et al. Safety and efficacy of rituximab in systemic lupus erythematosus: results from 136 patients from the French AutoImmunity and Rituximab registry[J]. Arthritis Rheum, 2010, 62:2458-2466.
[12] Neunert C, Lim W, Crowther M, et al. The American Society of Hematology 2011 evidence-based practice guideline for immune thrombocytopenia[J]. Blood, 2011, 117:4190-4207.
[13] Chen H, Zheng W, Su J, et al. Low-dose rituximab therapy for refractory thrombocytopenia in patients with systemic lupus erythematosus-a prospective pilot study[J]. Rheumatology (Oxford, England), 2011, 50:1640-1644.
[14] Zheng WJ, Zhang X, Wang Q, et al. Refractory severe connective tissue disease thrombocytopenia: is rituximab treatment effective and safe? [J]. Ann Rheum Dis, 2009, 68:1077-1078.
[15] Hochberg MC. Updating the American College of Rheumatology revised criteria for the classification of systemic lupus erythematosus[J]. Arthritis Rheum, 1997, 40:1725.
[16] Vitali C, Bombardieri S, Jonsson R, et al. Classification criteria for Sjögren’s syndrome: a revised version of the European criteria proposed by the American-European Consensus Group[J]. Ann Rheum Dis, 2002, 61:554-558.
[17] Stasi R, Cooper N, Del Poeta G, et al. Analysis of regulatory T-cell changes in patients with idiopathic thrombocytopenic purpura receiving B cell-depleting therapy with rituximab[J]. Blood, 2008, 112:1147-1150.
[18] Abdulahad WH, Meijer JM, Kroese FGM, et al. B cell reconstitution and T helper cell balance after rituximab treatment of active primary Sjögren’s syndrome: a double-blind, placebo-controlled study[J]. Arthritis Rheum, 2011, 63:1116-1123.
[19] Sutter JA, Kwan-Morley J, Dunham J, et al. A longitudinal analysis of SLE patients treated with rituximab (anti-CD20): factors associated with B lymphocyte recovery[J]. Clin immunol, 2008, 126:282-290.
[20] Leandro MJ, Cambridge G, Ehrenstein MR, et al. Reconstitution of peripheral blood B cells after depletion with rituximab in patients with rheumatoid arthritis[J]. Arthritis Rheum, 2006, 54:613-620.
[21] 张文. 系统性红斑狼疮生物疗药物浅谈[J]. 中华临床免疫和变态反应杂志, 2012, 6:85-87.
[22] Rubenstein E, Arkfeld DG, Metyas S, et al. Rituximab treatment for resistant antiphospholipid syndrome[J]. J Rheumatol, 2006, 33:355-357.
[23] Suzuki K, Nagasawa H, Kameda H, et al. Severe acute thrombotic exacerbation in two cases with anti-phospholipid syndrome after retreatment with rituximab in phase I/II clinical trial for refractory systemic lupus erythematosus[J]. Rheumatology (Oxford), 2009, 48:198-199.
