紫外分光光度法测定复方氢醌脂质体含量和包封率*
2013-02-06重庆医科大学附属永川医院重庆402160
刘 娟,廖 娟,李 远,金 梅(重庆医科大学附属永川医院,重庆 402160)
复方氢醌制剂结合了氢醌能降低皮肤色素沉着和维甲酸能消除皮肤细小的皱纹的特点,主要用于治疗黄褐斑、雀斑及炎症后色素沉着斑等[1]。然而,氢醌作为光感性物质,性质极不稳定,易氧化变色而失效,维甲酸则刺激性比较大[2-3]。笔者制备了复方氢醌脂质体,旨在对提高氢醌抗氧化能力和降低维甲酸的刺激性,但目前国内外尚无可用于复方氢醌脂质体体外分析的方法[4-6]。本研究拟建立其体外药物分析方法,为进一步分析其体外药物释放行为奠定基础。
1 材料与方法
1.1 仪器与试剂 CP224电子天平(上海奥豪斯),RE-52AA旋转蒸发仪(上海亚荣),SHB-Ш循环水式多用真空泵(上海瑞智),Varioskan Flash酶标仪(美国Thermo),Purelab classic纯水器(法国Elga),SB-5200DTDN超声波清洗机(宁波新芝),Neofuge 15R离心机(香港力康),GL-88B旋涡混合器(海门其林贝尔)。复方氢醌脂质体(氢醌1 200μg/mL,维甲酸200 μg/mL)和空白脂质体由本院中心实验室自制。氢醌(成都科龙)、维甲酸(上海安耐吉)、硫酸氢钠(天津大茂)、无水乙醇(美国Amresco)、Ⅱ-S型磷脂(美国Sigma)、胆固醇(纯度大于98%,上海生工生物)均为分析纯试剂。
1.2 方法
1.2.1 空白脂质体和复方氢醌脂质体的制备 联合采用薄膜分散法和超声法制备空白脂质体和复方氢醌脂质体。具体操作如下:称取处方量磷脂和胆固醇置于茄形瓶中,加入适量氯仿,待膜材溶解完全后,快速加入氢醌、维甲酸和硫酸氢钠的无水乙醇溶液后混匀,50℃水浴减压旋转蒸发,去除有机溶剂,制备均匀干膜;加入50℃预热的0.2mol/L磷酸缓冲液(pH5.7)50mL,旋转洗膜,超声30min,制备复方氢醌脂质体悬液,4℃放置备用。空白脂质体制备方法同上,加入的无水乙醇溶液不含氢醌和维甲酸。
1.2.2 方法专属性 按处方量称取维甲酸、氢醌和空白脂质体,无水乙醇完全溶解,分别进行紫外扫描。
1.2.3 线性范围 按处方量称取维甲酸和氢醌,无水乙醇完全溶解,制备200μg/mL维甲酸和1 200μg/mL氢醌混合溶液,分别用无水乙醇稀释40、20、10、8、5倍,每一浓度为3个样本,检测波长294、340nm处吸收峰,并对氢醌和维甲酸浓度作图,得到标准曲线。
1.2.4 精密度实验 取上述40、20、10倍稀释的维甲酸和氢醌混合溶液,以高、中、低3个浓度水平的混合样品进行检测。每一浓度制备5个样品,1d内连续测定5次计算日内精密度;每日测定1次,连续测定5d,计算日间精密度。将日内精密度代入回归方程,计算测得量,以测得量与加入量之比计算相对回收率。
1.2.5 回收率实验 分别在空白脂质体中加入维甲酸,使其浓度分别为0.50、0.75、1.00、1.25、1.50mg/mL,并按处方比例加入氢醌,空白脂质体定容至1mL,振荡混匀。取200μL破乳,稀释后分别在294、340nm处测定绝对回收率。
1.2.6 氢醌与维甲酸浓度检测 吸取复方氢醌脂质体0.2 mL至试管中,0.8mL氯仿破乳,加入0.8mL无水乙醇稀释,摇匀,取0.2mL稀释5倍后作为供试液,分别测定294、340 nm处吸收峰。根据标准曲线计算氢醌和维甲酸浓度。
1.2.7 脂质体包封率 取1mL脂质体悬液,4℃条件下12 000r/min离心20min,取上清液0.2mL,破乳稀释后测定包封率,包封率(%)=(C总-C上清液)/C总×100%[7]。
2 结 果
2.1 方法专属性 维甲酸和氢醌分别在波长340、294nm处有吸收;在294nm处,空白脂质体有一定吸收,对检测专属性有稍许影响,故检测脂质体氢醌含量时,须扣除空白脂质体在294nm的吸收;维甲酸在294nm处吸收小,对氢醌的干扰较小。氢醌和空白脂质体在维甲酸检测波长340nm处吸收较小,基本无干扰。见图1。
2.2 线性范围 维甲酸浓度5~40μg/mL,以340nm处光密度值(OD值)为纵坐标,以维甲酸浓度为横坐标,得到直线回归方程:Y=0.016 4X+0.054(r2=0.99,n=5)。氢醌浓度30~240μg/mL,以290nm处OD值为纵坐标,以浓度为横坐标,得到直线回归方程:Y=0.117 9X+0.158 1(r2=0.99,n=5)。
2.3 精密度和回收率 维甲酸、氢醌绝对回收率分别为96.6%[n=5,相对标准偏差(RSD)4.7%]和93.3%(n=5,RSD4.9%);相对回收率均值为80.95%。见表1。
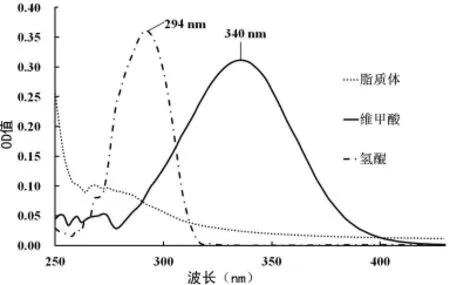
图1 维甲酸、氢醌及空白脂质体紫外扫描图

表1 日内精密度、日间精密度及方法回收率(n=5)
2.4 脂质体浓度与包封率 根据标准曲线计算氢醌和维甲酸的浓度分别为91.7%(RSD0.022)、90.0%(RSD0.019)。制备2个批次脂质体,氢醌包封率分别48.2%、48.9%,维甲酸包封率为77.1%、78.4%。
3 讨 论
氢醌是颜面皮肤色素沉着病局部用药的首选药物,由于为对苯二酚结构,性质极不稳定,易氧化变色而失效,在光照及碱性条件下尤甚,故本实验选无水乙醇作溶媒,棕色容量瓶做容器,以减少误差。由于无水乙醇易挥发,所以在测定紫外吸收时,比色皿均加盖,以减少由于溶媒挥发而造成误差。
本研究制备的复方氢醌脂质体结合了氢醌能降低皮肤色素沉着和维甲酸能消除皮肤细小皱纹的优势。利用脂质体作为药物载体,可增加药物溶出度,增强药物进入角质层或表皮类脂内的作用,增加药物在皮肤局部的积累,缓慢持续释放药物,有利于保持局部药物浓度[8-9]。
复方氢醌脂质体中的氢醌、维甲酸在紫外区都有吸收,故本研究将氢醌、维甲酸与空白脂质体单独扫描,结果显示按处方量用无水乙醇溶解的维甲酸和氢醌检测波长分别为294、340nm。在294nm的氢醌检测波长处,维甲酸吸收较小,对氢醌的干扰较小,但空白脂质体在该波长下有一定吸收,故在实际检测中,本研究用空白脂质体作对照,以扣除空白脂质体对氢醌检测的影响,平均回收率为86.76%。氢醌和空白脂质体在340nm的维甲酸检测波长处吸收较小,基本无干扰,因此维甲酸仍在340nm波长处检测。用紫外分光光度法测定复方氢醌脂质体浓度和包封率结果准确可靠,简单易行,可推广。
[1]李宗华,方远芳,阮红,等.维A酸霜与氢醌霜联合治疗黄褐斑50例[J].中国美容医学,2007,16(11):1571-1572.
[2]李国成,陈楚雄,马永良,等.基质及附加剂对氢醌乳膏稳定性的影响[J].广东药学,2005,15(4):74.
[3]邢卫斌,付国俊,张秉新,等.维甲酸对体外培养的正常人黑素细胞的影响[J].河北医药,2005,27(1):27-28.
[4]陈新谦,金有豫.新编药物学[M].16版.北京:人民卫生出版社,2007:594.
[5]杨桂明,谷健梅,宋丽艳.脂质体技术在化妆品制剂中的应用[J].中国美容医学,2009,18(3):396-398.
[6]杨彤.新型脂质体的研究进展[J].医药导报,2009,28(3):336-338.
[7]蔡明志,黄复生,王昆.维甲酸脂质体的制备及评价[J].中国新药杂志,2006,15(14):1181-1183.
[8]Sharma P,Jain D,Maithani M,et al.Development and characterization of dutasteride bearing liposomal systems for topical use[J].Curr Drug Technol,2011,8(2):136-145.
[9]徐今宁.脂质体作为皮肤局部给药载体的研究与应用[J].河北北方学院学报,2008,25(5):73-76.
