用加速量热仪研究双基发射药的绝热分解特性
2013-01-29贾昊楠路桂娥江路明安振涛江劲勇
贾昊楠,路桂娥,江路明,安振涛,江劲勇
(1.军械工程学院,河北 石家庄050003;2.军械工程学院军械技术研究所,河北 石家庄050003;
3.中国石油大学,北京102249)
引 言
目前,研究发射药热分解特性和热稳定性通常采用的热分析方法有热重分析(TG)、差热分析(DTA)以及差示扫描量热(DSC)。由于这些方法使用的样品量仅为几毫克,测试结果受样品的均一性影响较大,同时无法测得分解产物的压力,因此,在热安定性测试上存在缺陷,绝热加速量热仪(ARC)可弥补这方面的不足[1]。
绝热加速量热仪具有测试数据丰富,测试样品量为克量级的特点,在一定程度上能够保证取样的均匀性和代表性。国内周新利[2]等人利用ARC 研究了某新型膨化硝铵炸药在绝热条件下的热分解过程,计算出绝热分解动力学参数。王志新[3]等人采用ARC研究了一种新型塑性炸药PBX-HKF 的热分解特性,并发现该炸药具有良好的热稳定性。此外,还有许多关于使用ARC 研究炸药绝热分解研究的报道[4-8]。
本实验用基于绝热原理设计的加速量热仪研究了SF-3双基发射药的热分解过程,计算了动力学参数,为更深入了解发射药的热分解特性提供参考。
1 绝热动力学模型的建立[4,8-10]
1.1 绝热动力学方程的推导
Wilhelmy发现在酸性条件下反应速率与蔗糖的剩余量有关,Waage正式提出质量作用定律,即:

通常式(1)只适用于气相或均相溶液的一些反应。对于固体含能材料的均相反应,可假设反应物质的转变分数为α,则反应速率为:


在绝热条件下,化学反应产生的热量全部用于加热反应物自身,因此可由能量守恒原理得到:Cv为反应物的平均热容;ΔTad为单位时间反应物的绝热温升,ΔTad=Tf-T0;Q为单位时间单位质量反应物产生的热量。
式(3)两边对时间t求导,可得:
式中:m为反应物的质量;


式(5)表达了在绝热条件下的化学动力学原理。
根据Arrhenius公式:

对于简单放热反应反应机理函数为:
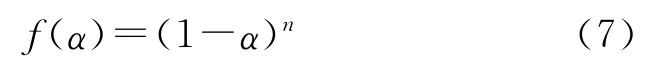
式中:n为反应级数。其升温速率方程为:

1.2 测试结果的修正
以上绝热动力学方程的推导是基于一种理想情况,即化学反应放出的热量全部用于加热样品自身,而实际上还需要考虑反应容器对热量的吸收。在这种近似绝热条件下,根据热力学原理,可得平
衡方程为:

式中:mb为反应容器质量;为反应容器的平均热容;为由样品和样品容器等组成系统的温升速率。
引入惰性因子φ:
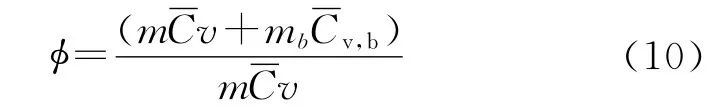
反应系统的温升速率可以表示为:
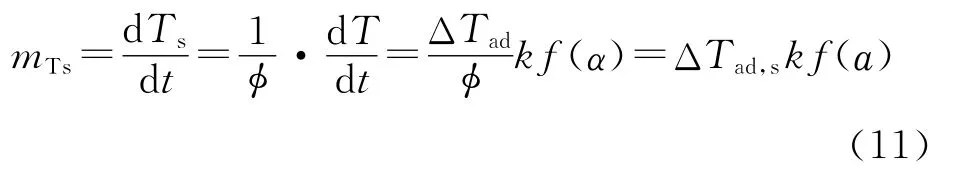
式中:ΔTad,s为由样品和样品容器等组成系统的绝热温升,。
若热惰性因子对简单放热反应过程的机理没有影响,则样品的初始放热温度为:
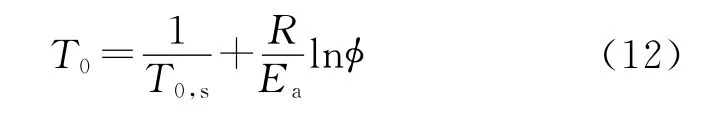
样品放热终止温度为:

1.3 绝热动力学参数计算
为了求指前因子A和活化能E,对式(5)两端取积分,可得:
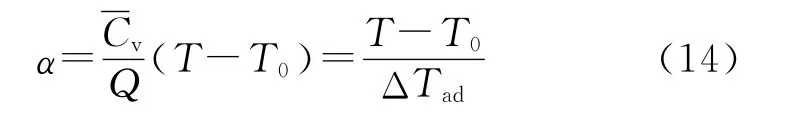
将上式代入式(7),可得:
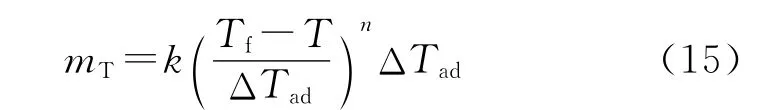
经整理可得:

通过ARC可以测得样品的温升速率mT、Tf以及ΔTad。在Arrhenius公式两边取对数可得:
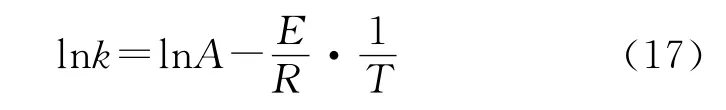
当反应级数选取合适时,将计算得到的lnk代入式(16),lnk-成一条直线,由直线斜率和截距可分别计算得到指前因子A和活化能E。
2 实 验
2.1 样 品
SF-3双基发射药,山西北方兴安化学工业有限公司,配方为:硝化棉56.0%(质量分数,下同)、硝化甘油26.5%以及二号中定剂3.0%。
2.2 仪器与测试条件
绝热加速量热仪(ARC),英国热危险技术公司(THT)生产,原理及结构参见文献[1-2,9-10]。样品量及测试条件见表1。密闭样品容器为四分之一英寸口径的厚壁钛合金小球(Ti-LCQ)。
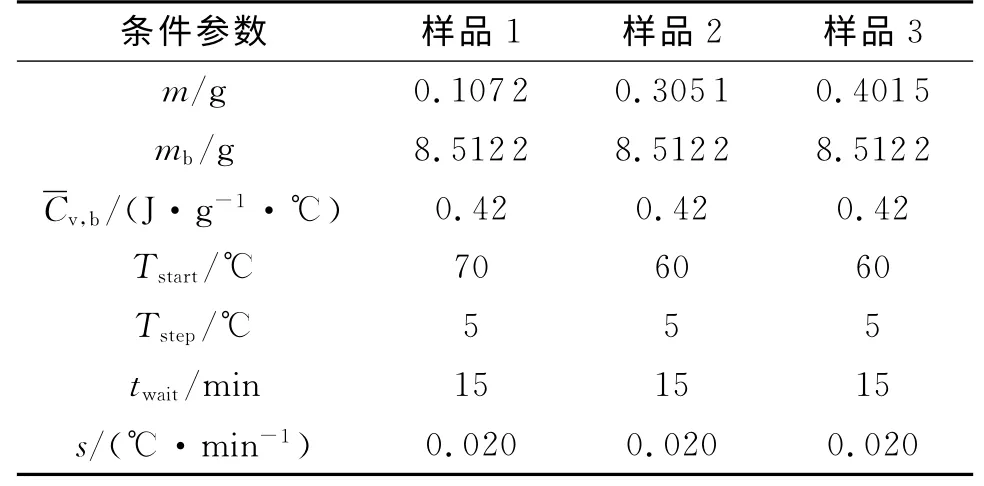
表1 样品量及测试条件Table 1 Mass of samples and measuring conditions
3 结果及讨论
3.1 双基发射药的热分解特性
用ARC测试3种质量双基发射药的热分解过程,结果如图1和图2所示,其绝热分解特性及热力学参数见表2,修正后的绝热分解特性参数见表3。
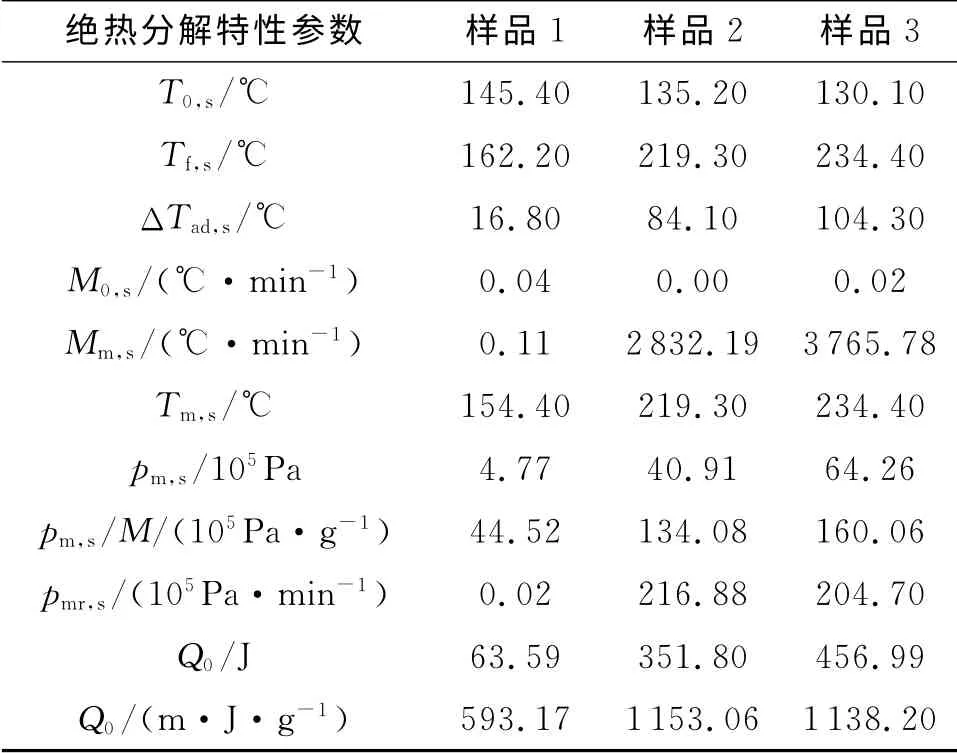
表2 双基发射药的绝热分解特性参数及热力学参数Table 2 Thermal decomposition characteristic data and thermodynamic parameters of double-base gun propellant
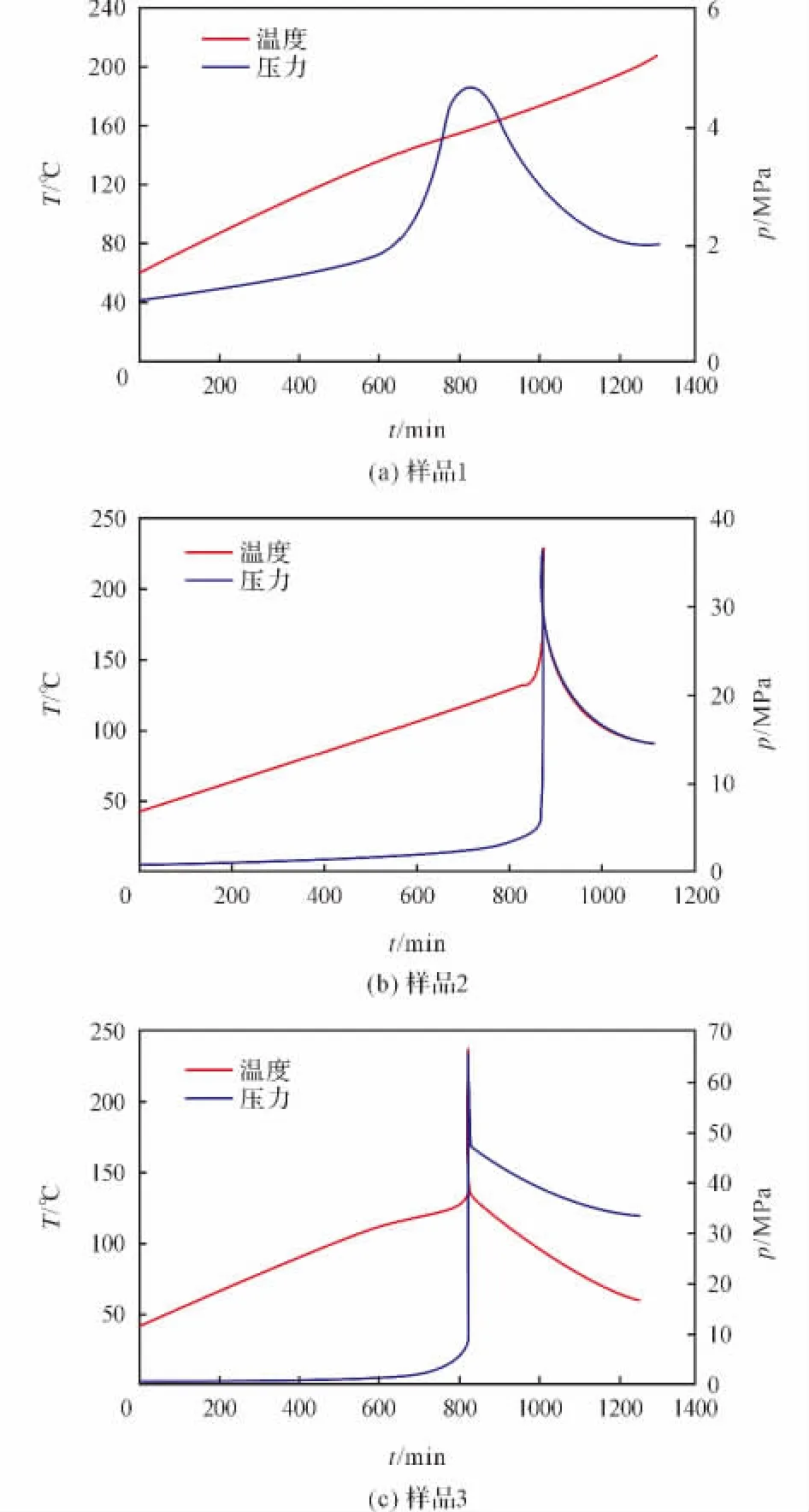
图1 3种样品的T-t和p-t曲线Fig.1 T-t and p-t curves of three samples
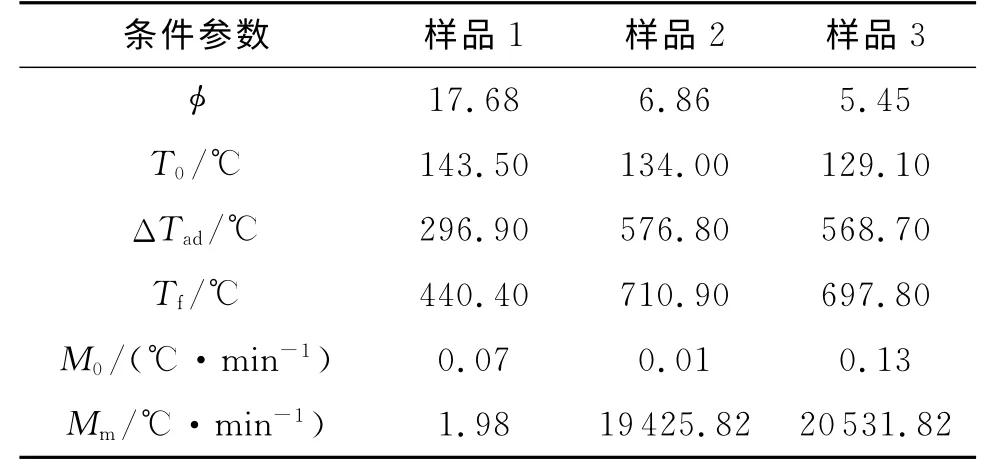
表3 热分解特性参数的校正结果Table 3 Modified results of thermal decomposition characteristic parameters
由图1(a)、图2(a)和表3可以看出,当样品质量为0.1072g时,热惰性因子φ为17.68,双基发射药发生缓慢的热分解反应,其绝热分解可分为3个阶段:

图2 3种样品的β-t和p-t曲线Fig.2 β-t,pmrosand p-t curves of three samples
(1)升温速率缓慢上升阶段。当加速量热仪探测到样品发生分解反应前,存在缓慢的分解反应,并释放出少量的气体产物。
(2)升温速率持续提高阶段。在143.50℃样品出现分解反应之后,升温速率持续提高,压力在达到最大值后,随升温速率的提高而降低。在154.40℃时样品的升温速率达到最大值1.98℃/min。
(3)升温速率降低阶段。升温速率达到最大值以后,随着反应物的消耗,升温速率逐渐降低,直到反应结束,此时样品温度达到最大值440.50℃。
在整个绝热分解反应过程中,样品的绝热升温为297.00℃,单位质量反应物产生的最大气体压力为4.452MPa/g,单位质量放热量为593.17J/g。
由图1(b)~(c)、图2(b)~(c)和表3 可以看出,当样品质量分别为0.3051g和0.4015g时,热惰性因子φ分别为6.86和5.45。两种质量的样品具有相近的绝热分解特性,并均发生了快速的热自燃反应。如样品3,在128.90℃出现热分解反应,初始放热速率为0.02℃/min,随着温度的提高,样品内部热量积累逐渐增多,在160℃左右时,样品发生快速的燃烧反应,放热速率迅速增大,温度急剧上升。样品最大温升速率为20 531.82℃/min,反应终止时温度为697.60℃,单位质量反应物产生的最大气体压力为16.006MPa/g,单位质量放热量为
1 138.20J/g。
3.2 绝热分解动力学参数计算
通过Origin 7.5软件对测试数据进行计算,得到双基发射药绝热分解动力学参数,结果见表4。
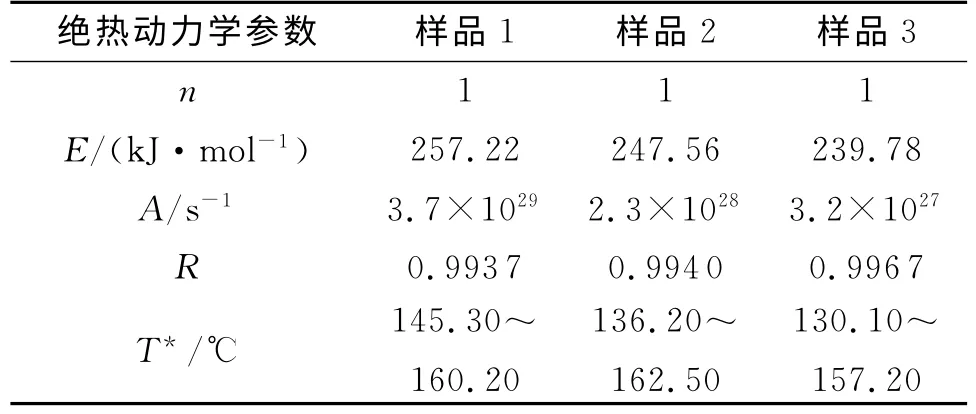
表4 绝热分解动力学参数计算结果Table 4 Calculated results of adiabatic decomposition reaction kinetic parameters
通过计算得到,双基发射药绝热分解反应的反应级数为1,其表观活化能为239.78~257.22kJ/mol。
4 结 论
(1)用速率常数法确定了双基发射药的绝热分解反应的反应级数为1,表观活化能为239.78~257.22kJ/mol。
(2)热惰性因子φ值较大时,双基发射药仅发生缓慢的热分解反应;φ值较小时,在热分解的基础上还发生了快速的燃烧反应,并释放出大量气体和热量。因此,φ值较小时,样品自加热反应速率较大,发生快速燃烧反应的可能性增大。
(3)样品质量较大时,T0较低,Mm、Pmr,s以及Pm,s/M等值均较高,说明φ值大小对样品绝热分解特征量有较大的影响。因此用ARC 测试或评价含能材料的热稳定性,应该统一反应容器的材料和尺寸、试样量及其他相关试验条件等。
[1]王耘.含能材料热安全性的绝热评价方法研究[D].北京:北京理工大学,1998.
WANG Yun.Studies on the adiabatic assessment method of the thermal safety of energetic materials[D].Beijing:Beijing Institute of Technology,1998.
[2]周新利,刘祖亮,吕春绪.3#煤矿许用膨化硝铵炸药的绝热分解[J].火炸药学报,2007,30(5):15-18.
ZHOU Xin-li,LIU Zu-liang,LüChun-xu.Adiabatic decomposition of No.3permissible expanded ammonium nitrate explosive[J].Chinese Journal of Explosives and Propellants,2007,30(5):15-18.
[3]王志新,李国新,劳允亮,等.用加速量热仪研究PBX-HKF的热稳定性[J].含能材料,2005,13(2):113-127.
WANG Zhi-xin,LI Guo-xin,LAO Yun-liang,et al.Study on thermal stability of PBX-HKF by accelerating rate calorimeter[J].Energetic Materials,2005,13(2):113-127.
[4]张凤.简单放热化学反应体系热安全性研究判据[J].中国安全生产科学技术,2011,7(8):79-82.
ZHANG Feng.Research criteria of thermal safety of simple exothermic chemical reaction system[J].Journal of Safety Science and Technology,2011,7(8):79-82.
[5]沈立晋,汪旭光.采用加速量热法评价防爆硝酸铵的热稳定性[J].火炸药学报,2004,27(2):73-76.
SHEN Li-jin,WANG Xu-guang.The thermal stability evaluation of anti-explosive ammonium nitrate by ac-celerating rate calorimeter[J].Chinese Journal of Explosives and Propellants,2004,27(2):73-76.
[6]周新利,刘祖亮,吕春绪.岩石乳化炸药绝热分解安全性的加速量热法分析[J].火炸药学报,2003,26(2):62-65.
ZHOU Xin-li,LIU Zu-liang,LüChun-xu.Analysis on adiabatic decomposition safety of rock emulsion explosive using acceleration rate calorimeter[J].Chinese Journal of Explosives and Propellants,2003,26(2):62-65.
[7]Turcotte R,Lightfoot P D.Thermal hazard assessment of AN and AN-based explosives[J].Journal of Hazardous Materials,2003,A101:1-27.
[8]冯长根,傅智敏,钱新明.绝热方法评价热安定性的改进模型与应用[J].北京理工大学学报,2003,23(1):22-25.
[9]刘丽.绝热加速量热仪理论及应用的若干研究[D].北京:北京理工大学机电工程学院,2005.
LIU Li.Study on the theory and application of accelerating rate calorimeter[D].Beijing:Beijing Institute of Technology,2005.
[10]郭洪.利用加速量热仪(ARC)研究热分析动力学反应机理[J].曲靖师范学院学报,2005,24(3):1-3.
GUO Hong.Application of accelerating rate calorimeter(ARC)to the thermoanalytic study on dynamics mechanism[J].Journal of Qujing Teachers College,2005,24(3):1-3.
