星点设计-效应面法优化氯化血红素滴丸处方
2013-01-04何丹鸿袁曦洪清叶景鹏福建医科大学附属第一医院药学部福建福州350005福建医科大学药学院福建福州35000
何丹鸿,袁曦,洪清,叶景鹏 (.福建医科大学附属第一医院药学部,福建 福州350005;.福建医科大学药学院,福建 福州35000)
氯化血红素(hemin)具有生物利用度高、无体内铁蓄积中毒及胃肠刺激等优点,同时还是抗贫血和抗肿瘤药物的重要原料[1-3]。氯化血红素滴丸是我院治疗缺铁性贫血的医院制剂,其主要成分氯化血红素为难溶性药物,对于难溶性药物口服固体制剂,药物在制剂中的分散状态是影响溶出与吸收的主要因素。固体分散技术能将难溶性药物高度分散于适宜的载体材料中,利用载体与药物形成固体分散体系,药物主要呈胶体、分子、或微晶状态分散于载体中,使药物总表面积增大,从而溶出速率加快,吸收完全,使其溶度维持在有效治疗窗内,对进一步提高其生物利用度具有重要的意义。本实验以PEG6000和Poloxamer 188为联合载体,应用集数学和统计学方法于一体的星点设计(central composite design,CCD)-效应面优化法(response surface methodology,RSM)优化氯化血红素滴丸的处方,并通过体外溶出度来考察其释放效果,为氯化血红素的新剂型研究提供了理论依据。
1 仪器与材料
BS110S型电子分析天平(德国赛多利斯);pHS-3C型精密pH计(上海雷磁仪器厂);TU-1901型双光束紫外可见分光光度计(北京普析通用仪器有限责任公司);ZRS-6型智能溶出试验仪(天津大学无线电厂)。
氯化血红素对照品(美国Sigma-Fluka化学公司,批号1206798,纯度≥98%);氯化血红素供试品(福建省医学科学研究所提供,纯度≥94%);氯化血红素分散片(本院制剂室提供,批号20121108);氯化血红素胶囊(福建中加美保健品开发有限公司提供,批号20111214);泊洛沙姆188(Poloxamer 188,江苏海安石油化工厂,批号20120426);聚乙二醇6000(PEG6000,国药集团化学试剂有限公司,批号20061117);无水乙醇(天津市永大化学试剂开发中心,批号20061221);氢氧化钠(上海化学试剂总厂,批号20070818);磷酸氢二钠(天津市光复细化工研究所,批号20021115);磷酸二氢钠(鑫科股份合肥工业大学化学试剂厂,批号20010101);十二烷基硫酸钠(SDS,天津市永大化学试剂开发中心,批号20060518)。
2 方法与结果
2.1 氯化血红素滴丸的制备 分别称取PEG6000和Poloxamer 188适量,置水浴上加热熔融,待完全熔融后缓缓加入用少量碱性无水乙醇溶解的氯化血红素,边加边搅拌,加热至无乙醇味,将熔融物保持温度,并滴入冷却液中,取出成形的滴丸用滤纸吸附滴丸表面的冷却液,低温真空干燥48 h,即得。
2.2 测定波长的选择 精密称取经105℃干燥至恒重的氯化血红素对照品18.5 mg,以0.1 mol·L-1氢氧化钠溶液为溶剂,配成5.55μg·mL-1的溶液。取上述溶液在300~500 nm波长之间扫描吸收光谱,结果本品在(385±2)nm波长处有最大吸收。
2.3 标准曲线的制备 精密称取经105℃干燥至恒重的氯化血红素对照品18.5 mg,置于100 mL量瓶中,加0.1 mol·L-1氢氧化钠溶液适量,使之完全溶解后,稀释至刻度,摇匀,分别精密吸取上述溶液0.5,1.0,2.0,3.0,4.0,5.0mL,置 于 100 mL 量 瓶中,用0.1 mol·L-1氢氧化钠溶液稀释至刻度,摇匀,以溶剂为空白,用分光光度计在(385±2)nm波长处测定吸光度,经线性回归,得回归方程:A=0.095 5C+0.003 4,r=0.999 3(n=6)。结果表明,本品在0.93~9.25μg·mL-1范围内与吸光度呈良好的线性关系。
2.4 辅料对吸光度的影响 以空白样品在(385±2)nm波长处进行扫描,结果得PEG6000和Poloxamer 188在此波长处无吸收,提示辅料对吸光度测定没有影响。
2.5 稳定性试验 分别将上述标准液于0.0,0.5,1.0,3.0,6.0,12.0h测定其吸光度。结果表明,吸光度基本不变,提示供试品至少在12 h内稳定。
2.6 精密度试验 精密称取经105℃干燥至恒重的氯化血红素对照品约18.5 mg,9份,按“2.3”项下的方法制备高、中、低3个质量浓度的溶液各3份,以溶剂为空白,用分光光度计在(385±2)nm波长处测定吸光度,代入回归方程计算,得RSD为0.87%,提示精密度良好。
2.7 加样回收率试验 取已知含量的样品(约相当于氯化血红素20 mg)9份,置于100 mL量瓶中,用0.1 mol·L-1氢氧化钠溶液溶解并定容,吸取上述溶液10 mL置于50 mL量瓶中,用0.1 mol·L-1氢氧化钠稀释至刻度,摇匀,得备用供试品溶液,取供试品溶液10 mL,置于100 mL量瓶中,按高、中、低3个质量浓度,分别精密加“2.3”项下的溶液10 mL,用0.1 mol·L-1氢氧化钠溶液定容,以溶剂为空白,用分光光度计在(385±2)nm波长处测定吸光度,代入回归方程计算,结果表明:平均回收率为98.68%,RSD为0.87%。
2.8 样品的含量测定 分别精密称取氯化血红素滴丸适量(相当于氯化血红素约20 mg),按“2.7”项下的方法测定含量,结果平均含量分别为98.04%,RSD为0.93%。
2.9 丸重差异 按《中国药典》2010年版(二部)附录Ⅰ H丸剂[3]项下规定,取本品20丸,精密称定总质量,求得平均丸重后,再分别精密称定各丸的质量。每丸质量与平均丸重相比较。
2.10 溶出度试验 取上述滴丸适量(相当于氯化血红素30 mg),按《中国药典》(2010年版)二部附录ⅩC第一法[3],以加入0.5%十二烷基硫酸钠(SDS)pH6.8的磷酸盐缓冲液900 mL为溶出介质,温度(37±0.5)℃,转速105 r·min-1,在5,10,60 min时定位吸取样品20 mL(同时补充等量介质),立即经0.45μm微孔滤膜滤过。取续滤10 mL置于50 mL量瓶中,用0.1 mol·L-1氢氧化钠液稀释至刻度,摇匀,以溶剂为空白,用分光光度计在(385±2)nm波长处测定吸光度,代入回归方程计算不同时间段的溶出度。
2.11 优化试验
2.11.1 因素水平 参考相关文献[4-5]及单因素试验结果,选择对滴丸成形及释放速率有显著性影响的主药质量分数(X1)和Poloxamer 188质量分数(X2)作为考察因素。按CCD设计为2因素5水平,因素极值分别为X1=15%~35%,X2=30%~60%。因素水平见表1。
2.11.2 实验安排与结果 根据实验安排表进行试验,并测定滴丸的丸重差异和溶出度,以丸重差异及5,10,60 min的溶出度作为评价指标。实验安排和结果见表2。
2.11.3 数据处理 应用SPSS17.0统计软件对实验结果进行数据处理,以主药质量分数X1和Poloxamer 188质量分数X2分别对丸重差异及5,10,60 min溶出度评价指标进行多元线性回归和二次多项式拟合。对于拟合方程各个系数分别进行方差分析(ANOVA)及t检验。结果表明,线性回归方程的复相关系数(r)均小于0.9,相关性差,拟合度也较差;相比而言,二次多项式拟合方程的r值大幅提高,且从表3方差分析结果可见整体模型达显著水平(P<0.05),故选用二次多项式拟合方程进行模型的预测。

表2 实验安排及结果Tab 2 Experiment design and results
2.11.4 处方优化与预测 根据二项式方程,应用Origin 7.5软件分别绘制三维效应面和等高线图。见图1~8。
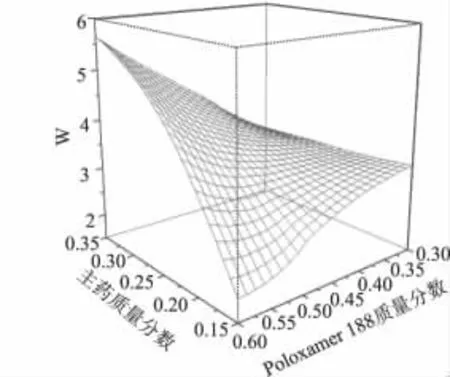
图1 W 对X1和X2的效应面Fig 1 Response surface of Was a function of X1and X2

图2 D5对X1和X2的效应面Fig 2 Response surface of D5as a function of X1and X2
从三维效应面的趋势及二维等高线图的较优区域,并综合各方面影响因素,在本实验中丸重差异越小越好,即选取等高值趋小的曲面范围;而氯化血红素滴丸作为一种速释制剂,其溶出速度越快越好,故氯化血红素滴丸在5,10,60 min的溶出度越大越好,即尽可能选取等高值趋大的曲面范围。从三维效应面及二维等高图可得到对应的较佳实验条件范围,几个效应所选择的较佳条件通过叠加,进一步统一较佳条件范围。由图1~8优选出2个因素较佳的处方条件范围,X1为16%~28%,X2为40%~60%,代入二项式拟合处理。综合药剂学范畴,在有利于制备符合标准产品的情况下,考虑到主药应尽可能多,载体量尽可能少,能更好地节省成本等几方面因素,得到最佳取值,X1为23%,X2为45%。
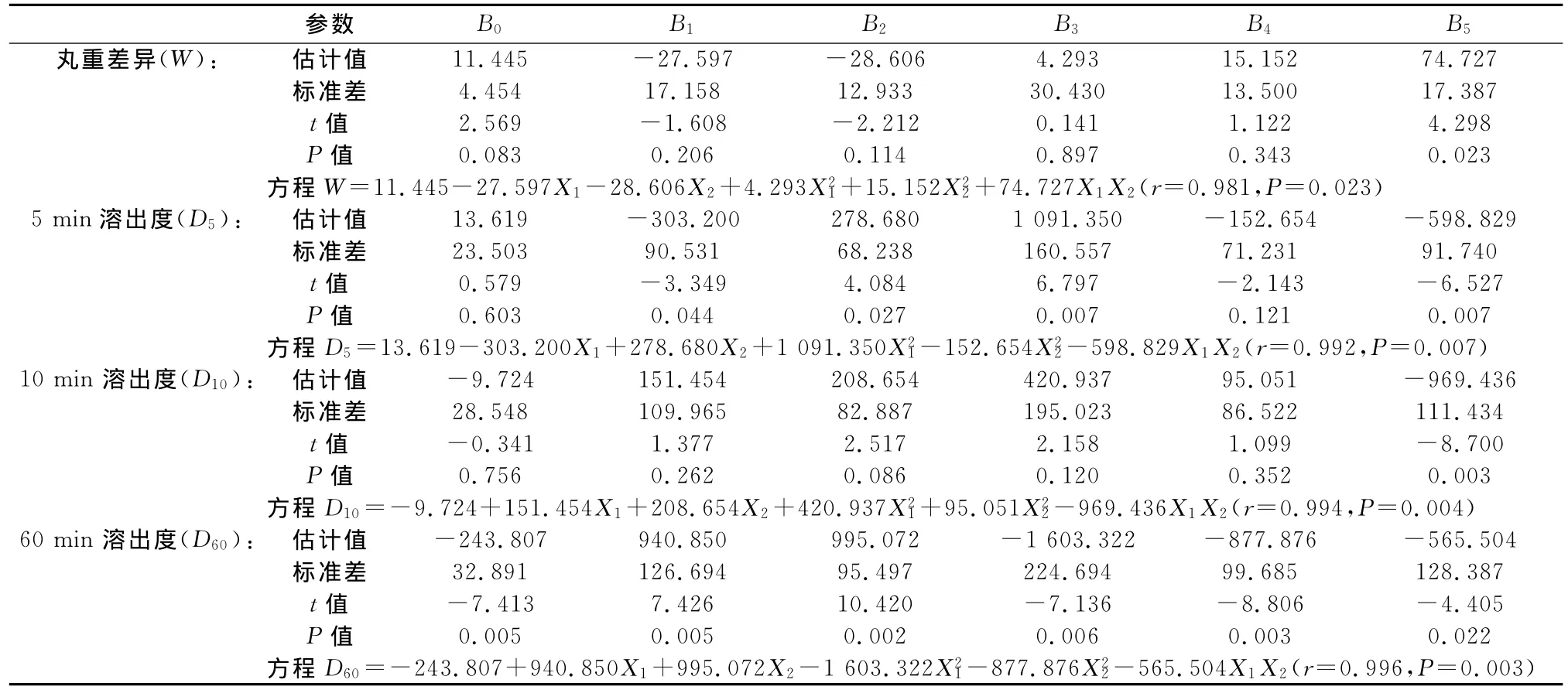
表3 丸重差异、5、10、60 min溶出度对主药和Poloxamer 188质量分数的二项式拟合结果Tab 3 Quadratic polynomial estimation results of weight variation of pills and the dissolution rate of 5,10,60 min to hemin and Poloxamer 188 content
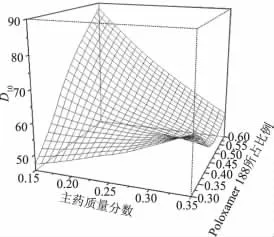
图3 D10对X1和X2的效应面Fig 3 Response surface of D10as a function of X1and X2

图4 D60对X1和X2的效应面Fig 4 Response surface of D60as a function of X1and X2

图5 W 对X1和X2的等高线Fig 5 Predicted contour plots of Was a function of X1and X3
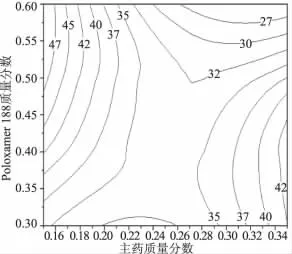
图6 D5对X1和X2的等高线Fig 6 Predicted contour plots of D5as a function of X1and X3

图7 D10对X1和X2的等高线Fig 7 Predicted contour plots of D10as a function of X1and X3

图8 D60对X1和X2的等高线Fig 7 Predicted contour plots of D60as a function of X1and X3
2.11.5 验证试验 根据优选的处方制备滴丸,考察其丸重差异及5,10,60 min的溶出度,进行3次平行试验,得实测值(observed value),与预测值(predicted value)进行比较,以偏差(bias)表示实测值偏离预测值的程度,其绝对值越小,表明预测性能越好。结果见表4。结果表明,各评价指标的预测值与实测值的偏差较小,本实验所建立的数学模型具有极好的预测性。
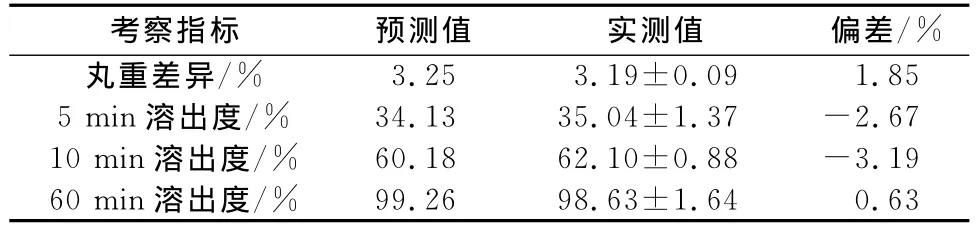
表4 预测值和实测值的偏差(n=3)Tab 4 Bias between predicted and observed values(n=3)
2.11.6 与其他剂型的比较 对氯化血红素滴丸和原药、分散片、胶囊的溶出度进行比较,结果见图9。
由图9可见,分散片、胶囊和滴丸溶出度较原药均有显著提高。其中胶囊内容物是由氯化血红素经β-环糊精包合而成,氯化血红素-β-环糊精包合物与原药相比溶出度有大幅提高;分散片则是药物与载体采用固体分散技术制成固体分散体后,经压片而得,与原药相比溶出度也有提高。滴丸在20 min时已经达到90%,30 min时药物几乎完全溶出,且相当于原药的20多倍。滴丸与胶囊、分散片相比较,能更快达到全部溶出的状态。结果表明,将氯化血红素制成滴丸后溶出度有了大幅提高,并符合《中国药典》的规定。

图9 氯化血红素滴丸、胶囊、分散片和原药的溶出曲线比较(±s,n=10)Fig 9 Comparison of dissolution curves of Hemin Dropping Pill,capsule,dispersible tablet and powder(±s,n=10)
3 讨论
在对实验结果进行拟合处理中,线性拟合结果的相关性差,不宜作为本实验的拟合数学模型;而非线性二次多项式拟合结果见表3,拟合相关系数均超过0.98,模型可信度高,通过验证实验也证实了所建模型具有极好的预测性,偏差均小于10%。
氯化血红素的水溶性差,将其制成滴丸后,主药及载体在滴丸中的质量分数对滴丸的处方条件筛选及药物的溶出影响很大。若滴丸中主药的质量分数过高,滴丸收集时易聚集,质量也不稳定,丸重差异也会增大,且滴丸溶出度也将下降,不利于速释制剂的迅速崩解和药物溶出;但也不能过低,否则要通过增加服药量以达到疗效,不符合药物的安全性原则。Poloxamer 188作为增溶剂虽能增加氯化血红素的溶解性和溶出速率,但若其质量分数过高,会使药液黏度增大,下滴时速度慢,产生拖尾,不利于滴丸成形;量也不可过低,否则增溶效果不明显。而PEG 6000虽能增加滴丸的机械强度,但其对于氯化血红素无抑晶作用,且不利于成形,氯化血红素在PEG 6000中的溶解度也较在Poloxamer 188中差,需加入较多助溶剂碱性无水乙醇。根据处方优化预测以及验证试验的结果,结合图1-8可知,当主药质量分数控制在23%,Poloxamer 188质量分数控制在45%时,丸重差异(W)为3.27%,在5,10,60 min时的溶出度分别为34.13%,60.18%,99.26%,均符合《中国药典》规定,且以Poloxamer 188和PEG6000作为固体分散体的混合载体为最佳。
十二烷基硫酸钠(SDS)是一种可以增加制剂亲水性的表面活性剂,对药物的释放度有明显的影响。氯化血红素较难溶解,易形成饱和溶液,无法满足漏槽条件,为此选择在溶出介质中加入适量SDS,使药物释放较完全。在900 mL磷酸盐缓冲液中加入0.5%SDS,30 mg的氯化血红素几乎完全溶解,而且冷却后基本不会析出结晶,故本实验选择0.5%SDS磷酸盐缓冲液为溶出介质,得到较好的实验结果。本文旨在优选氯化血红素滴丸的处方条件,须参照《中国药典》2010年版(二部)附录Ⅰ H丸剂和附录ⅩC第一法的规定进行试验。本实验结果表明氯化血红素制成滴丸后溶出度显著提高,CCD-RSM法可以很好地应用于其处方筛选优化,此法可广泛应用于药物制剂的新技术和新剂型的研究。
[1]袁曦,洪清.氯化血红素提取工艺及质量标准研究[J].中国药学杂志,1997,32(6):360-362.
[2]王君,陈红亮,张向东,等.氯化血红素提取新工艺的研究[J].当代化工,2001,30(3):125-127.
[3]黄毅,闫明,徐芳,等.微粉化工艺对羊血提取物中氯高铁血红素溶出度的影响[J].西北药学杂志,2005,20(5):212-214.
[4]中国药典.二部[S].2010:附录Ⅰ-ⅩC.
[5]陈伟,夏红,吴伟.星点设计-效应面法优化水飞蓟素滴丸的制备工艺[J].中草药,2005,36(5):679-683.
[6]吴伟,崔光华.星点设计-效应面优化法及其在药学中的应用[J].国外医学药学分册,2000,27(5):292-298.
