扁桃叶的化学成分研究
2012-12-22周荣光杨兆祥田立文张颖君
周荣光,杨兆祥,王 金,田立文,张颖君
1昆明制药集团药物研究院,昆明650100;2昆明理工大学生命科学与技术学院; 3中国科学院昆明植物研究所植物化学与西部植物资源持续利用国家重点实验室,昆明650204
扁桃(Mangifera persiciformis C.Y.Wu et T.L.Ming)系漆树科芒果属植物,主要分布在我国云南(东南部)、贵州(南部)和广西(南部)三省海拔300~600 m地区,多为野生[1]。扁桃叶为云南、广西民间习用药材,与同科同属植物芒果(M.indical L.)叶有类似的镇咳、平喘、祛痰等作用[2]。目前,国内外对扁桃化学成分的研究报道较少[3,4],为进一步深入开发扁桃叶这一丰富资源,作者对扁桃叶的化学成分进行了研究,从扁桃叶的乙醇提取物乙酸乙酯萃取部位中分离得到7个化合物,分别为没食子酸甲酯(1),没食子酸(2),3,4-二羟基苯甲酸(3),槲皮素(4),山奈酚-3-O-β-D-葡萄糖苷(5),槲皮素-3-O-β-D-葡萄糖苷(6)和芒果苷(7)。其中,化合物1、 3、5、6为首次从该植物中分离得到(图1)。
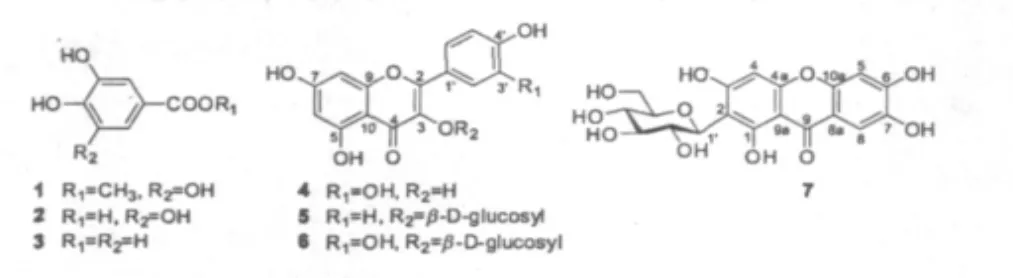
图1 化合物1~7的化学结构Fig.1 The chemical structures of compounds 1-7
1 仪器与材料
XRC-1显微熔点仪(温度计未校正),四川大学科学仪器厂;AB204-N型电子天平(瑞士Mettler公司);Shimadzu UV2401PC紫外可见分光光度仪(日本岛津公司);BRUKER TENSOR27傅立叶变换中红外光谱仪(德国布鲁克公司);BRUKER AM-400 MHz超导核磁共振仪(德国布鲁克公司);Autospec Premier P776双聚焦三扇型磁质谱仪(美国沃特斯公司)。
柱色谱用硅胶(200~300目)及TLC检测用硅胶板(GF254),青岛海洋化工厂。扁桃叶于2010年5月采自云南省景洪市,由昆明理工大学杨博教授鉴定为漆树科芒果属植物扁桃(Mangifera persiciformis C.Y.Wu et T.L.Ming)叶。
2 提取分离
取干燥的扁桃叶10 kg,粉碎至粗粉,用10倍量的95%乙醇室温浸渍过夜,滤过,收集滤液,滤渣再次用5倍量95%乙醇同法提取2次,合并滤液,减压浓缩得黑色粘膏状提取物485 g。热水混悬该提取物,依次用石油醚、乙酸乙酯、正丁醇萃取,经回收溶剂后得石油醚萃取物62 g,乙酸乙酯萃取物83 g,正丁醇萃取物115 g。将乙酸乙酯萃取物83 g进行硅胶(200~300目)柱层析,氯仿-甲醇(100∶0→0∶100)梯度洗脱,得6个组分Fr.1~Fr.6。Fr.2 (485 mg)再行硅胶柱色谱(200-300目),以石油醚-丙酮(20∶80→40∶60)梯度洗脱,经TLC检查后合并为3个亚组份A1~A3,亚组份A2(262 mg)用氯仿反复重结晶得化合物1(205 mg)。Fr.3(537 mg)再行硅胶柱色谱(200~300目),以氯仿-甲醇(70∶30→40∶60)梯度洗脱,经TLC检查后合并为4个亚组份B1~B4,亚组份B2(114 mg)再次上硅胶柱(200~300目),用氯仿-甲醇(1∶1)洗脱分离,得化合物2 (52 mg)和3(25 mg);亚组份B3(125 mg)用90%甲醇反复重结晶得化合物4(95 mg)。Fr.5(521 mg)再行硅胶柱色谱(200~300目),以氯仿-甲醇(1∶4)洗脱,甲醇重结晶得化合物5(32 mg)和6(350 mg)。Fr.6(1350 mg)用80%乙醇反复重结晶,得化合物7(950 mg)。
3 结构鉴定
化合物1 白色粉末;mp.198~200℃;EI-MS (pos.)m/z:184[M]+;1H NMR(DMSO-d6,400 MHz)δ:3.73(3H,s,OCH3),6.92(2H,s,H-2,H-6);13C NMR(DMSO-d6,100 MHz)δ:119.8(C-1),108.7(C-2,6),145.5(C-3,5),138.5(C-4),166.9(C=O),51.3(OCH3)。以上数据与文献[5]对照,鉴定为没食子酸甲酯。
化合物2 无色针状结晶(MeOH);mp.234~236℃;EI-MS(pos.)m/z:170[M]+;1H NMR(DMSO-d6,400 MHz)δ:6.91(2H,s,H-2,H-6),8.80 (1H,s,4-OH),9.14(2H,s,3-OH,5-OH),12.18 (1H,s,COOH);13C NMR(DMSO-d6,100 MHz)δ: 121.2(C-1),109.2(C-2,6),145.5(C-3,5),138.0(C-4),167.9(COOH)。以上数据与文献[6]对照,鉴定为没食子酸。
化合物3 白色粉末;mp.182~184℃;EI-MS (pos.)m/z:154[M]+;1H NMR(DMSO-d6,400 MHz)δ:7.32(1H,s,H-2),7.28(1H,d,J=8.5 Hz,H-5),6.65(1H,d,J=8.5 Hz,H-6);13C NMR (DMSO-d6,100 MHz)δ:121.9(C-1),118.2(C-2),145.1(C-3),150.6(C-4),115.4(C-5),121.1 (C-6),171.2(COOH)。以上数据与文献[5]对照,鉴定为3,4-二羟基苯甲酸。
化合物4 黄色针状晶体(MeOH);mp.308~310℃;UV(MeOH)λmax258,376 nm;IR(KBr) νmax3408,1667,1605,1542,1500,1465,1360,1266 cm-1;1H NMR(DMSO-d6,400 MHz)δ:6.19(1H,d,J=2.0 Hz,H-6),6.42(1H,d,J=2.0 Hz,H-8),7.66(1H,d,J=2.0 Hz,H-2'),6.91(1H,d,J=8.5 Hz,H-5'),7.54(1H,dd,J=8.5,2.0 Hz,H-6'),12.45(1H,s,5-OH),10.79(1H,s,7-OH),9.33 (3H,s,3-OH,3'-OH,4'-OH);13C NMR(DMSO-d6,100 MHz)δ:146.6(C-2),135.9(C-3),175.8(C-4),161.2(C-5),98.3(C-6),164.4(C-7),93.9 (C-8),156.8(C-9),103.9(C-10),122.5(C-1'),115.1(C-2'),145.2(C-3'),147.3(C-4'),115.0 (C-5'),120.5(C-6')。以上数据与文献[7]对照,鉴定为槲皮素。
化合物5 黄色针晶(MeOH);mp.166~168℃;1H NMR(DMSO-d6,400 MHz)δ:6.20(1H,d,J =2.0 Hz,H-6),6.44(1H,d,J=2.0 Hz,H-8),8.07 (2H,d,J=8.5 Hz,H-2',H-6'),6.91(2H,d,J= 8.5 Hz,H-3',H-5'),5.47(1H,d,J=7.5 Hz,glc H-1),3.05~3.62(6H,m,glc H-2,3,4,5,6a,6b);13C NMR(DMSO-d6,100 MHz)δ:156.4(C-2),133.4( C-3),177.5(C-4),161.3(C-5),98.6(C-6),164.5(C-7),93.6(C-8),156.3(C-9),104.1(C-10),120.9(C-1'),130.8(C-2',6'),115.1(C-3',5'),159.9(C-4'),100.9(C-1''),74.3(C-2''),76.7(C-3''),70.1(C-4''),77.5(C-5''),60.9(C-6'')。以上数据与文献[8]对照,鉴定为山奈酚-3-O-β-D-葡萄糖苷。
化合物6 黄色粉末;mp.224~226℃;1H NMR(DMSO-d6,400 MHz)δ:6.20(1H,d,J=2.5 Hz,H-6),6.41(1H,d,J=2.5 Hz,H-8),7.60(1H,d,J=2.5 Hz,H-2'),6.88(1H,d,J=8.5 Hz,H-5'),7.59(1H,dd,J=8.5,2.5 Hz,H-6'),5.48 (1H,d,J=7.2 Hz,glc H-1),3.05~3.62(6H,m,glc H-2,3,4,5,6a,6b);13C NMR(DMSO-d6,100 MHz)δ:156.2(C-2),133.6(C-3),177.8(C-4),161.2(C-5),98.8(C-6),164.7(C-7),93.8(C-8),156.6(C-9),103.9(C-10),121.5(C-1'),115.5(C-2'),145.1(C-3'),148.6(C-4'),115.9 (C-5'),121.2(C-6'),101.2(C-1''),74.5(C-2''),76.8(C-3''),70.2(C-4''),77.9(C-5''),61.2(C-6'')。以上数据与文献[9]对照,鉴定为槲皮素-3-O-β-D-葡萄糖苷。
化合物7 淡黄色针状晶体(MeOH);mp.271~272℃;UV(MeOH)λmax241,258,315,365 nm; IR(KBr)νmax3350,3180,1649,1620,1591,1565,1493 cm-1;1H NMR(DMSO-d6,400 MHz)δ:13.74 (1H,s,1-OH),10.37(3H,br s,3,6,7-OH),6.36 (1H,s,H-4),6.85(1H,s,H-5),7.38(1H,s,H-8),4.61(1H,d,J=8.7 Hz,glc H-1'),4.86(1H,m,glc H-2'),3.68(1H,m,glc H-3'),4.03(1H,t,J =8.9 Hz,glc H-4'),3.66(1H,m,glc H-5'),3.20 (1H,dd,J=10.3,2.3 Hz,glc H-6'a),3.10(1H,dd,J=10.2,7.0 Hz,H-6'b);13C NMR(DMSO-d6,100 MHz)δ:161.8(C-1),107.2(C-2),163.8(C-3),93.4(C-4),156.2(C-4a),102.5(C-5),154.0 (C-6),143.6(C-7),108.2(C-8),111.9(C-8a),179.1(C-9),101.5(C-9a),150.9(C-10a),70.7 (C-1'),73.4(C-2'),79.4(C-3'),70.2(C-4'),81.5(C-5'),61.4(C-6')。以上数据与文献[10]对照,鉴定为芒果苷。
1 Editorial Board of Flora of China,Chinese Academy of Sciences(中国科学院中国植物志编委会).Flora of China(中国植物志).Beijing:Science Press,1980.75.
2 Lin QY(林启云),Wang JR(王建如),Zhou F(周芳),et al.Pharmacology studies on the leaves of Mangifera persiciformis.Guangxi J Tradit Chin Med(广西中医药),1981,(5):37.
3 Si XL(思秀玲),Wei S(韦松),Xu XJ(许学健),et al.Studies on the chemical constituents from the leaves of Mangifera persiciformis.China J Chin Mater Med(中国中药杂志),1995,20:295-296.
4 Wei S(韦松),Yang XL(杨小良),Zhao WF(赵卫峰),et al.Study on the chemical constituents from the bark of Mangifera persiciformis.Chin Tradit Pat Med(中成药),2008,30:1399-1400.
5 Shang XY(尚小雅),Li S(李帅),Wang YH(王映红),et al.Chemical constitutents of Bauhinia aurea.China J Chin Mater Med(中国中药杂志),2006,31:1953-1955.
6 Deng AJ(邓安珺),Qin HL(秦海林).Studies on the chemical constituents of fruits of Bridelia tomentosa.China J Chin Mater Med(中国中药杂志),2008,33:158-160.
7 An Q(安琪),Yang CJ(杨春娟),Song Y(宋洋),et al.Studies on the chemical constituents of the fruit of Acanthopanax sessiliflorus(Rupr.et Maxim.)Seem..Nat Prod Res Dev(天然产物研究与开发),2008,20:765-769.
8 Li XY(李兴玉),Long CL(龙春林),Wang YH(王跃虎),et al.Chemical constituents of Oxyria digyna.Nat Prod Res Dev(天然产物研究与开发),2008,20:816-820,845.
9 Chen L(陈龙),Du LJ(杜力军),Ding Y(丁怡),et al.Studies on chemical constituents from flowers of Apocynum venetum.China J Chin Mater Med(中国中药杂志),2005,30:1340-1342.
10 Rancona S,Chaboud A,Darbour N,et al.A new C-glycosyl xanthone isolated from Dayallia solida.Phytochemistry,1999,52:1677-1679.
