长春西汀注射液的过敏性、溶血性和血管刺激性的实验研究
2012-12-01陈颖丽张殿文王清李伟
陈颖丽 张殿文 王清 李伟
长春西汀注射液为脑血管扩张药,能抑制磷酸二酯酶活性,增加血管平滑肌松弛的信使c-GMP的作用,选择性地增加脑血流量,此外还能抑制血小板凝集,降低人体血液粘度,增强红细胞变形力,改善血液流动性和微循环,促进脑组织摄取葡萄糖,增加脑耗氧量,改善脑代谢。临床上用于治疗由于大脑血液循环障碍而引起的精神性或神经性症状,改善脑梗死后遗症、脑出血后遗症、脑动脉硬化症等诱发的各种症状。本实验拟对长春富春制药有限公司生产的长春西汀注射液的溶血性、血管刺激性和过敏反应做出评价,为其临床用药的安全性提供科学依据。
1 材料
1.1 药物和试剂 长春西汀注射液,规格为2 ml/支,5 mg/ml,由长春富春制药有限公司提供,批号:20090801,每次临用前用生理盐水或5%葡萄糖溶液配制成适宜浓度备用。牛血清白蛋白,Genview产品,批号:9AD105106,购自北京鼎国生物技术有限责任公司。天花粉蛋白,由本院药理室提供。伊文思蓝,Flaka进口分装,上海化学试剂采购供应站分装厂。甲醛溶液,沈阳经济技术开发区试剂厂,批号:081006。水合氯醛,国药集团化学试剂有限公司,批号:T20080926。
1.2 动物 ①Wistar种大鼠,体重180~220 g,雌雄各半,合格证号:(J)2008-0005。②白色豚鼠,体重200~250 g,雄性,合格证号:(J)2008-0004。③家兔,体重2.5-3 kg,雌雄各半,合格证号:(J)2008-0004。均购自吉林大学实验动物中心。
2 方法与结果
2.1 溶血试验[1-3]取10 ml洁净试管21只,1~5号管为供试品管,6号管为阴性对照管,7号管为阳性对照管。按表1所示剂量依次加入2%兔红细胞混悬液、生理盐水或蒸馏水或供试品液体,各管轻轻摇匀后放入37℃恒温水浴箱中孵育,观察记录0.25、0.5、0.75、1、2、3、4 h 溶血反应结果。溶血评价标准为:全溶血为溶液澄明红色,管底无红细胞残留;部分溶血为溶液澄明红色或棕色,管底有少量红细胞残留;不溶血为红细胞全部下沉,上层液体无色澄明;凝聚为虽不溶血,但出现红细胞凝聚,振摇后不能分散。结果见表1。
由表1可见,长春西汀注射液0.3 mg/ml(5倍临床使用浓度)、溶媒及阴性对照管(生理盐水)在4 h内均未见澄明红色,且红细胞全部下沉,上层液体无色澄明,经振摇后红细胞能均匀分散,未见溶血和凝聚现象。而阳性对照管(蒸馏水)则产生明显的溶血反应。表明长春西汀注射液在0.3 mg/ml以下浓度无溶血及无红细胞凝聚作用。
2.2 全身主动过敏试验[1-3]实验开始前,动物预先饲养1周以观察其活动表现,取96只健康雄性白色豚鼠,随机分成六组,每组16只,第一组为生理盐水组,第二组为5%葡萄糖组,第三组为溶媒组,第四组为阳性对照组(牛血清白蛋白25 mg/kg),第五、六组分别为长春西汀(0.35 mg/ml或1.75 mg/ml)0.5 mg/kg、2.5 mg/kg。分别给各组豚鼠隔日腹腔注射一次,体积均为0.5 ml/只,共注射3次,使豚鼠致敏。然后将每组分成两批,于第1次致敏后14 d及21 d各组分别耳静脉注射生理盐水、溶媒、牛血清白蛋白50 mg/kg、长春西汀2 mg/kg、10 mg/kg,体积均为1 ml/只,进行激发过敏反应。观察豚鼠在静脉注射后30 min内有无表4中的躁动、抓鼻、竖毛、咳嗽、呼吸困难、痉挛、休克甚至死亡等过敏反应症状。并按全身主动过敏反应评价标准判定过敏反应级别。结果见表2。
由表2结果可见,生理盐水组、5%葡萄糖组、溶媒组、长春西汀注射液大、小剂量组,在静脉给药30 min内,豚鼠活动正常,未出现1~20级反应症状,判定为过敏反应阴性。而阳性对照组豚鼠出现躁动、抓鼻、竖毛、咳嗽、呼吸困难、痉挛、休克甚至死亡等现象,判定为过敏反应极强阳性。表明浓度为0.35 mg/ml或1.75 mg/ml的长春西汀注射液全身过敏反应试验合格。
2.3 被动皮肤过敏试验[1-3]实验开始前,动物预先饲养1周以观察其活动表现,取54只健康大鼠,雌雄各半,随机分为六组,每组9只,第一组为生理盐水组,第二组为5%葡萄糖组,第三组为溶媒组,第四组为阳性对照组(天花粉蛋白2 mg/ml)5 mg/kg,第五、六组分别为长春西汀(0.2 mg/ml和1 mg/ml)0.5 mg/kg、2.5 mg/kg。
2.3.1 大鼠含IsE的抗血清制备 从每组中各取1只大鼠,按注射剂大鼠同种被动皮肤过敏试验的要求,分别肌内注射上述剂量的生理盐水、5%葡萄糖、溶媒、天花粉蛋白和长春西汀大、小剂量,体积均为0.5 ml/只,隔日1次,共3次。末次致敏后第10天,以3%水合氯醛麻醉,腹主动脉取血,2000r/min离心10 min,分离血清,-20℃保存,备用。
2.3.2 大鼠同种被动皮肤过敏反应实验 取其余48只健康大鼠,每组8只,分别在各组大鼠背中线两侧距脊柱约1.5 cm处备皮4 mm×4 mm。取上述含IgE的不同抗血清,用生理盐水按1∶4和1∶8比例分别稀释成2个稀释度,将稀释的抗血清按左侧(1∶4比例)、右侧(1∶8比例)注射于大鼠背部预先备皮部位,每侧注射一个点,每点注射0.1 ml。于致敏48 h后,各组尾静脉注射与致敏剂量相同的激发抗原加等量的0.8%伊文思兰染料共1 ml,进行激发。30 min后处死各组大鼠,测量皮肤内层的蓝色反应斑直径,不规则斑点的直径为长径与短径之和,直径大于5 mm者判定为阳性,结果见表3。
由表3结果可见,生理盐水、5%葡萄糖组、溶媒、长春西汀大、小剂量组大鼠背部皮肤均未见蓝色反应斑点。阳性对照组注射部位皮肤均不同程度的出现蓝色斑点反应,且两侧(1∶4或1∶8稀释度)蓝斑直径均大于5 mm,判定为阳性反应。结果表明:长春西汀注射液无同种被动皮肤致敏作用。
2.4 血管刺激性试验[1-3]取健康日本大耳白家兔16只,雌雄各半,随机分成四组。按无菌操作方法于耳缘静脉滴注(10 ml/kg,1 ml/min)给药,第一组右耳滴注溶媒生理盐水溶液,左耳滴注生理盐水;第二组右耳滴注溶媒5%葡萄糖溶液,左耳滴注5%葡萄糖;第三组右耳滴注长春西汀生理盐水溶液0.3 mg/ml,左耳滴注溶媒生理盐水溶液;第四组右耳滴注长春西汀5%葡萄糖溶液0.3 mg/ml,左耳滴注溶媒5%葡萄糖溶液,体积均为10 ml/kg,1次/d,连续5 d,于每日给药前及末次给药后72 h,肉眼观察注射部位有无红肿、充血等刺激现象。处死动物,以耳缘静脉注射点至向心方向(避开注射部位)2 cm,连续取3段血管连同周围组织,每段1 cm,用10%甲醛溶液固定,做病理组织学检查,观察静脉血管组织有无炎症反应,甚至变性、坏死等显著性刺激反应。另一侧对照血管同法处理。
表4为血管刺激性试验的结果,各给药组4只家兔耳缘静脉注射部位均未见红肿、充血等刺激现象。病理组织学检查结果,生理盐水、5%葡萄糖左耳对照组,耳缘静脉血管内皮细胞排列正常,未见层次增多、排列紊乱的改变,血管腔内无附壁血栓,无炎细胞浸润。管壁内、中、外三层结构清晰,可见内弹力板,未见纤维组织增生。管壁无增厚、坏死及炎症等形态学改变,为正常组织结构;溶媒和长春西汀注射液右耳给药组血管组织结构正常,与左耳对照组血管比较无异常改变。
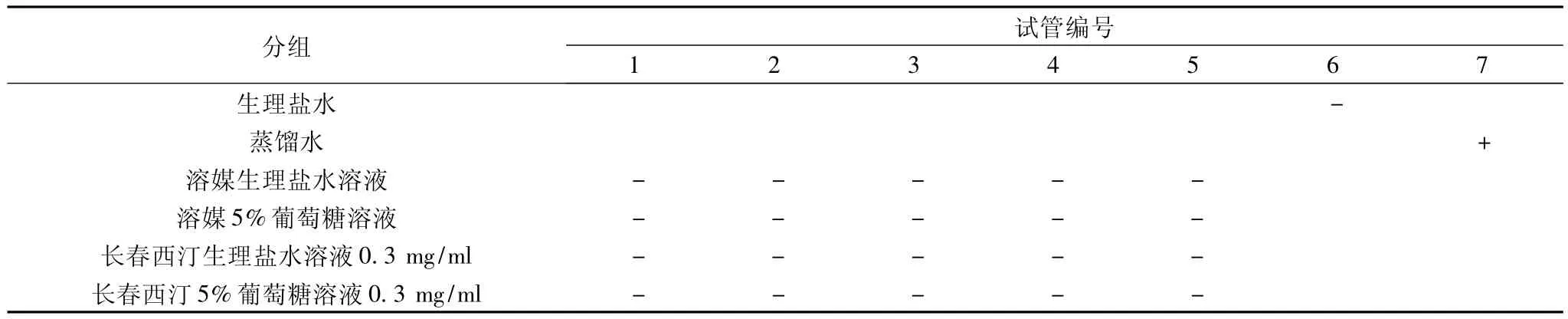
表1 长春西汀注射液溶血实验结果

表2 全身主动过敏反应实验结果
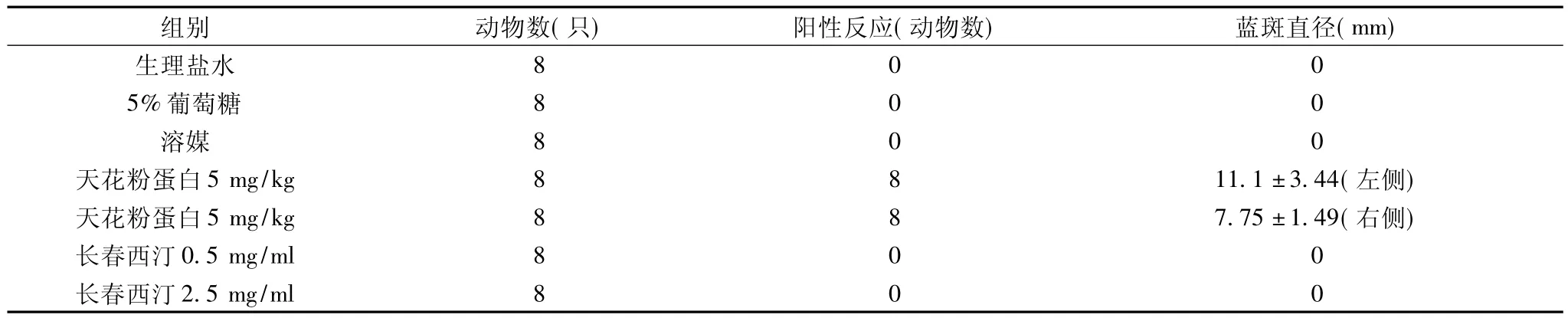
表3 被动皮肤过敏实验结果

表4 长春西汀注射液静脉滴注血管刺激性实验结果
3 小结
上述实验结果表明,长春西汀注射液在0.3 mg/ml浓度时,未见红细胞发生溶血和凝聚现象;多次静脉滴注0.3 mg/ml,注射部位血管无红肿、充血等刺激性现象,且血管病理组织学检查给药组与对照组血管组织结构基本相同,未见明显异常变化;给药组豚鼠活动正常,未见躁动、竖毛、咳嗽、呼吸困难、痉挛、休克甚至死亡等过敏反应症状,全身主动过敏反应阴性。给药组大鼠背部皮肤均未见蓝色斑点反应,即无同种被动皮肤致敏作用。
[1]化学药物刺激性、过敏性和溶血性研究技术指导原则课题研究组.化学药物刺激性、过敏性和溶血性研究技术指导原则,2005.
[2]梁新丽,等.注射用盐酸槐定碱对血管刺激性、溶血、过敏性试验研究.时珍国医国药,2007,8(18):1890.
[3]田日升,等.葛根素注射液的血管刺激性、溶血及过敏性实验研究.西北药学杂志,2009,4(24):278.
