两种头孢噻呋注射液在猪体内的比较药动学研究
2012-11-29陈启友廖雪玲赵永达方秋华黄显会
陈启友,廖雪玲,赵永达,杨 刚,方秋华,章 敏,黄显会
(1.湖南省兽药饲料监察所,长沙 410006;2.上海公谊兽药厂,上海奉贤 201401;3.华南农业大学兽医学院/国家残留基准实验室,广州 510642)
头孢噻呋是畜禽专用第3代头孢菌素,具有抗菌谱广、抗菌活性强的特点,对革兰氏阳性菌、阴性菌及一些厌氧菌都有很强的抗菌活性,目前已被美国、日本和欧洲一些国家正式批准用于肉牛、奶牛、马、猪、羊、鸡等细菌性疾病,如猪细菌性呼吸道感染和鸡的大肠杆菌、沙门氏菌的感染等方面的治疗,显示了广阔的应用前景[1-2]。
近几年,新型兽药的应用极大地促进了养殖业的发展,产生了巨大的经济效益和社会效益。头孢噻呋因其显著的疗效,被诸多企业开发。本文进行了两种头孢噻呋注射液在猪体内的比较药动学研究,为兽医临床用药提供理论依据。
1 材料与方法
1.1 试验动物 12头健康的杜洛克×长白×约克夏杂交猪,公母各半,体重(26.39 ±2.83)kg,购自广东省原种猪场。按常规饲养,自由饮水和采食,饲料为全价日粮,不含任何抗菌药物。临床观察两周表现健康。试验前16 h起及给药后4 h期间禁食,仅自由饮水。
1.2 药品与试剂 供试药品:长效盐酸头孢噻呋注射液,含量10%(100 mL:10 g),批号100720,由上海公谊兽药厂提供。对照药品:盐酸头孢噻呋注射液(速解灵注射液),含头孢噻呋5%(100 mL:5 g),批号:0A4SM,美国辉瑞(动物保健品)有限公司生产。头孢噻呋对照品:含量87.5%,批号:K0330406,中国兽医药品监察所。二硫赤藓糖醇(DTE):批号BM0462-2,SIGMA公司。碘乙酰胺(Iodoacetamide):批号 I6125,SIGMA公司。乙腈:色谱纯,德国CNW公司。水:符合GB/T6682规定的二级水。其他试剂均为国产分析纯。
1.3 仪器设备 美国Waters公司超高效液相色谱仪(配紫外检测器、四元泵、脱气泵、自动进样器、柱温箱等);电子分析天平:FA2004N型,上海精密科学仪器有限公司。旋涡混合仪:XW-80A型,上海青浦泸西仪器厂。高速离心机:美国Thermo公司。轨道式摇床:KS501digital型,德国IKA公司;MCX小柱:MCX BondElut Varian 1CC 100MG,批号171069,德国CNW公司。
1.4 给药与血样采集 12头猪随机分为两组,每组6头,分别进行肌注长效盐酸头孢噻呋注射液(上海公谊)和肌注速解灵注射液(美国辉瑞),给药剂量均为5 mg/kg。猪只仰卧保定,分别于颈部肌肉注射,给药前采一次空白血。肌肉(颈部)注射给药后分别于 5、10、15、30 min 及 1、2、3、4、6、8、12、16、24、36、48、60、72、96、120、144、168、192 h 采集血样,每次约5 mL,置于含肝素的离心管中,4000 r/min离心10 min,分离血浆,-20℃冰箱保存,待测。
1.5 血浆样品预处理 血浆样品自然解冻,摇匀。准确量取血浆1.0 mL于15 mL离心管中,加入2.5 mL DTE工作液,漩涡混合1 min,50℃水浴振荡20 min;放置室温下降温;加入1 mL碘乙酰胺工作液,旋涡10 s,用锡纸包好置于恒温震荡培养箱中30℃200 r/min培育30 min;加200 μL 20%的磷酸酸化后,加2.5 mL水混合均匀;7000 g离心20 min;取上清液备用。
往MCX小柱中依次加入3 mL色谱甲醇,3 mL水活化净化小柱,弃去流出液;加入上述上清液,弃去流出液;再依次加入3 mL水,3 mL甲醇淋洗,真空抽干4 min;加入1 mL 1 mol/L醋酸胺:乙腈(85+15,V/V)混合液洗脱;将洗脱液用 0.22 μm微孔滤膜滤过,上UPLC仪测定。
1.6 色谱条件 色谱柱:Waters ACQUITY BEH RP18(2.1 mm ×50 mm,1.7 μm),柱温:25 ℃,紫外检测器,检测波长:265 nm,流速:0.5 mL/min,进样量:10 μL,流动相:0.2%三氟乙酸(A)+乙腈(B),梯度洗脱,见表1。
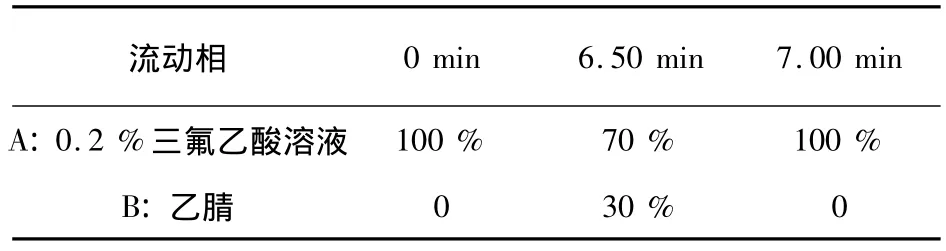
表1 流动相梯度洗脱条件
1.7 数据处理与统计分析 采用美国Pharsight公司药动学软件 Winnonlin5.2.1的非房室模型来处理药动数据,计算出每头试验猪的药动学参数,然后计算平均值()及标准差(s),同时以血药浓度平均值对时间作药-时曲线图。所得药动学参数,采用SPSS 16.0进行t检验,显著性水平为0.05。
2 结果
2.1 色谱条件适用性 在本试验建立的色谱条件下,基线平稳,头孢噻呋衍生物去呋喃羰基头孢噻呋乙酰胺(DCA)与血浆中组分分离良好,DCA的色谱峰保留时间分别为3.29 min左右。本方法可获得较好的峰形,保留时间稳定(图1)。
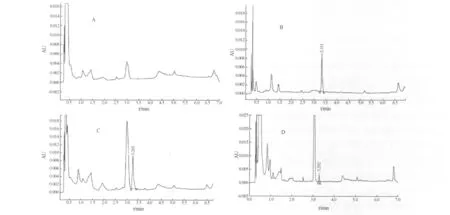
图1 头孢噻呋衍生化UPLC色谱图
2.2 标准曲线和检测限 经UPLC测定,以峰面积(A)对药物浓度(C)回归,得回归方程 A=25247C+269.12,r=0.9992。头孢噻呋衍生物去呋喃羰基头孢噻呋乙酰胺与头孢噻呋添加量之间在0.05~20 μg/mL范围内线性关系良好。检测限数据满足药动学研究要求。在上述条件下,头孢噻呋的检测限为0.02 μg/mL。血浆中头孢噻呋的平均回收率76.63% ~93.61%,本方法批内变异系数为1.46% ~7.37%,批间变异系数为6.16% ~8.05%。
2.3 回收率测定 头孢噻呋在添加浓度0.1、1、10 μg/mL的平均回收率分别为(92.37±4.30)%、(76.63% ±4.94)%、(93.61% ±7.54)%(n=5),方法回收率高,符合生物样品测定要求。
2.4 精密度测定 0.1、1、10 μg/mL 头孢噻呋药物浓度的日内RSD均小于8%,日间RSD均小于9%(表2),符合精密度要求,测定方法可靠。
2.5 血浆中的药物浓度和主要动力学参数 肌肉注射头孢噻呋注射液和速解灵注射液后,血药浓度-时间曲线图见图2。
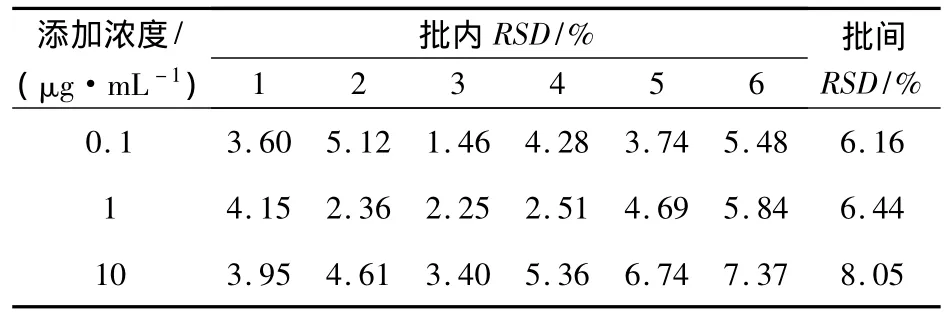
表2 头孢噻呋在猪血浆中UPLC色谱分析的变异系数(n=6)
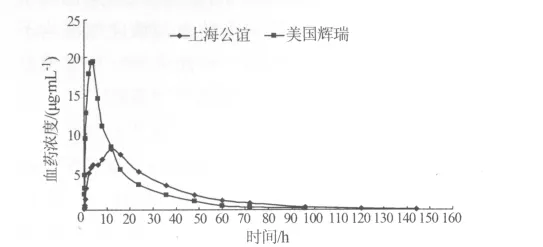
图2 两种盐酸头孢噻呋注射液猪单剂量(5 mg/kg)肌注后血浆药-时曲线
猪单剂量肌注头孢噻呋注射液和肌注速解灵注射液的药时数据最佳模型为非房室模型,头孢噻呋注射液和肌注速解灵注射液后药动学参数见表3。
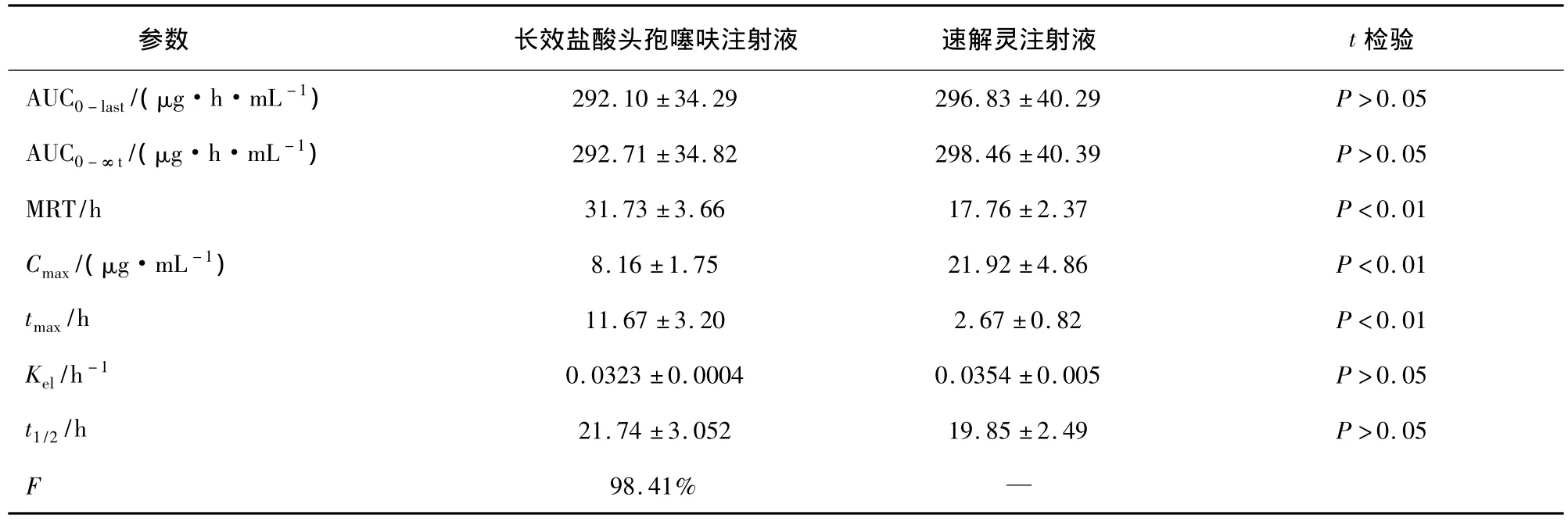
表3 两种头孢噻呋注射液主要药动学参数比较
通过表3中的各项平均药动学参数可以看到,健康猪肌注长效盐酸头孢噻呋注射液5 mg/kg后,吸收较慢,注射给药后11.67 h,血药浓度达峰值,Cmax为8.16 μg/mL。血浆中平均消除半衰期(t1/2)为20.05 h;AUC 为 292(μg·h)/mL,平均滞留时间(MRT)为31.7 h;肌注速解灵注射液5 mg/kg后,吸收迅速,肌肉注射给药后2.67 h,血药浓度达峰值,Cmax为21.92 μg/mL,t1/2为 18.31 h;AUC 为 296.83(μg·h)/mL,MRT 为17.76 h。
3 讨论与结论
3.1 最佳房室模型的选择 根据国外已有报道,头孢噻呋的药动学数据大都采用非房室模型分析[3-17]。采用 3P97药物动力学参数计算程序,Marquardt法对一、二、三房室分别以权重1、1/C、1/C2等3种情况进行计算,AIC值愈小,则认为该模型拟合愈好[18]。在微机电脑上处理实测血浆头孢噻呋血药浓度-时间数据,结果显示,头孢噻呋注射液和肌注速解灵注射液的血药浓度数据均不能拟合出合适的生理模型。因此采用非房室模型的分析方法,计算出有关药物动力学参数。
3.2 肌注长效盐酸头孢噻呋注射液药动学特征经肌肉注射给药结果表明,健康猪肌注长效盐酸头孢噻呋注射液5 mg/kg后,吸收较慢,给药后11.67 h,血药浓度达峰值,与 Brown 等[4]的研究结果(tmax=0.33 h)相比,达峰时间显著延长;但达峰浓度远低于Brown的研究结果(28.3 μg/mL)。与胡振英等[19]的研究结果相比,本试验研究表明长效头孢噻呋注射液具有较长的半衰期,较胡振英研究结果(14.64 h)长7 h。长效头孢噻呋注射液的药动学参数与文献报道相似[20]。长效头孢噻呋注射液的相对生物利用度为98.41%,说明国产长效头孢噻呋注射液与进口产品生物利用度相当。本试验结果表明上海公谊兽药厂研制的长效头孢噻呋注射液峰浓度有所降低,但达峰时间和半衰期均延长,表明具有缓释作用,能更好的起到动物疾病的防治效果。
3.3 肌注速解灵注射液的药动学特征 通过对长效盐酸头孢噻呋注射液和速解灵注射液(辉瑞)药动学研究,药动参数经 t检验,MRT、Cmax、tmax存在极显著性差异(P<0.01),表明健康猪肌注长效盐酸头孢噻呋注射液(5 mg/kg)与肌注速解灵注射液相比,长效盐酸头孢噻呋注射液单剂量肌注给药吸收较慢,达峰时间显著延迟,达峰浓度显著降低,平均驻留时间显著延长,参数AUC、Kel、t1/2统计无显著性差异(P>0.05),长效盐酸头孢噻呋注射液与肌注速解灵注射液的生物利用度相当。
3.4 长效头孢噻呋注射液临床给药方案的建议健康猪肌注长效盐酸头孢噻呋注射液5 mg/kg后,在 72 h 平均血药浓度达 0.88 μg/mL,120 h 达0.2 μg/mL,144 h仍可检测到药物。肌注速解灵注射液5 mg/kg后,在72 h 平均血药浓度为0.36 μg/mL,120 h血药浓度已经低于定量限,144 h检测不到药物。结果表明,健康猪肌注长效盐酸头孢噻呋注射液(5 mg/kg)有效血药浓度维持时间更长,对临床敏感菌感染,可用长效盐酸头孢噻呋注射液肌内注射,每kg体重5 mg,每2 d给药1次,连续给药2次。
本研究进行了国产头孢噻呋注射液与进口头孢噻呋注射液的比较药动学研究,通过研究发现,国产药物与进口药物生物利用度相似。
[1] 党晓林,祁长川,刘红艳,等.复方盐酸头孢噻呋混悬剂的药代动力学研究[J].中国兽药杂志,2012,46(2):10 -15.
[2] 李长流,俞道进,马玉芳,等.猪血浆中去呋喃甲酰基头孢噻呋浓度的HPLC测定[J].福建农林大学学报(自然科学版),2010,1(39):58 -62.
[3] Barere S D,Pille F,Croubels,et al.High - performance liquid chromatographic-UV detection analysis of ceftiofur and its active metabolite desfuroylceftiofur in horse plasma and synovial fluid after regional intravenous perfusion and systemic intravenous injection of ceftiofur sodium[J].Analytica Chimica Acta,2004,1(512):75-84.
[4] Brown S A,Hanson B J,Mignot A,et al.Comparison of plasma pharmacokinetics and bioavailability ofceftiofursodium and ceftiofur hydrochloride in pigs after a single intramuscular injection[J].Journal of Veterinary Pharmacology and Therapeutics,1999,1(22):35-40.
[5] Berendsen B J,Stolker L A,Nielen M W.Assessment of liquid chromatography-tandem mass spectrometry approaches for the analysis of ceftiofur metabolites in poultry muscle[J].Food Addit Contam Part A Chem Anal Control Expo Risk Assess,2012,29(2):197-207.
[6] Caraigmill A L,Brown S A,Wetzlich S E,et al.Pharmacokinetics of ceftiofur and metabolites after single intravenous an intramuscular administration and multiple intramuscular adm intration of ceftiofur sodium to sheep[J].Journal of Veterinary Pharmacology and Therapeutics,1992,1(6):431 -438.
[7] Cervantes C C,Brown M P,Gronwall R R,et al.Pharmacokinetics concentration of ceftiofur sodium in body fluids and endometrium after repeated intramuscular inmares[J].Am J Vet Res,1993,54(4):573-575.
[8] Collard W T,Cox S R,Lesman S P,et al.Pharmacokinetics of ceftiofur crystalline-free acid sterile suspension in the equine[J].Journal of Veterinary Pharmacology and Therapeutics,2011,34(5):476-481.
[9] Courtin F,Graigmill A,Wetzlich S E,et al.pharmacokinetics of ceftiofur and metabolites after single intravenous and intramuscular administration and mutiple intramuscular admintration of ceftiofur sodium to dairy goats[J].Journal of Veterinary Pharmacology and Therapeutics,1997,20(5):368 -373.
[10] Doré E,Angelos J A,Rowe J D,et al.Pharmacokinetics of ceftiofur crystalline free acid after single subcutaneous administration in lactating and nonlactating domestic goats(Capra aegagrus hircus)[J].Journal of Veterinary Pharmacology and Therapeutics,2011,34(1):25 -30.
[11] Dumonceaux G,Isaza R,Koch D E,et al.Pharmacokinetics and im bioavailability ofceftiofurin Asian elephants(Elephas maximus)[J].Journal of Veterinary Pharmacology and Therapeutics,2005,28(3):441 -446.
[12] Hall,T L,L A Tell,et al.Pharmacokinetics of ceftiofur sodium and ceftiofur crystalline free acid in neonatal foals[J].Journal of Veterinary Pharmacology and Therapeutics,2011,34(4):403 -409.
[13] Liu S,Guo D,Guo Y,et al.Preparation and pharmacokinetics of ceftiofur sodium liposomes in cows[J].Journal of Veterinary Pharmacology and Therapeutics,2011,34(1):35 -41.
[14] Meyer J C,Brown M B,Gronwall R R,et al.pharmacokinetics of ceftiofur sodium in neonatal foals after intramuscular injection[J].Equine Veterinary Journal,1992,24(6):485 - 486.
[15] Meyer S,Giguère S,Rodriguez R,et al.Pharmacokinetics of intravenous ceftiofur sodium and concentration in body fluids of foals[J].Journal of Veterinary Pharmacology and Therapeutics,2009,32(4):309-316.
[16] Soback S,Ziv G,Winkler M,et al.Pharmacokinetics of ceftiofur administered intravenously and intramuscularly to lactating cows[J].Israeli Joumal of Rat Ned,1989,1(4):118 -123
[17] Tantituvanont A,Yimprasert W,Werawatganone P,et al.Pharmacokinetics of ceftiofur hydrochloride in pigs infected with porcine reproductive and respiratory syndrome virus[J].Journal of Antimicrobial Chemotherapy,2009,63(2):369 -373.
[18]魏树礼,张 强.生物药剂学与药物动力学[M].北京:北京大学医学出版社,2004:16.
[19]胡振英,张新国,罗永江,等.头孢噻呋钠在猪体内的药代动力学和生物利用度研究[J].中兽医医药杂志,2003,05:14-17.
[20] Wojick K B,Langan J N,Adkesson M J,et al.Pharmacokinetics of long-acting ceftiofur crystalline-free acid in helmeted guineafowl(Numida meleagris)after a single intramuscular injection[J].American Journal of Veterinary Research,2011,72(11):1514-1518.
