鸭瘟活疫苗外源病毒检验方法(鸡检查法)的修订
2012-11-29李启红李俊平杨承槐黄建华蒋桃珍李慧姣
李启红,李俊平,杨承槐,黄建华,蒋桃珍,李慧姣
(中国兽医药品监察所,北京 100081)
为了保证疫苗纯净、安全、有效,活疫苗应进行外源病毒检验。《中华人民共和国兽药典》(简称《兽药典》)二〇〇五年版中规定的禽源制品外源病毒检验方法有鸡胚检查法、细胞检查法和鸡检查法。通常情况下,采用鸡胚检查法和细胞检查法进行,如果检验无结果或结果可疑时,用鸡检查法进行检验[1]。鸡胚检查法和细胞检查法均采用高效价的抗血清中和本病毒后接种鸡胚、细胞,观察是否有外源病毒引起的病变。采用鸡检查法进行外源病毒检验时不需要中和疫苗病毒,但需要接种疫苗的剂量大,即每只鸡需接种2次,每次经滴鼻、点眼和肌肉注射共接种120羽份。
目前,国内使用的鸭瘟活疫苗系用鸡胚化的鸭瘟病毒接种SPF鸡胚或鸡胚成纤维细胞,收获感染的鸡胚液、胎儿及绒毛尿囊膜并混合研磨或收获病毒培养液,加适宜稳定剂,经冷冻真空干燥制成。在实际检验工作中,因抗鸭瘟病毒血清中和效价不高,不能中和《兽药典》规定的羽份数,所以无法通过鸡胚检查法和细胞检查法进行外源病毒检验。选用鸡检查法对鸭瘟活疫苗进行外源病毒检验时,按《兽药典》使用1、4月龄的SPF鸡接种疫苗后,大部分鸡在1周内死亡,无法继续检验。所以,有必要对目前鸭瘟活疫苗的外源病毒检验的鸡检查法进一步修订,以便更好地控制疫苗质量。本实验室对实验用SPF鸡的周龄和基础免疫程序进行了研究。
1 材料与方法
1.1 实验动物 SPF鸡,购自北京梅里亚维通实验动物中心。
1.2 鸭瘟种毒 从中国兽医药品监察所菌种保藏中心领取种毒,经SPF鸡胚繁殖,制备的湿毒病毒含量为 107.4ELD50/0.2 mL。
1.3 鸭瘟活疫苗 来自3个企业5批次。
1.4 抗体检测ELISA试剂盒 鸡传染性支气管炎病毒(IBV)、传染性法氏囊病病毒(IBDV)、禽呼肠孤病毒(REOV)、鸡网状内皮增生症病毒(REV)、J亚型禽白血病病毒(ALV-J)、禽脑脊髓炎病毒(AEV)抗体检测试剂盒,均购自IDEXX公司。
1.5 血凝(HA)抗原 新城疫病毒(NDV)、减蛋综合征病毒(EDS)HA抗原,由中国兽医药品监察所制备供应;H5亚型和H9亚型禽流感病毒(AIV)HA抗原,由国家禽流感参考实验室制备供应。
1.6 方法
1.6.1 建立检验方法 SPF鸡只周龄、基础免疫的时间和接种剂量的试验方案见表1。购进4周龄SPF鸡后,隔离器分组饲养,饲养至4、7、9周龄后进行试验。先用小剂量的鸭瘟种毒进行基础免疫,14 d后再按照《兽药典》(二〇〇五年版)附录20页“鸡检查法”进行免疫及抗体检测。
1.6.2 验证检验方法 按照1.6.1建立的方法,选取5批疫苗样品进行外源病毒检验,对所建立方法进行验证。
2 结果
2.1 检验方法的建立 结果见表1。选用4周龄SPF鸡进行鸭瘟活疫苗的外源病毒检验时,首次接种 103.0、104.0、105.0ELD50的鸭瘟种毒均引起免疫鸡100%发病,50%以上死亡。7周龄 SPF鸡接种103.0ELD50以上的鸭瘟病毒引起25%以上发病,20% 以上死亡。9 周龄 SPF 鸡免疫 102.0、103.0的鸭瘟种毒均未引起临床症状和死亡。
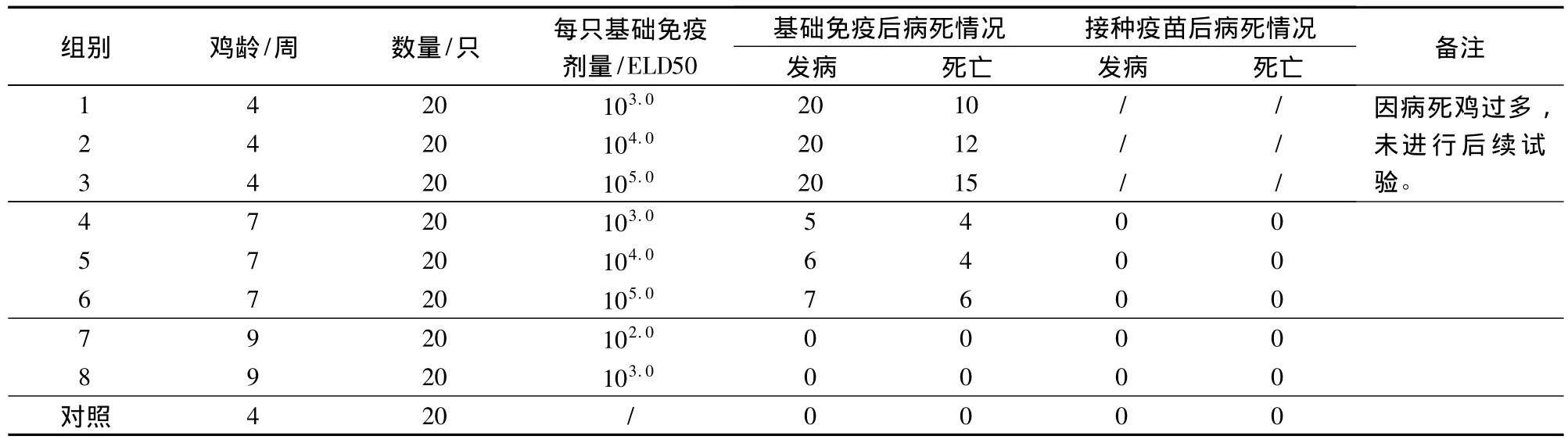
表1 建立检验方法的试验方案及各组发病和死亡情况
2.2 检验方法的验证 结果见表2。9、10周龄SPF鸡免疫103.0ELD50的鸭瘟种毒均未引起鸡只特异性发病和死亡,基础免疫后14 d按《兽药典》(二〇〇五年版)附录20页“鸡检查法”规定的剂量和程序鸭瘟活疫苗,均未出现因疫苗引起的异常临床症状和特异性死亡。

表2 验证检验方法的试验方案及各组鸡发病死亡情况
2.3 抗体检测结果 见表3。选取建立方法试验的第6组(免疫剂量最大)、检验方法验证试验的5批疫苗及对照组鸡的血清样品,按《兽药典》(二〇〇五年版)检测11种(亚型)病原抗体,结果C和E 2批次疫苗中污染REV(抗体阳性率为47%和60%,S/P 比值为0.60 ~8.1 和0.69 ~7.48),说明目前我国鸭瘟活疫苗中有污染外源病毒的现象。
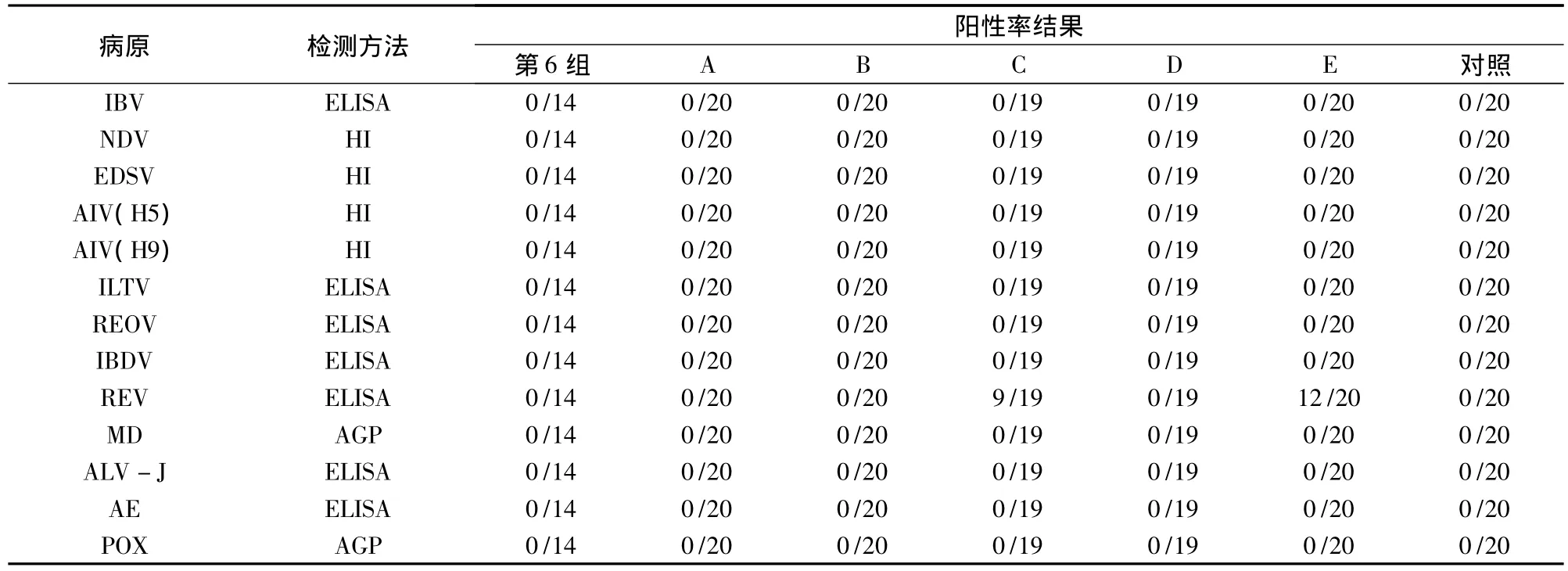
表3 抗体检测结果
3 讨论
目前国内使用的鸭瘟活疫苗种毒为1957年分离自发病鸭的强毒株[2],经鸡胚连续传代60多代后获得,对鸭失去致病性,但保留了良好的免疫原性[3]。鸡非鸭瘟病毒的自然易感宿主[4],但经鸡胚连续传代的鸭瘟病毒可在鸡胚上增殖,其可以获得高滴度的病毒,同时也可增强对鸡的致病性。早在1981年,黄如意等研究人员就报道了鸭瘟活疫苗能致雏鸡发病、死亡[5]。
外源病毒检验是兽用活疫苗质量标准中的关键项之一,有效控制外源病毒污染关系到疫苗使用的安全性和有效性,直接影响疫病防控效果和养殖业的健康发展,以及动物源性食品安全。有关外源病毒检验,《欧洲药典》[6]、美国的《联邦法规》(9CFR)[7]均有严格的规定和原则要求,我国《兽药典》有关规定和要求与欧美相似,外源病毒检验方法参考国外的方法建立,并逐步完善。
我国是养鸭大国,鸭的养殖量占全球的60%以上,用于预防鸭病的生物制品品种相对较多,用量大。国外鸭的养殖量少,用于预防鸭病的活疫苗品种也少,鲜见鸭用活疫苗外源病毒检验的具体方法。鸭瘟活疫苗外源病毒检验按照我国原有《兽药典》的有关规定无法进行,参照《欧洲药典》有关水禽活疫苗种毒外源病毒鸡检查法的原则,研究建立用鸡检查法对鸭瘟活疫苗进行外源病毒检验的切实可行的方法。
本研究证实,9周龄以下的 SPF鸡接种103.0ELD50的鸭瘟活疫苗可引起严重的发病和死亡,发病及死亡率随着接种剂量增加有升高的趋势,随着接种鸡日龄的提大,发病率和死亡率明显下降,9周龄和10周龄SPF鸡免疫103.0ELD50的鸭瘟活疫苗病毒后均无临床症状和特意死亡。根据试验结果,为保证外源病毒检验时免疫鸡不发病,选择9~12周龄的SPF鸡用于检验。在按药典规定剂量免疫前,先用低剂量鸭瘟病毒进行基础免疫,从而建立了鸭瘟活疫苗的外源病毒检验的鸡检查法,该方法已被《兽药典》(二〇一〇年版)[8]收录。
应用建立的检验方法,对3个企业5批次的鸭瘟活疫苗进行了外源病毒检验,同时选取建立方法试验时的第6组(免疫剂量最大)进行抗体检测。结果表明,用于基础免疫的鸭瘟种毒无外源病毒污染,2批次疫苗中污染了REV,说明目前我国鸭瘟活疫苗中有污染外源病毒的现象,有必要加强对鸭瘟活疫苗的监督检验。
致谢 感谢中国兽药典委员会对本研究的资助。感谢瑞普(保定)生物药业有限公司在动物实验过程中给予的大力帮助。
[1] 中国兽药典委员会.中华人民共和国兽药典二○○五年版三部[S].
[2] 黄引贤.拟鴨瘟的研究[J].华南农学院学报,1959,1:67 -78.
[3] 农业部第四届兽用生物制品规程委员会.中华人民共和国兽用生物制品规程2000年版[S].
[4] Saif Y M.Disease of Poultry[S].12thEdition.USA:Blackwell Publshing,2008.
[5] 黄如意,肖俊发,陈荷凤,等.鸭瘟弱毒疫苗对鸡致死研究初报[J].上海农业科技,1981,2:37,34.
[6] Council of Europe.European Pharmacopoeia[S].6thEdition.Section 2.6.24;Revised 2008.
[7] Office of the Federal Register National Archives and Records Administration.Code of Federal Regulations(9 Animal and Animal Products)[S].USA:US Government Pringting Officeh,2007.
[8] 中国兽药典委员会.中华人民共和国兽药典二○一○年版三部[S].
