超高效液相色谱法测定头孢噻呋晶体注射液中头孢噻呋含量
2020-11-03魏秀丽王艳芬杨志昆冯言言张传津徐恩民李有志
魏秀丽,常 雪,王艳芬,杨志昆,冯言言,张传津*,徐恩民*,李有志
(1.山东省兽药质量检验所,山东省畜产品质量安全监测与风险评估重点实验室,动物源细菌耐药性监测与精准化用药山东省工程实验室,济南250022;2.齐鲁动物保健品有限公司,济南250100)
头孢噻呋晶体注射液是一种缓释制剂,活性成分是头孢噻呋,用于治疗和预防溶血性巴氏杆菌、多杀性巴氏杆菌和睡眠嗜血杆菌感染引起的牛呼吸系统疾病(肺炎,运输热),以及治疗胸膜肺炎放线杆菌、多杀性巴氏杆菌、副猪嗜血杆菌和猪链球菌引起的猪呼吸系统疾病[1-2]。在中华人民共和国农业农村部公告第11号等文献中头孢噻呋晶体及其注射液或其他相关制剂对头孢噻呋含量测定均采用高效液相色谱方法[3-8],检测所用流动相配制比较复杂,有机试剂品种较多,对实验室人员操作性要求较高。本实验开发了超高效液相色谱-光电二极管阵列检测法(UPLC-PDA)测定头孢噻呋晶体注射液中头孢噻呋的含量,与高效液相色谱法相比建立的方法流动相组成简单,配制容易,毒性相对较小,简单快速,经济环保。
1 材料与方法
1.1 药品及试剂 头孢噻呋对照品,批号K0331711,含量89.5%,中国兽医药品监察所;乙腈、冰醋酸、甲醇、四氢呋喃等均为色谱纯;醋酸铵、正丁醇、二甲基甲酰胺、正己烷、氢氧化四丁基铵等为分析纯;超纯水。
头孢噻呋晶体注射液(猪用),来自齐鲁动物保健品有限公司产品,规格,50 mL:5 g,100 mL:10 g;头孢噻呋晶体注射液(牛用),来自齐鲁动物保健品有限公司产品,规格,50 mL:10 g,100 mL:20 g。
1.2 仪器 Waters AcquityTMUltra performance LC超高效液相色谱仪,配备二极管阵列检测器,美国waters 公司;Agilent 1260高效液相色谱仪,配备紫外检测器,美国安捷伦公司。分析天平,感量0.00001 g,瑞士梅特勒公司。
1.3 方法
1.3.1 供试品溶液制备 严格按照农业农村部公告第11号头孢噻呋晶体注射液质量标准。
1.3.2 标准储备液的制备 精密称取头孢噻呋对照品44.7 mg,按照农业农村部公告第11号头孢噻呋晶体注射液质量标准配制成400 μg/mL储备液。
1.3.3 标准工作液的制备 取储备液适量,配制成标准工作液:每1 mL含头孢噻呋200、80、40、20、8、4、2 μg的溶液。
1.3.4 色谱操作条件及参数 色谱柱:C8色谱柱(2.1 mm×100 mm,1.7 μm);以乙腈为流动相A,0.1%甲酸为流动相B,按表1规定进行梯度洗脱;光电二极管阵列检测器,扫描范围190~400 nm,检测波长为292 nm,柱温35 ℃,进样室温度10 ℃,流速0.35 mL/min,进样量1 μL。
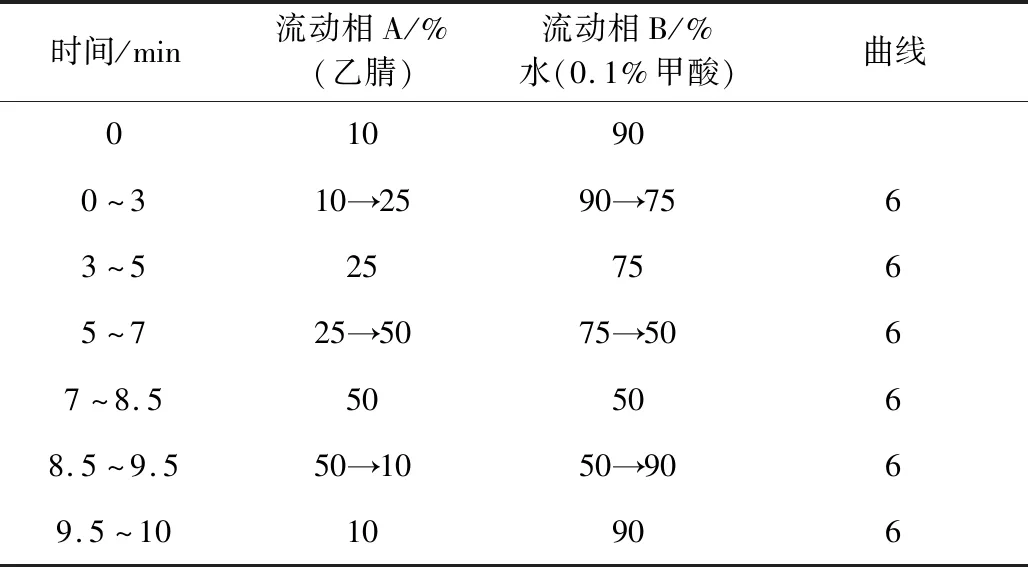
表1 梯度洗脱条件表Tab 1 Gradient elution condition
1.3.5 重复性试验和精密度试验 精密吸取头孢噻呋对照品储备溶液,制成每1 mL含头孢噻呋40 μg的对照品溶液,重复配制6份,进样,计算其峰面积RSD。精密吸取上述对照品溶液,重复进样6次,计算其峰面积RSD。
1.3.6 检测限和定量限的测定 对头孢噻呋的标准工作液,进行UPLC的分析,并逐级降低其浓度,以溶液检测时的信噪比S/N≥3作为检测限、S/N≥10作为定量限。
1.3.7 不同色谱条件样品检测比较 分别使用高效液相色谱仪(参照农业农村部公告第11号文[1],紫外检测器,254 nm;流速:1.5 mL/min;进样量:20 μL)和超高效液相色谱仪(光电二极管阵列检测器,254、292 nm;流速:0.35 mL/min;进样量:1 μL)在不同的色谱条件下运行,对同一样品中头孢噻呋的含量和出峰时间分别进行比较。
2 结果与分析
2.1 色谱分离 在优化的色谱条件下,测得头孢噻呋色谱峰峰形良好,且均达到基线分离,在1.3.4项条件下,头孢噻呋对照品和头孢噻呋晶体注射液样品,色谱保留时间约为5.05 min,分离度均满足要求。头孢噻呋UPLC色谱图见图1。

(a.40 μg/mL头孢噻呋对照品;b.10%头孢噻呋晶体注射液;c.20%头孢噻呋晶体注射液)图1 UPLC图(254 nm 1 μL)Fig 1 (40 μg/mL Ceftiofur reference,10% Ceftiofur Crystalline Free Acid Injection,20% Ceftiofur Crystalline Free Acid Injection)chromatogram UPLC 254 nm 1 μL
2.2 线性 在选定的色谱条件下,使用梯度洗脱的方法,可以有效地分离目的峰,头孢噻呋在4~200 μg/mL的范围内,线性回归方程为y=6417.2x-2328.8,R2>0.9998。其标准曲线见图2。

图2 头孢噻呋标准曲线Fig 2 Standard curve of Ceftiofur
2.3 重复性和精密度试验 在选定的色谱条件下,配制40 μg/mL头孢噻呋对照品溶液,重复配制6份,进样,测得头孢噻呋峰面积RSD为0.33%;取40 μg/mL头孢噻呋对照品溶液,重复进样6次,测得头孢噻呋峰面积RSD为0.21%,均满足实验要求。
2.4 检测限和定量限 2 μg/mL头孢噻呋对照品溶液信噪比≥3,为检出限,4 μg/mL头孢噻呋对照品溶液信噪比≥10,为定量限。
2.5 不同色谱条件样品检测结果的比较 不同色谱条件下的主成分理论塔板数、保留时间等参数的比较见表2。

表2 不同色谱条件下的主成分不同色谱参数的比较Tab 2 Comparison of principal components and chromatographic parameters under different chromatographic conditions
由表2可见,使用的Waters 的C8 色谱柱理论塔板数非常高,性能是完全满足要求的。通过响应值比较及光谱图各成分的最大吸收波长为254 nm和292 nm,两波长结果偏差极小,小于1%,都能满足检测需求;农业农村部质量标准选择的254 nm,但292 nm的响应值较高,所以选择292 nm。光谱图见图3;色谱图见图1、图4。保留时间为约5.05 min,满足检测需求。

图3 头孢噻呋对照品光谱图Fig 3 Ceftiofur control spectrum
使用Waters超高效液相色谱仪(本实验色谱条件1.3.4项)和高效液相色谱仪(1.3.7项),对同一样品中头孢噻呋的含量分别进行了比较,无显著差异,相对偏差均小于1%,表明本实验方法简单可行,结果精确可靠。结果如表3所示。

表3 不同色谱条件检测结果表 (n=4)Tab 3 Test results using different chromatographic method (n=4)
由于两种色谱方法均已通过其方法学验证,均可以准确控制其指标成分。从检测效率上看,优选超高效液相色谱法(UPLC),各色谱图见图1、图4、图5。从样品噪音和峰形分离度等方面来看,优选超高效液相色谱仪条件,背景更干净,与杂质峰的分离度更好。

(a.40 μg/mL头孢噻呋对照品;b.10%头孢噻呋晶体注射液;c.20%头孢噻呋晶体注射液) (40 μg/mL Ceftiofur reference,10% Ceftiofur Crystalline Free Acid Injection,20% Ceftiofur Crystalline Free Acid Injection)图4 UPLC图(292 nm,1 μL)Fig 4 chromatogram UPLC 292 nm 1 μL

(a.40 μg/mL头孢噻呋对照品;b.10%头孢噻呋晶体注射液;c.20%头孢噻呋晶体注射液) (40 μg/mL Ceftiofur reference,10% Ceftiofur Crystalline Free Acid Injection,20% Ceftiofur Crystalline Free Acid Injection)图5 HPLC图(254 nm 1 μL)Fig 5 chromatogram HPLC 254 nm 1 μL
3 讨论与结论
3.1 UPLC方法色谱柱耐用性实验 本研究将头孢噻呋的对照溶液利用PDA检测器采集其光谱图,在波长190~400 nm范围内进行扫描,头孢噻呋在254/292 nm处有最大吸收,根据光谱图可以判断含有主成分;改变流速0.34、0.36 mL/min,柱温35 ℃不变,保留时间上下浮动0.3 min以内。改变柱温33、38 ℃,流速0.35 mL/min不变,保留时间上下浮动0.3 min以内,均能达到良好的分离度和精确的含量测定结果。色谱柱性能稳定,适合本项目头孢噻呋含量的测定。最终选择292 nm作为检测波长,35 ℃柱温,保留时间约为5.05 min。
3.2 本方法与农业农村部颁布的进口质量标准[3]方法的对比 本实验分别采用建立的超高效液相色谱方法和标准规定的高效液相色谱方法,对兽药企业生产的头孢噻呋晶体注射液进行含量测定,测得头孢噻呋晶体注射液中头孢噻呋含量相对偏差均小于1%,说明本试验建立的超高效液相色谱方法满足该产品质控检测要求。此外,超高效液相色谱法流速为0.35 mL/min,运行10 min,每个样品需要消耗3.5 mL流动相;高效液相色谱法流速为1.5 mL/min,运行时间14 min,每个样品需要消耗21 mL流动相。通过比较,超高效液相色谱法更节约实验溶剂等,每个样品节省流动相16.5 mL、缩短4 min分析时间,提高了工作效率。
本实验建立的超高效液相色谱法,对头孢噻呋晶体注射液中头孢噻呋进行定性和定量测定,方法快速,可以作为企业内控标准方法,具备精准快捷、经济环保的特点,能有效控制头孢噻呋晶体注射液的质量。
