伏立康唑滴眼液的处方优化及质量控制
2012-11-21刘美欣高翔刘彤闫瑾张毅天津市眼科医院天津市眼科学与视觉科学重点实验室天津30000天津医科大学药学院天津300070
刘美欣,高翔,刘彤,闫瑾,张毅(.天津市眼科医院天津市眼科学与视觉科学重点实验室,天津30000;.天津医科大学药学院,天津 300070)
伏立康唑滴眼液的处方优化及质量控制
刘美欣1*,高翔2,刘彤1,闫瑾1,张毅1(1.天津市眼科医院天津市眼科学与视觉科学重点实验室,天津300020;2.天津医科大学药学院,天津 300070)
目的:设计伏立康唑滴眼液的处方并建立其质量控制方法。方法:以滴眼液渗透压的综合评分为指标,选取辅料丙二醇、聚乙二醇400和吐温-80的加入量为影响因素,通过3次正交试验进行处方优化设计及验证试验;考察优化处方所制制剂的初步稳定性(4周)和家兔刺激性,并对制剂进行质量评价。结果:优化处方中丙二醇、聚乙二醇400和吐温-80的加入量分别为0、25、125mL,其渗透压为0.230~0.320Osmol。4周稳定性考察中各指标未见明显变化;刺激性评分结果为0(无刺激性)。质量评价中本品pH值为5.5~6.5,百分含量为96.38%~102.61%。结论:本品制备工艺简单,质量可控,值得在临床推广使用。
伏立康唑滴眼液;处方设计;优化;质量控制
伏立康唑是新一代合成的三唑类广谱抗真菌药物,为氟康唑衍生物,化学结构与氟康唑类似。其作用机制是抑制真菌中由细胞色素P450介导的14α-固醇去甲基化,从而抑制麦角固醇的生物合成[1]。其抗菌谱广,对临床分离的支顶孢霉属、链格孢属、双极霉菌属、荚膜组织胞浆菌有抗菌作用,在0.05~2μg·mL-1浓度以下可以抑制大多数的菌株[2]。目前国内临床已有其口服和注射剂型,滴眼剂型还处在实验室阶段尚未见商品上市。由于伏立康唑在水中的固有溶解度很低,为3.49×10-4g·mL-1,因此其要用于眼科的治疗,必须提高伏立康唑在水中的溶解度。有报道[3],伏立康唑0.5%、1.0%或3.0%溶液于健康马眼滴眼(q 4h,连续滴7次)后,马眼房水质量浓度(μg·mL-1)分别为:1.43±0.37、2.35±0.78、2.40±0.29,即其在房水中的质量浓度已超过包括念珠菌属和曲菌属在内的多数眼部真菌感染株的抑制90%菌生长的最小药物质量浓度(MIC90)[4]。为此,笔者制备了0.5%的伏立康唑滴眼液,临床用于预防和治疗真菌性角膜炎和眼内炎。该制剂处方简单,工艺简便,适用于医院配制使用,现介绍如下。
1 仪器与材料
LC-10AVP型高效液相色谱(HPLC)仪(日本岛津公司);AG135电子分析天平、FE20型pH计(瑞士梅特勒-托利多仪器有限公司);SMC 30B渗透压摩尔浓度测定仪(天河医疗仪器有限公司)。
伏立康唑原料药(批号:20091102,纯度:99.0%)、伏立康唑对照品(批号:20091222,纯度:99.1%)均由珠海丽珠医药集团股份有限公司提供;0.5%伏立康唑滴眼液(天津市眼科医院制剂室,规格:每支2mL);丙二醇、聚乙二醇400(PEG)、吐温-80、5%苯扎溴铵均为药用级,甲醇、乙腈均为色谱纯,其他试剂均为分析纯。
家兔6只,♀♂各半,体重2.5~3.0kg,由北京维通利华实验动物有限公司提供,许可证号:SCXK(京)2005-0002,为动物提供符合卫生标准的颗粒饲料(北京科澳协力饲料有限公司,产品许可证号:京动许(字)2000第015号)。
2 方法与结果
2.1 滴眼液处方设计及制备
2.1.1 基础处方。伏立康唑、丙二醇、吐温-80、PEG、5%苯扎溴铵、注射用水。
2.1.2 正交试验a。选用L9(34)正交试验表,以空白滴眼液(不含主药)渗透压的综合评分为指标(标准值为0.2867Osmol),选取丙二醇、PEG和吐温-80的加入量为影响因素,考察各因素对渗透压的影响。空白滴眼液总量为20mL。若将渗透压的标准值设为1,则各因素水平的综合评分=(1-|实际值-标准值|)×100%。预试验因素水平见表1,试验结果见表2,方差分析见表3(表中“*”表示影响具有显著性,下各表同)。
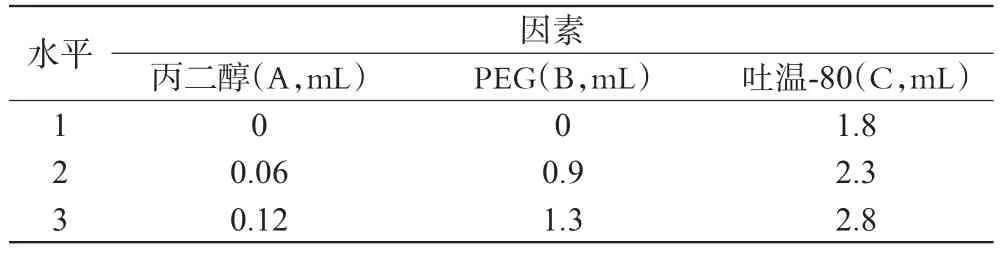
表1 试验a因素水平表Tab 1 Factors and levels of experiment a
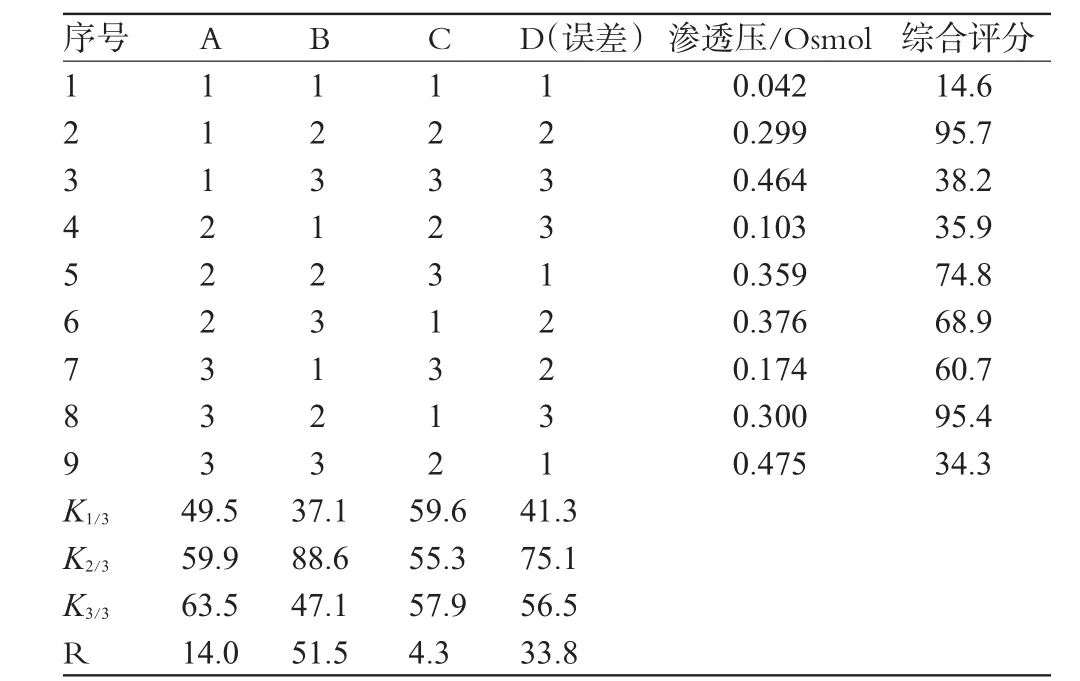
表2 试验a结果Tab 2 Results of experiment a
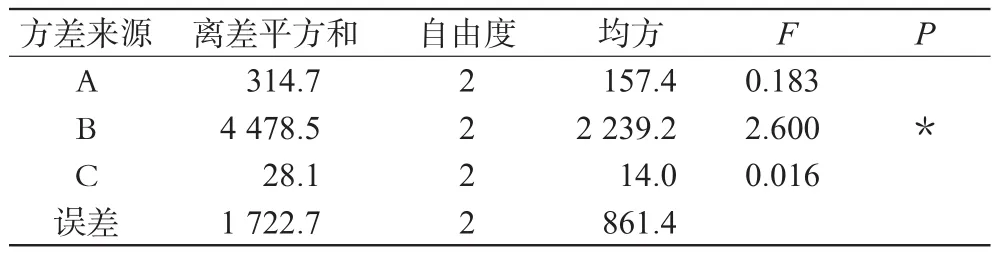
表3 试验a方差分析Tab 3 Analysis of variance of experiment a
经直观分析和方差分析可知,A3B2C1为最佳处方组合;其中B因素对滴眼液渗透压有显著影响,影响因素从大到小为:B>A>C。由于B因素是主要影响因素,则在下一试验中取其中间点,即加入量控制在1.0mL以内,同时加大丙二醇及吐温-80的用量,即丙二醇、吐温-80的加入量要超过表2中的水平3的量。由此设计了正交试验b。
2.1.3 正交试验b。因素水平见表4,正交试验结果见表5,方差分析见表6。
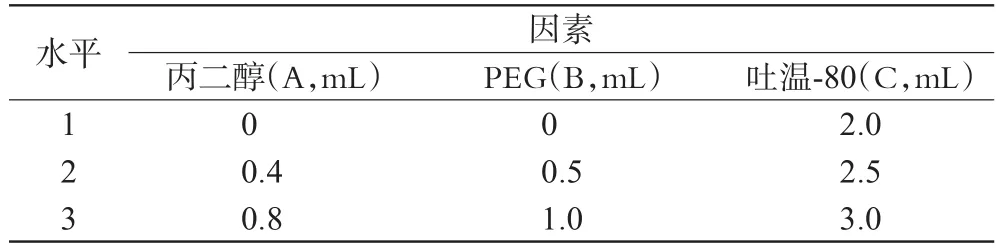
表4 试验b因素水平表Tab 4 Factors and levels of experiment b
经直观分析和方差分析可知,A1B1C2为最佳处方组合;3个因素中因素A对滴眼液渗透压有显著影响,影响因素从大到小为:A>B>C。
综合2次试验的结果,经分析,在丙二醇量较小时其对渗透压的影响效果居中;当其量加至0.4mL以上时其对渗透压的影响成为最主要因素。由此确定丙二醇水平为0~0.4mL、PEG水平为0~1.0mL,吐温-80水平为1~3.0mL,由此设计正交试验c。
2.1.4 正交试验c。因素水平见表7,试验结果见表8,方差分析见表9。
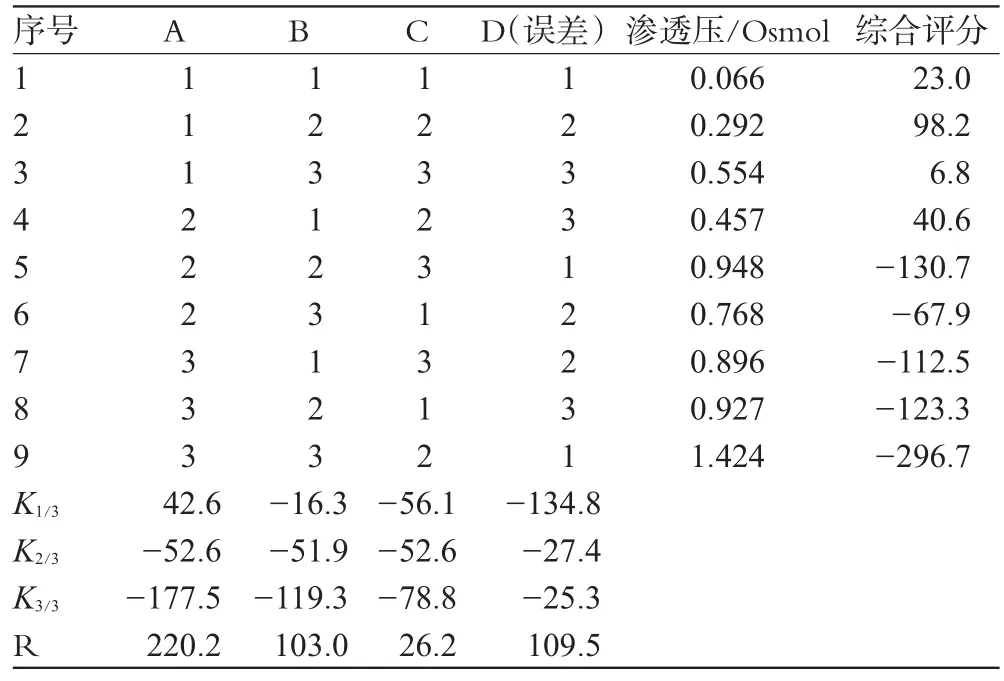
表5 试验b结果Tab 5 Results of experiment b
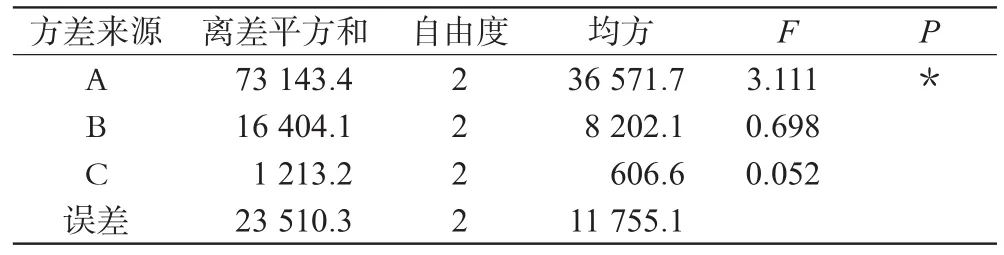
表6 试验b方差分析Tab 6 Analysis of variance of experiment b
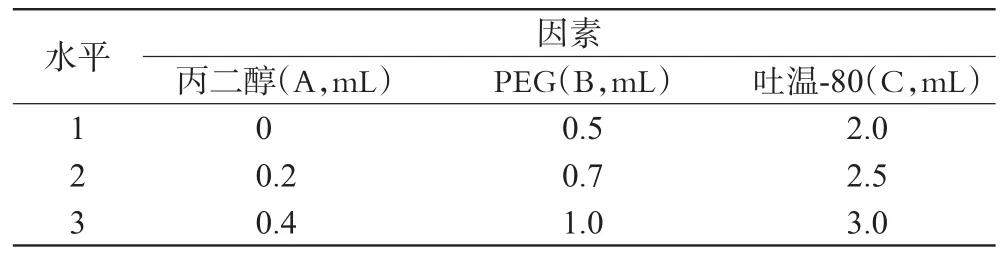
表7 试验c因素水平表Tab 7 Factors and levels of experiment c
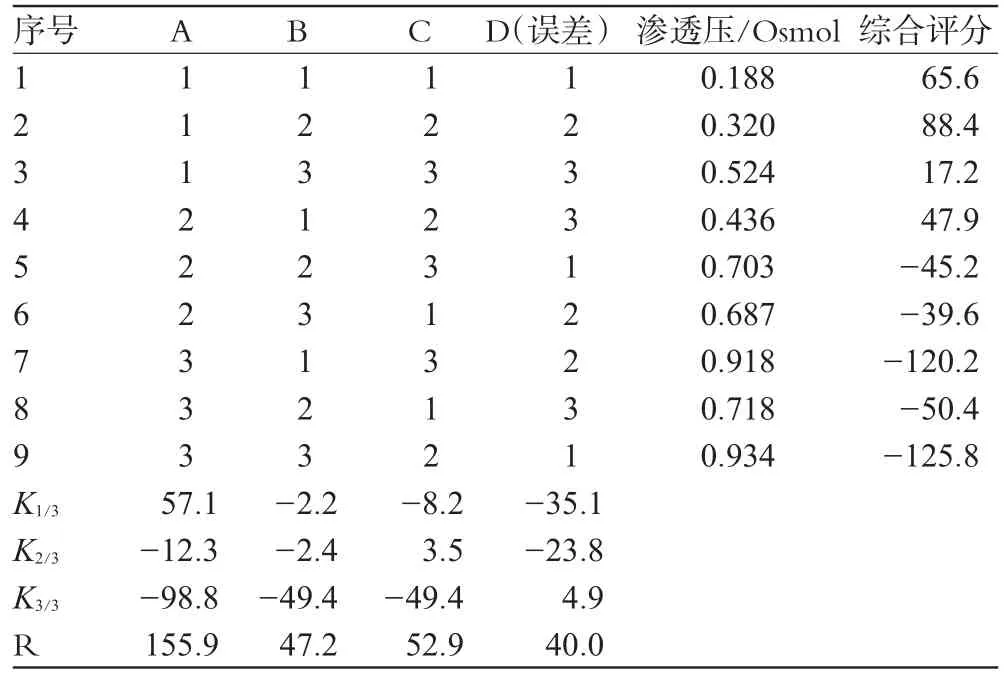
表8 试验c结果Tab 8 Results of experiment c
经直观分析和方差分析可知,A1B1C2为最佳处方组合,即丙二醇0mL、PEG 0.5mL、吐温-802.5mL。3个因素中A因素对滴眼液渗透压有较显著性影响(0.05<P<0.10),影响因素从大到小为:A>C>B。
2.1.5 滴眼液最佳处方。根据正交试验a、b、c结果,确定滴眼液最佳处方为:伏立康唑5g,吐温-80125mL,PEG 25mL,5%苯扎溴铵2mL,纯化水适量,合计1000mL。
处方中伏立康唑为主药,吐温-80为增溶剂,PEG为潜溶剂,苯扎溴铵为抑菌剂[5]。
2.1.6 制备。精密称取伏立康唑5.0g,置于200mL烧杯中,加入PEG 25mL,超声并搅拌使其分散均匀,取吐温-80125mL加入烧杯中,超声并搅拌使成为澄明溶液,将溶液移至适宜容器中,加入适量纯化水,超声并快速搅拌使其成为澄明溶液,加入纯化水至1000mL,用0.45μm微孔滤膜过滤,100℃流通蒸汽灭菌30min,无菌条件下灌装于5mL眼药瓶中,即得。
2.1.7 验证试验。以最佳处方制备3批样品,对其渗透压、pH值、百分含量等指标进行考察,结果符合要求,见表10。
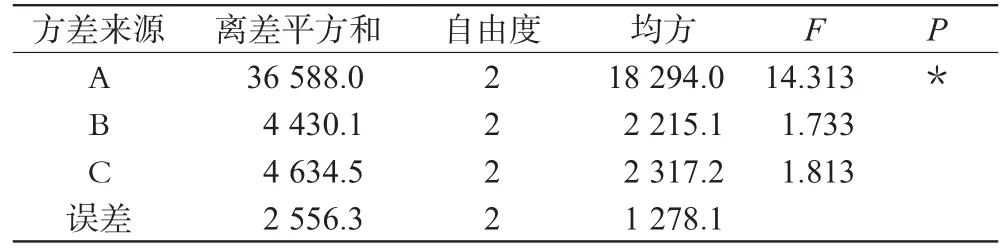
表9 试验c方差分析Tab 9 Analysis of variance of experiment c
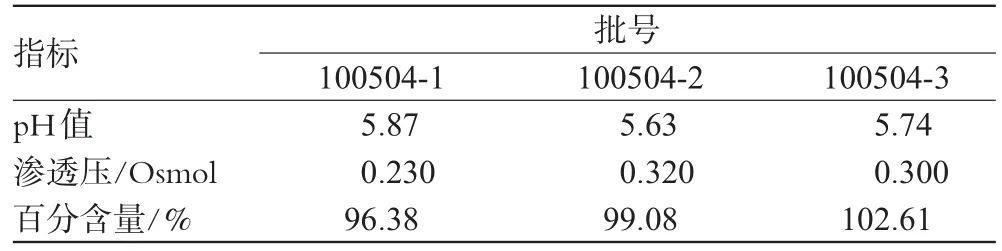
表10 3批样品质量评价Tab 10 Quality evaluation of 3batches of samples
2.2 伏立康唑滴眼液质量标准
2.2.1 性状。本品为淡黄色的澄明液体。
2.2.2 鉴别。取滴眼液2.0mL置于50mL量瓶中,加甲醇至刻度,于紫外分光光度计上扫描,结果在(256±1)nm波长处有最大吸收。
2.2.3 检查。本品pH值5.5~6.5;渗透压为0.230~0.320Osmol;其他均符合《中国药典》2010年版附录眼用制剂项下的规定[6]。
2.2.4 含量测定。(1)含量测定分析方法的建立。①色谱条件。色谱柱:Shim-packvp-ODS C18(150mm×4.6mm,5μm);流动相:乙腈-水=40∶60,流速:1.0mL·min-1;检测波长:256nm;柱温:30℃;进样量:20μL。②方法学考察。按相关方法进行线性试验、回收率试验和精密度试验。以浓度(c)为横坐标、峰面积(A)为纵坐标进行回归,得回归方程为A=157946.909736+13576.427012c(r=0.9998),伏立康唑检测浓度线性范围为0.0200~1.0000mg·mL-1。高、中、低3种浓度溶液平均回收率97.65%(RSD=0.69%);精密度试验结果RSD分别为0.12%、0.40%、0.58%,平均值为0.37%。(2)测定。对照品溶液:精密称取伏立康唑对照品20mg,加乙腈溶解,转移至100mL量瓶中定容。供试品溶液:精密量取2mL伏立康唑滴眼液至50mL量瓶中,加乙腈定容。各取2种溶液20μL进样,以外标法计算,3批样品百分含量结果见表10。
2.3 伏立康唑滴眼液初步稳定性考察
取3批样品,置于室温、相对湿度为60%的环境中放置4周,根据前述考察项目和方法,分别于第0、1、2、4周取样检测,各项考察指标与0周比较,结果无明显变化,详见表11。
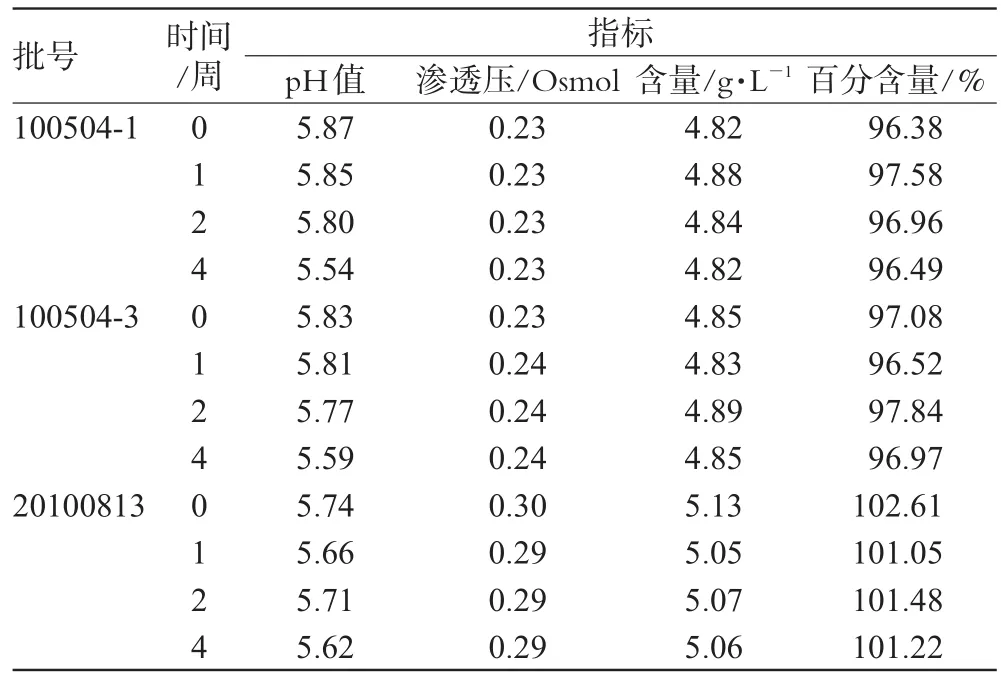
表11 样品初步稳定性考察Tab 11 Investigation of preliminary stability of samples
2.4 刺激性试验
预实验前家兔肉眼观察:角膜无混浊,结膜无充血、水肿及分泌物,瞳孔圆形,两侧等大,对光反射良好;裂隙灯检查:角膜透明,无云翳、斑翳;虹膜纹理清晰,无充血水肿。荧光素染色:2%荧光素钠溶液,每兔眼滴1滴后,用生理盐水冲洗干净,观察角膜未着色者为角膜正常。经上述预选出无眼疾而健康的家兔4只用于以下实验。
将家兔放入固定箱中,待其安定后,将眼睫毛剪去,轻轻把眼睑拉成环形,每只家兔左眼结膜囊内滴受试药物即:0.5%伏立康唑滴眼液(每眼50μL),滴入药液50μL,滴样量为0.25μg;右侧眼结膜囊内滴0.9%氯化钠注射液作为对照[7]。每次给药时压迫鼻泪管,并使眼被动闭合5~10s。每日3次,每次1滴,连续7d,记录家兔0、1、3、5、7d的眼局部反应情况,依据眼刺激反应评分(从正常到反应严重评分依次为0、1、2、3、4分)标准[8]对实验结果进行分析和评价,结果表明本品无刺激性,详见表12。
从教育教学内容来看,当前创新创业教育主要形式包括理论政策宣讲、创业人士经验分享等,内容较为单一。创业是一个体系化的工程,从前期的计划、项目的路演到后期公司的注册成立等,有非常多的细节需要了解。但这在课堂教学过程中基本无法完全涉猎。此外,各高校开展的创业大赛等千篇一律,形式简单,学生多为功利性的参加比赛积累综合测评加分等,竞赛水平大打折扣(王玉霞, 2015)。
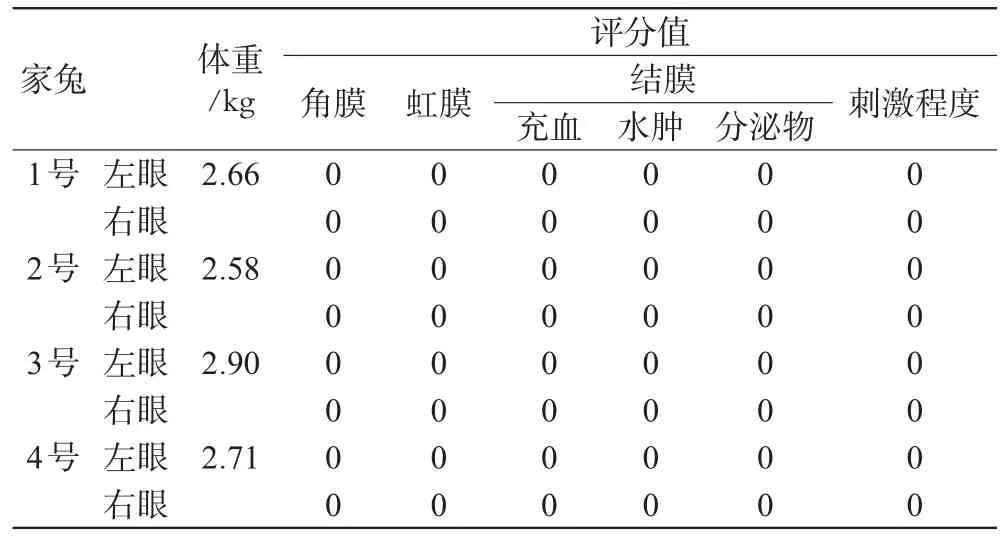
表12 家兔眼刺激反应评分结果Tab 12 Results of eyes stimulation response score of rabbits
3 讨论
3.1 立题依据
真菌性角膜炎(Fungal keratitis,FK)是一种严重的致盲性眼病。20世纪90年代后,FK发病率明显升高,已由原来单纯疱疹病毒性角膜炎占首位演变为真菌性角膜炎占首位,并且还有上升的趋势[9]。目前,眼科常用的局部抗真菌药物有两性霉素B、那他霉素和氟康唑,酮康唑和伊曲康唑等用于口服。那他霉素价格昂贵未能普及;两性霉素B毒性大,眼部刺激症状明显;氟康唑眼内通透性较好、刺激性小、抗真菌谱广,但其抗真菌作用不如两性霉素B;且由于临床上唑类药物广泛应用导致耐药菌株日渐增多[1]。而随着2002年新三唑类抗真菌药伏立康唑的上市,由于其对临床常见真菌的抗菌活性显著,因此,为眼科真菌感染性疾病的治疗提供了有力的武器[10]。伏立康唑通常耐受良好,最常见的不良反应为可逆性视力障碍,表现为视觉改变、视力模糊、色觉改变或畏光,通常为轻度,口服用药者发生率约15%,静脉给药者接近30%;13.4%患者可发生血清氨基转移酶升高,因此,应用伏立康唑的患者应定期监测肝功能[11]。局部用药不良反应的报道还没发现。体外试验证实伏立康唑质量浓度≤250mg·L-1时,对视网膜色素上皮细胞及视神经胶质细胞无毒性,未见明显视网膜毒性[12]。伏立康唑25μg玻璃体注射0.1mL可应用于真菌性眼内炎的治疗[13],其局部应用在房水和玻璃体中均能达到较高的药物质量浓度[14]。笔者据此设计了伏立康唑滴眼液。
3.2 正交试验参考指标的确定
滴眼液的渗透压应尽量与泪液等渗。高渗溶液容易吸收水分,从而使眼部组织脱水、干燥而产生不适的感觉;低渗溶液则会造成角膜组织膨胀而引起疼痛。2010年版《中国药典》附录眼用制剂项[6]下新增渗透压检查项,因此,本试验以渗透压为正交试验的参考指标。人眼可耐受的渗透压范围是0.8%~1.2%NaCl溶液的渗透压[5],在渗透压摩尔浓度比(OT/OS)值为0.8~1.2的范围内大多数人可以耐受,即渗透压为0.228~0.372Osmol。
3.3 增溶剂的选择
伏立康唑在水中溶解度小,易溶于有机溶剂,所以选择适当增溶剂是提高伏立康唑溶解度的有效方法。查阅文献[15]获知在伏立康唑注射用灭菌粉末的溶解过程中使用了专用溶媒:丙二醇-乙醇(1∶1.6)。笔者先尝试使用丙二醇作为增溶剂,但效果不是很好,加入量要在0.8mL以上才能使伏立康唑溶解,而预试验显示当其量加至0.4mL以上时其对渗透压的影响成为最主要因素,另外用量较大还可引起刺激性增加。吐温-80作为非离子表面活性剂,较阴离子及阳离子表面活性剂毒性低,安全性能好,因此,笔者尝试选择吐温-80作为增溶剂。PEG作为潜溶剂,在适当比例条件下可以较好地增加主药的溶解度,控制其对渗透压的影响。本文的处方及制备方法可使伏立康唑的滴眼液浓度达到0.5%,从而发挥良好的抗真菌活性,试验结果较为理想。
3.4 流动相的选择
根据伏立康唑的溶解性,其在水中几乎不溶,而在乙腈溶液中易溶,因此选择乙腈-水体系作为流动相。分别以不同比例的流动相进行试验:以乙腈-水(60∶40)作为流动相,保留时间太短(2.140min),不易于测定,且理论板数较低(3200);以乙腈-水(50∶50)作为流动相,保留时间较好,但主峰与有关物质峰分离度较差(0.65)。最后确定以乙腈-水(40∶60)作为流动相,结果主峰保留时间为5.658min,与有关物质分离度较好(1.67),而且理论板数较高(4400.23)。经过方法学考察,表明此方法操作简单快捷,结果准确可靠。
综上所述,该制剂处方简单、工艺简便、质量可控,适用于医院配制使用,值得在临床推广使用。
[1] 陈祖基.新型抗真菌药在眼科的研究进展[J].眼科研究,2007,25(8):629.
[2] Shapiro BL,Lalitha P,Fothergill AW,et al.Sensitivity of filamentous fungi isolated from fungal keratitis to amphotericin B,natamycin,caspofungin,itraconazole,voriconazole,and posaconazole[J].Invest Ophthalmol Vis Sci,2005,46(ARVO abst):2622.
[3] Clode AB,Davis JL,Salmon J,et al.Evaluation of concentration of voriconazole in aqueous humor after topical and oral administration in horses[J].Am J Vet Res,2006,67(2):296.
[4] Hariprasad SM,Mieler WF,Holz ER,et al.Determination of vitreous,aqueous,and plasma concentration of orally administered voriconazole in humans[J].Arch Ophthalmol,2004,122(1):42.
[5] 陈祖基.眼科临床药理学[M].北京:化学工业出版社,2002:35-36.
[6] 国家药典委员会.中华人民共和国药典(二部)[S].2010年版.北京:中国医药科技出版社,2010:附录ⅠG.
[7] 王文彤,陶遵威,张 娜,等.盐酸左氧氟沙星滴眼液在兔眼房水内的药动学[J].中国医药工业杂志,2011,4(2):117.
[8] 国家食品药品监督管理局.化学药物急性毒性试验技术指导原则[S].2006.
[9] 刘昭升,谢素贞,闫 蕾,等.福建地区真菌性角膜炎的调查[J].中国眼耳鼻喉科杂志,2009,9(4):239.
[10] Bunya VY,Hammersmith KM,Rapuano CJ,et al.Topical and oral voriconazole in the treatment of fungal keratitis[J].Am J Ophthalmol,2007,143(1):151.
[11] 申兰慧,石 涛,张 岩,等.新一代广谱抗真菌药伏立康唑[J].东南大学学报,2004,23(1):62.
[12] Kernt M,Neubauer AS,de Kaspar HM,et al.Intervitreal voriconazole:in vitro safety-profile for fungal endophthalmitis[J].Retina,2009,29(3):362.
[13] Lin RC,Sanduja N,Hariprasad SM.Successful treatment of postoperative fungal endophthalmitis using intravitreal and intracameral voriconazole[J].J Ocul Pharmacol Ther,2008,24(2):245.
[14] Wu PC,Lai CH,Tan HY,et al.The successful medical treatment of a case of Paecilomyces lilacinus keratitis[J].Cornea,2010,29(3):357.
[15] 肖 静,康学军,黄 晓.注射用伏立康唑专用溶剂的气相色谱含量测定[J].化学试剂,2005,27(10):616.
Formula Optimization and Quality Control of Voriconazole Eye Drops
LIU Mei-xin,LIU Tong,YAN Jin,ZHANG Yi(Tianjin Key Lab of Ophthalmology and Visual Science,Tianjin Eye Hospital,Tianjin 300020,China)
GAO Xiang(School of Pharmacy,Tianjin Medical University,Tianjin 300070,China)
OBJECTIVE:To design the formula of Voriconazole eye drops and to establish its method of quality control.METHODS:The formula was optimized by L9(34)orthogonal test for 3times with comprehensive score of osmotic pressure of eye drops as index using the amount of propylene glycol,PEG400and Tween-80as factors.The preliminary stability of preparations(4weeks) and its stimulation to rabbits were investigated,and the quality of preparation was evaluated.RESULTS:The added amounts of propylene glycol,PEG400and Tween-80were 0,25,125mL,and the osmotic pressure of the preparation was 0.230~0.320Osmol.The index of stability test had no significant change in 4weeks.Irriation score was 0(not irritant).In quality evaluation,pH value of sample was 5.5~6.5and labblled amounts were 96.38%~102.61%.CONCLUSION:The preparation of Voriconazole eye drops is simple in technology process and controllable in quality,and it is worthy of promoting in clinic.
Voriconazole eye drops;Formula design;Optimization;Quality control
R943;R988.1;R978.5
A
1001-0408(2012)05-0430-04
DOI 10.6039/j.issn.1001-0408.2012.05.17
*副主任药师。研究方向:医院药学、医院制剂。电话:022-27313336-80162。E-mail:lmxing1964@sina.com
2011-03-09
2011-06-07)
