BRøNSTED酸性离子液体催化合成辛酸甘油酯的研究
2012-11-20杨丽萍潘秋月孙培龙孟祥河
杨丽萍 潘秋月 孙培龙 孟祥河
(浙江工业大学生物与环境工程学院1,杭州 310014)
(浙江经贸职业技术学院应用工程系2,杭州 310018)
BRøNSTED酸性离子液体催化合成辛酸甘油酯的研究
杨丽萍1潘秋月2孙培龙1孟祥河1
(浙江工业大学生物与环境工程学院1,杭州 310014)
(浙江经贸职业技术学院应用工程系2,杭州 310018)
以双磺基的Brønsted酸性离子液体1-磺酸丁基-3-甲基咪唑硫酸氢盐[MIm(CH2)4SO3H][HSO4])催化辛酸与甘油酯化合成低热量的中碳链三酰甘油,研究了催化剂用量、酸醇物质的量比、反应温度、反应时间对酯化反应的影响,在最优条件下考查了工艺稳定性及催化剂重复使用性能。结果表明,[MIm(CH2)4SO3H][HSO4]具有较高的酯化催化活性和重复使用性能。优化的合成辛酸甘油酯的工艺条件为:辛酸甘油物质的量比为3.5∶1,催化剂用量为底物质量的1%,反应温度160℃,反应时间6 h。在此条件下,酯化率达85%,三酰甘油质量分数达到80%。催化剂重复使用5次,仍保持90%的催化活性。
辛酸甘油酯 中碳链三酰甘油 Brønsted酸性离子液体 酯化
中碳链三酰甘油是指甘油的三个羟基均结合中碳链脂肪酸(C6-C12)的甘油酯,缩写为MCT,主要包括辛酸三酰甘油、癸酸三酰甘油和辛酸-癸酸三酰甘油[1]。作为一种优质的低热量油脂,MCT消化吸收快、热量低,食用后不会引起肥胖,因此广泛应用于食品、医药领域。
目前合成MCT的方法有化学法和酶法,其中化学法大多在超过200℃的高温高压下进行[2]。化学法传统的酯化反应催化剂主要是硫酸、氢氟酸及无水AlCl3等,其催化活性高,但具有强腐蚀性,后处理复杂,产生大量酸性废水。为此,长期以来,科研工作者在催化剂和生产工艺等方面进行了大量的改进工作,如用酸性阳离子交换树脂[3]、沸石分子筛[4]、杂多酸(盐)[5]、固体超强酸[6]和离子液体[7]等来代替硫酸。其中杂多酸(盐)价格昂贵,直接作均相催化剂回收困难;固体超强酸具有环境友好、选择性高及产物易分离等优点,但是催化剂制备周期长,高温下易炭化失活。
鉴于上述问题,人们广泛开展了对酸性离子液体的研究。酸性离子液体方面,国内外研究较早的是以金属卤化物为阴离子的Lewis酸性离子液体,尤其是AlCl3类离子液体,但此类离子液体的水稳定性较差,限制了其应用。Cole等[8]报道了一系列在N-烷基咪唑和三苯基磷阳离子上有烷基磺酸官能团的Brønsted酸性离子液体,成功地用于酯化、成醚等酸催化反应。Xing等[9]改进合成了几种在吡啶阳离子上含烷基磺酸官能团的Brønsted酸性离子液体,对酯化反应研究表明,具有HSO4阴离子的离子液体具有最好的催化效果。Fang等[10]通过改变阳离子中碳链长度及阴离子的类型制备了一系列以磺酸季铵为阳离子的Brønsted酸性离子液体,将其作为不同的酸与醇发生Fischer酯化反应的溶剂和催化剂,发现其催化活性与阴离子种类及离子液体与原料的相容性有关,阴离子酸性越高,原料与离子液体相容性越好,催化活性越高。
本试验探讨了不同催化剂催化合成辛酸甘油酯的效果,重点研究了[MIm(CH2)4SO3H][HSO4]催化辛酸与甘油的可行性。
1 材料与方法
1.1 材料与仪器
甘油(AR),正辛酸(CP):国药集团化学试剂有限公司;其余分析用试剂均为分析纯或色谱级;[MIm(CH2)4SO3H][HSO4],[BMIM][PF6],[BMIM][BF4]:上海成捷化学有限公司;负载催化剂[BMIM][PF6]/AlCl3和 S2O82-/Fe2O3-Al2O3的制备方法分别参见文献[11],[12]。
Aglient 7890A气相色谱仪:安捷伦公司。
1.2 方法
1.2.1 辛酸甘油酯的合成
在配有温度计、变色硅胶(除水)、充满氮气的气球的50 mL三口瓶内,加入0.15 mol辛酸与适量甘油,置于油浴中,磁力搅拌使之均匀混合,待温度升至设定值,加入适量催化剂,开始计时,间隔取样,于封闭体系反应至预定时间后,停止反应。每个反应重复2次,取平均值。
1.2.2 辛酸酯化率的测定
吸取100 μL样品准确称重,以反应后每克样品中游离脂肪酸减少的毫摩尔数与原料中游离脂肪酸的毫摩尔数的百分比表示。公式如下:
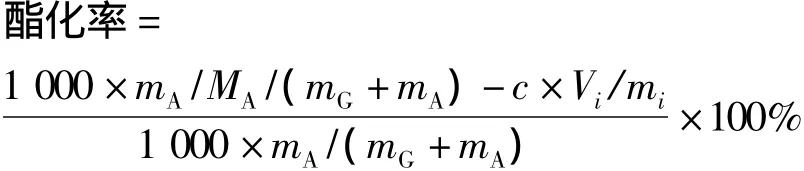
考查酸醇比对反应的影响时,折算成羟基的酯化率,即

式中:mA为辛酸的质量/g;mG为甘油的质量/g;mi为样品的质量/g;c为氢氧化钠溶液的浓度/mol/L;Vi为氢氧化钠溶液的消耗量/mL;MA为辛酸的摩尔质量/g/mol;MG为甘油的摩尔质量/g/mol。
1.2.3 产品分析
酯化过程监测采用TLC法,展开剂为正己烷/乙醚/乙酸(70/30/5,体积比);产物组成采用GC法,GC条件:Aglient 7890A,FID,HP-5(30 m ×0.32 mm,0.25 μm),进样口:320 ℃,分流比50∶1,检测器:320℃。柱温250℃,保持3 min,5℃/min升至280℃,保持6 min。载气:高纯氮气,流速25 mL/min;空气:400 mL/min;氢气:30 mL/min。
2 结果与讨论
2.1 催化剂的选择
2.1.1 不同催化剂催化性能的比较
不同催化剂对辛酸甘油酯合成的影响见表1。当无催化剂时,由于辛酸的自催化作用,反应10 h辛酸的酯化率为44.5%。ZnCl2催化下辛酸的酯化率最高,达到 79.4%,[MIm(CH2)4SO3H][HSO4]次之,产物中辛酸三酰甘油的含量却高于前者;ZnCl2催化得到的辛酸甘油酯颜色较深,离心后下层形成较厚皂状物质,[BMIM][PF6]/AlCl3、[BMIM][PF6]、[BMIM][BF4]催化过程中有白色物质形成,附在反应器壁,且不易清洗,可能是离子液体高温分解所致。[MIm(CH2)4SO3H][HSO4]、S2O82-/Fe2O3-Al2O3催化反应较快,2 h辛酸的酯化率均达到54%以上,略低于已知催化效率较好的磷钨酸,反应结束后产物与催化剂自动分相。但其中S2O82-/Fe2O3-Al2O3的炭化现象比较严重,制备工艺复杂、周期较长。
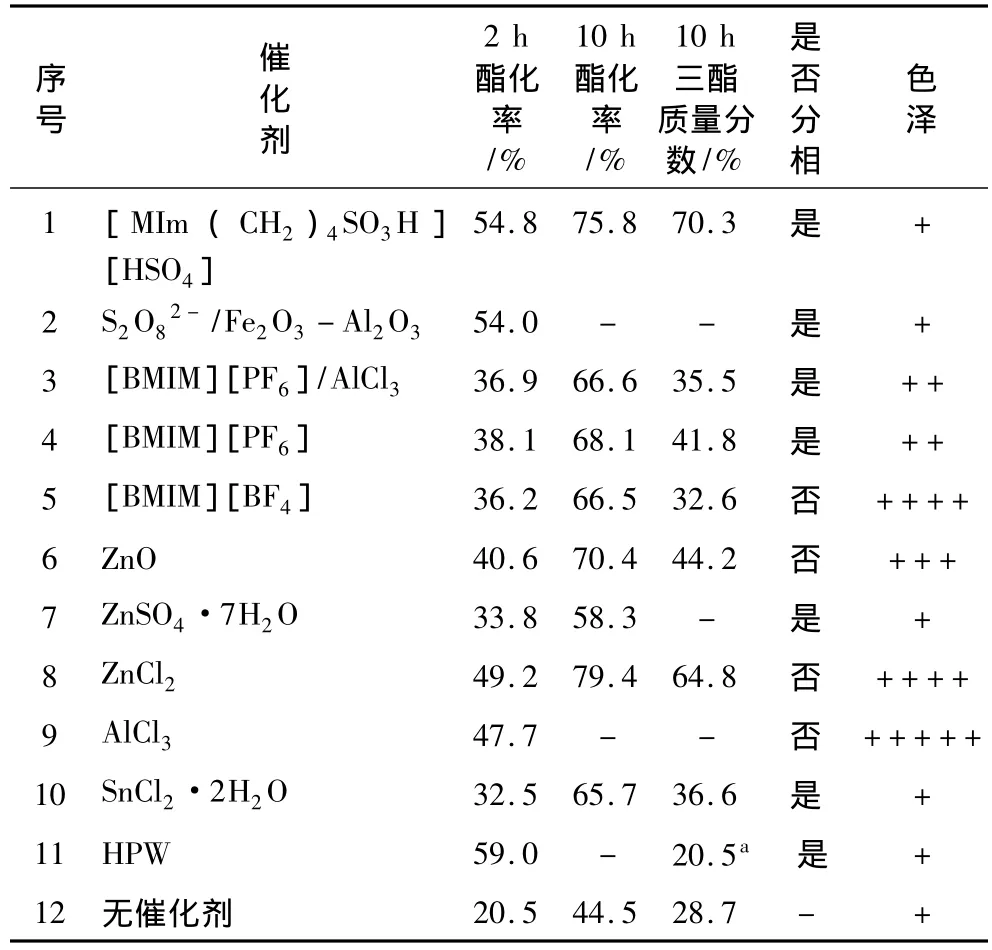
表1 离子液体催化剂与其他酯化催化剂催化性能比较
根据质子酸催化酸醇酯化机理,一般认为,质子酸解离的H+首先进攻羧基中的羰基氧使其质子化,提高了羰基碳原子的亲电能力,有利于醇羟基氧的进攻形成新的碳氧键;另外H+与中间体上羟基氧结合,形成鎓盐,使难于消除的OH转变成易消除的H2O,有利于中间体到产物的转变[13]。
从以上的机理可以看出,质子酸催化酯化反应的关键在于提供了 H+,[MIm(CH2)4SO3H][HSO4]是一种具有强酸性的质子酸,Hammett函数值约为1.3,H2SO4约为 1.2[14],其催化酯化反应的机理应该与一般的质子酸相同。[MIm(CH2)4SO3H][HSO4]含有两个磺酸基,阴、阳离子共有两个可以电离的氢,对酯化反应具有较好的催化活性。
2.1.2 [MIm(CH2)4SO3H][HSO4]的溶解性能
为考查[MIm(CH2)4SO3H][HSO4]在反应物及产物中的分散性,将[MIm(CH2)4SO3H][HSO4]分别与甘油、辛酸、辛酸三酰甘油按反应体系中的比例混合,涡流振荡器混合3 min,于设定温度静置,观察体系分相情况,结果见表2。
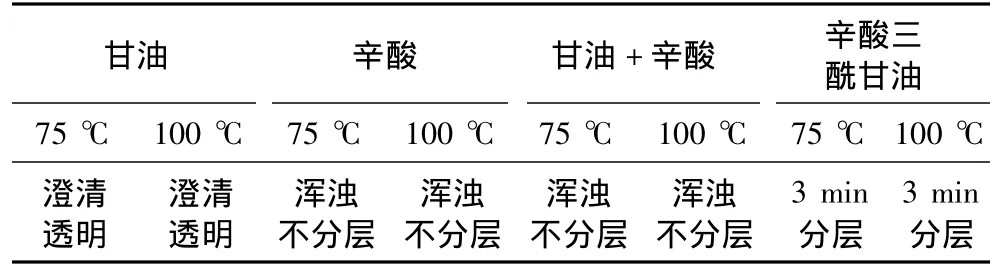
表2 [MIm(CH2)4SO3H][HSO4]在反应物及产物中的分散性
[MIm(CH2)4SO3H][HSO4]与极性的甘油互溶,与辛酸可以稳定共存,与非极性的三酰甘油不相容,3 min即自动分层,这可能是因为亲水基团HSO4的存在降低了离子液体的亲酯性。可以预见,在反应体系中,均匀分散的[MIm(CH2)4SO3H][HSO4]好像选择性透过的筛子一样,未反应的底物分子进入这个“筛子”,产物三酰甘油分子不断滤出,酯化过程生成的水则不断被硅胶吸收,这相当于不断移除产物,使得反应始终向酯化方向进行。因此[MIm(CH2)4SO3H][HSO4]作催化剂的反应酯化率及产物中三酰甘油含量均较高。
2.2 酯化反应条件对三辛酸甘油酯合成的影响
2.2.1 催化剂用量
从图1可以看出,随着催化剂用量的增加,辛酸的酯化率也相应地提高,当催化剂用量达到基于底物质量1%时,辛酸的酯化率达到66%以上,再增加催化剂用量酯化率无明显变化。因此选取催化剂用量为底物质量的1%。
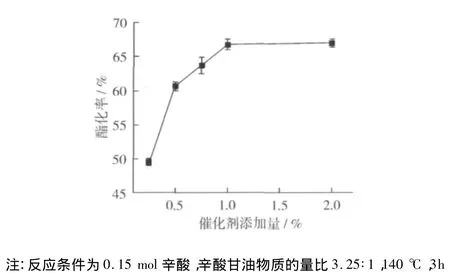
图1 催化剂用量对酯化反应的影响
2.2.2 辛酸甘油物质的量比
目标产物辛酸三酰甘油要求将甘油的3个羟基全部酯化,由于空间阻隔效应的存在,反应要在较高的温度下进行,目标产物的含量通常也比较低。考虑到尽量减少副反应产物偏甘油酯,尽可能把原料中的甘油的3个羟基全部转化,通常在反应体系中采取酸过量。为此,考察了辛酸甘油物质的量比对甘油羟基酯化率的影响,其结果如图2所示。
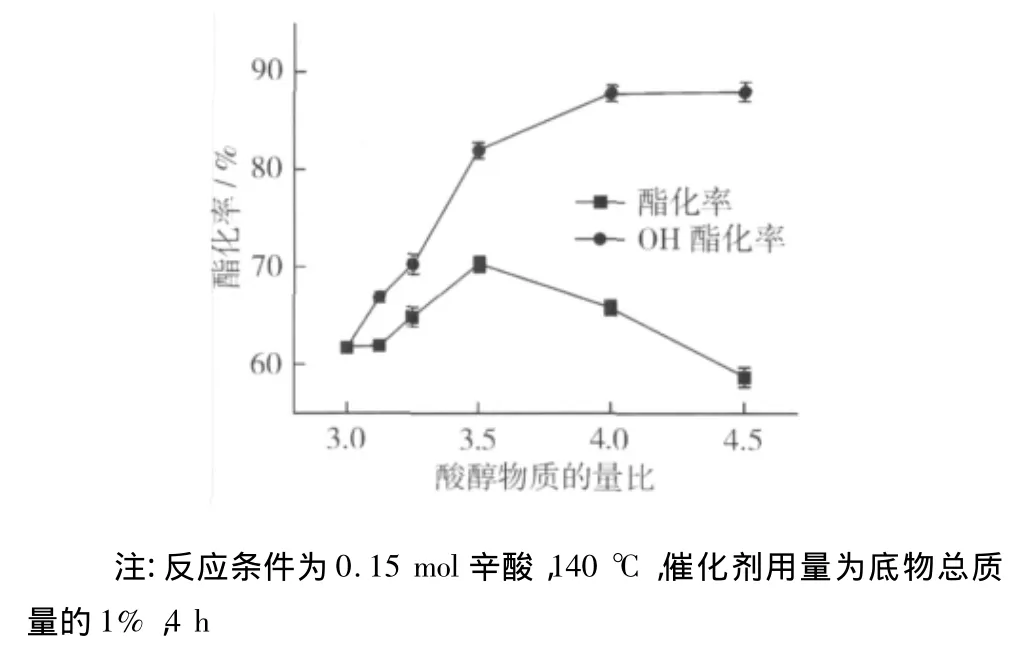
图2 辛酸甘油物质的量比对酯化反应的影响
从图2可知,随着辛酸甘油物质的量比的提高,甘油羟基的酯化率快速增加,辛酸酯化率则先升后减。当辛酸甘油物质的量比为3.5∶1时,甘油羟基的酯化率达到82%以上辛酸酯化率达到最大(70.3%),进一步提高酸醇物质的量比,羟基的酯化率虽然进一步增加到87%,但脂肪酸的酯化率反而下降,过量的脂肪酸会造成后续分离的困难。因此综合考虑酯化率及脂肪酸的节约,选择酸醇物质的量比 3.5∶1 为宜。
2.2.3 反应温度
由图3可以看出,温度越高,初始反应速率越快,反应越快达到平衡;较低温度下反应的酯化率随着时间的延长,可以与较高温度下相当。当温度为180℃时,2 h即可基本达到平衡,但是产物色泽深,催化剂炭化现象十分严重,因此反应温度取160℃。

图3 温度对酯化反应的影响
2.2.4 反应时间
从图4可以看出,随着反应时间的延长,酯化率不断上升;前2 h反应速率较快,随着底物的消耗和酯化产物的积累,反应速率变缓,反应6 h左右酯化基本达到平衡,酯化率达到85%,再延长时间,酯化率增幅不大,而产物色泽加深。因此,选择酯化反应较适宜的时间是6 h。
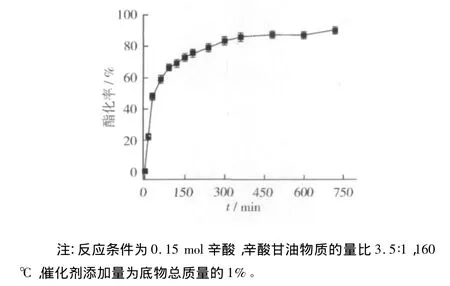
图4 时间对酯化反应的影响
2.3 工艺的稳定性及催化剂的重复使用性能
在辛酸甘油物质的量比3.5∶1、底物总质量1%的催化剂添加量,160℃下反应6 h,考察工艺稳定性和催化剂[MIm(CH2)4SO3H][HSO4]的重复使用性能。反应完成后,通过倾倒分离上层油相和下层离子液体,离子液体催化剂经正己烷洗去表面甘油酯后,直接重复使用。
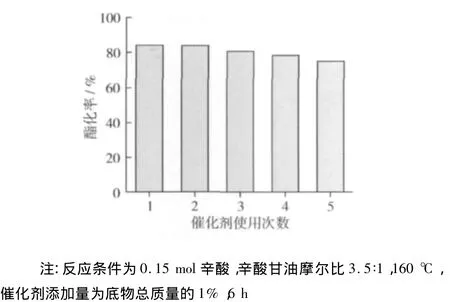
图5 催化剂重复使用性
最优条件下重复试验4次,酯化率依次是84.5%、85.1%、85.5%、84.2%,三酯质量分数依次是 80.7%、81.0%、81.4%、79.5%,平均值分别为(84.8± 1.03)%、(80.7 ± 2.02)%。[MIm(CH2)4SO3H][HSO4]重复使用5次,酯化率仅下降10%,表明[MIm(CH2)4SO3H][HSO4]在该酯化反应的催化中有优良的稳定性,可重复使用多次,有效降低反应成本。
3 结论
3.1 具有双磺基的 Brønsted酸性离子液体[MIm(CH2)4SO3H][HSO4]在催化合成辛酸甘油酯中具有较好的催化活性,2 h催化活性仅略低于磷钨酸。
3.2 [MIm(CH2)4SO3H][HSO4]为催化剂用于合成辛酸甘油酯的最佳工艺条件:酸醇物质的量比为3.5∶1,催化剂用量为基于底物质量的1%,反应温度160℃,反应时间6 h。在此所选择的条件下,酯化率达85%,辛酸三酰甘油质量分数达到80%。
3.3 [MIm(CH2)4SO3H][HSO4]作为辛酸和甘油酯化合成三辛酸甘油酯的催化剂,具有反应条件比较温和、酯化率高、产物中三酯含量高、可重复使用的优势,有一定的应用前景。
[1]余春涛.中碳链甘三酯合成与纯化的研究[D].无锡:江南大学,2004
[2]邵康群,支佩红,沈霞,等.中碳链甘油三酯合成研究进展[J].食品科学,2011(4):346 -347
[3]王树清.强酸性阳离子交换树脂催化合成甘油三乙酸酯的研究[J].南通大学学报:自然科学版,2005,4(1):25-27
[4]张进,肖国民.ZSM-5型分子筛的表面酸性与催化活性[J].分子催化,2002,16(4):307 -311
[5]张晋芬,高翔,徐华龙.微波辐射下活性炭负载杂多酸催化合成尼泊金丁酯[J].实验室研究与探索,2010,29(11):217-218
[6]苏娜,李坤兰,宫国梁.固体超强酸SO2-4/TiO2的制备及其在季戊四醇酯化反应中的催化性能[J].大连工业大学学报,2009,28(4):277 -280
[7]武光,吴伟.[EMIm]BF4离子液体催化酯化反应研究[J].现代化工,2006,26(5):31 -34
[8]Cole A C,Jensen J L,Ntai I,et al.Novel bronsted acidic ionic liquids and their use as dual solvent- catalysts[J].Journal of the American Chemical Society,2002,124(21):5962 -5963
[9]Xing H B,Wang T,Zhou Z H,et al.Novel bronsted - acidic ionic liquids for esterifications[J].Industrial & Engineering Chemistry Research,2005,44(11):4147 -4150
[10]Fang D,Zhou X L,Ye Z W,et al.Bronsted acidic ionic liquids and their use as dual solvent-catalysts for Fischer esterifications[J].Industrial& Engineering Chemistry Research,2006,45(24):7982 -7984
[11]陈卓,李梅,梁斌,等.室温离子液体介质中酯化反应的研究[J].西南师范大学学报:自然科学版,2006,31(3):66-69
[12]黄卫,李桂云,栗洪道.几种SO4/MxOy型固体超强酸酯化催化活性的研究[J].石油化工高等学校学报,2001,14(1):37-41
[13]岳彩波.离子液体中精细合成单元反应的研究[D].南京:南京理工大学,2007
[14]史娜,黄宝华,汪艳飞,等.咪唑硫酸氢盐离子液体催化酯化反应[J].化学试剂,2009,31(6):423 -426.
Study on the Synthesis of Caprylin Catalyzed by Brønsted Acidic Ionic Liquid
Yang Liping1Pan Qiuyue2Sun Peilong1Meng Xianghe1
(College of Biological& Environmental Engineering ,Zhejiang University of Technology1,Hangzhou 310014)
(Department of Application & Engineering,Zhejiang Economic & Trade Polytechnical2,Hangzhou 310018)
A Brønsted acidic ionic liquid,1-(4-sulfonic acid)-butyl-3-methylimidazolium hydrogen sulfate salt([MIm(CH2)4SO3H][HSO4])was used as a catalyst in synthesising a low -calorie medium -chain triglyceride from caprylic acid and glycerol.These parameters may affect conversion and tricaprylin yield were studied,including amounts of catalyst loaded,the molar ratio of caprylic acid to glycerol,reaction temperature and time.The process stability in the optimized conditions and the catalyst recyclable performance were also examined.Experimental results showed that,[MIm(CH2)4SO3H][HSO4]had a high catalytic activity and good recyclability for esterification.Optimized conditions were recommended as caprylic acid/glycerol ratio 3.5∶1,catalyst amount is 1%of the mass of the substrates,160 ℃,6 hours.Under these conditions,80%tricaprylin yield as well as 85%conversion was obtained.Catalyst was repeated for five times,and 90%catalytic activity was remained.
caprylin,medium - chain triglyceride,Brønsted acidic ionic liquid,esterification
TQ644
A
1003-0174(2012)03-0094-05
浙江省科技厅项目(2009C31140,2010C32017)
2011-06-28
杨丽萍,女,1986年出生,硕士,食品科学
孟祥河,男,1974年出生,副教授,硕士生导师,脂质研究
