高效液相色谱法同时测定双黄消炎片中黄芩苷和黄芩素含量
2012-11-06徐占方陈立柱姜雪敏
徐占方,陈立柱,姜雪敏,孙 菲
(黑龙江省鸡西市药品检验所,黑龙江 鸡西 158100)
双黄消炎片由三颗针、黄芩两味中药组方,具有消炎之功效[1],可用于咽喉痛、腹泻、痢疾、慢性痢疾等症,现行质量标准只有显微鉴别和黄酮类化合物的定性鉴别,无对黄芩主要成分的定量检测,无法有效控制产品的质量。黄芩质量好坏直接影响药品的疗效,黄芩的主要成分有黄芩苷、黄芩素、汉黄芩素[2]。对双黄消炎片中黄芩苷的高效液相色谱(HPLC)法测定已有报道[3-5],但仅用黄芩苷一种成分的含量不能全面地反映黄芩的质量。笔者建立了可同时测定双黄消炎片中黄芩苷、黄芩素两种主要成分含量的高效液相色谱法,报道如下。
1 仪器和试药
HP1100型高效液相色谱仪,HP1100型工作站(自动进样,紫外检测器);Sartorius电子天平;KQ-400KDE型高功率数控超声波清洗器;TU-1901型双光束紫外可见分光光度计(北京普析通用仪器有限责任公司)。黄芩苷对照品(批号为110715-200815,含量为95.2%),黄芩素对照品(批号为111595-200604),均购自中国药品生物制品检定所;双黄消炎片(市售样品3批,批号分别为20100924和20100305,通化万通药业有限公司;批号为20080701,吉林省俊宏药业有限公司);其他试剂均为色谱纯。
2 方法和结果
2.1 色谱条件
色谱柱:Agilent Eclipse XDB-C18柱(250 mm×4.6 mm,5μm);以甲醇(A)-0.4%磷酸溶液(B)为流动相梯度洗脱,40%A(0 min),80%A(40 min),40%A(60 min);检测波长:277 nm;流速:1.0 mL/min;进样量:10μL;柱温:30℃。在此条件下,理论板数不低于5 000,色谱图见图1。

图1 高效液相色谱图
2.2 溶液制备
精密称取样品适量(约相当于平均片重),置50 mL容量瓶中,加70%乙醇40 mL,超声提取40 min,放置至室温,加70%乙醇至刻度,摇匀,滤过,精密吸取5 mL,置20 mL容量瓶中,加甲醇稀释至刻度,摇匀,滤过,即得供试品溶液。分别精密称取经P2O5干燥过夜的黄芩苷对照品29.82 mg和黄芩素对照品10.61 mg,置同一50 mL容量瓶中,加甲醇适量,超声使溶解,用甲醇稀释至刻度,滤过,作为对照品贮备液。按双黄消炎片的处方、制法项下不加黄芩粉末,制备阴性样品,按供试品溶液制备的方法制成阴性对照品溶液。
2.3 方法学考察
线性关系考察:分别精密量取黄芩苷、黄芩素对照品贮备液1.0和0.5 mL,置同一10 mL量瓶中,加70%乙醇溶液稀释至刻度,摇匀,滤过,按上述色谱条件,分别进样 1,2.5,5,10,15,20,25μL,以峰面积 Y对质量浓度 X(μg/mL)进行回归分析。黄芩苷回归方程为 Y=37.45X+11.84,r=1.000 0(n=7),黄芩苷质量浓度在5.678~142.0μg/mL范围内与峰面积线性关系良好;黄芩素回归方程为 Y=61.55X-1.691,r=1.000 0(n=7),黄芩素质量浓度在2.122~53.05μg/mL范围内与峰面积线性关系良好。
精密度试验:取对照品溶液(含黄芩苷56.78μg/mL,黄芩素21.22μg/ml),重复进样5次。结果黄芩苷和黄芩素峰面积值的RSD分别为0.1%和0.3%(n=5),表明仪器精密度良好。
稳定性试验:精密吸取同一供试品溶液,分别在 0,2,4,8,12,16,24 h时重复进样。结果黄芩苷和黄芩素峰面积的 RSD分别为0.6%和0.7%(n=7),表明供试品溶液在24 h内稳定。
重复性试验:分别精密称取同一样品(批号为20080701)5份,依法制备供试品溶液并测定。结果黄芩苷和黄芩素平均含量分别为29.53 mg/g和9.053 mg/g,RSD分别1.2%和1.1%(n=5),表明方法重复性较好。
加样回收试验:取已知含量的样品(批号为20080701,平均片重为0.401 2 g)约0.2 g共6份,精密称定,分别置50 mL容量瓶中,分别精密加入对照品溶液(含黄芩苷2 917μg/mL和黄芩素 909 μg/mL)2.4,2.4,2.0,2.0,1.6,1.6 mL,加 70%乙醇溶液适量,超声40 min,放至室温,用70%乙醇溶液稀释至刻度,摇匀,滤过,精密吸取5 mL,置20 mL容量瓶中,加甲醇稀释至刻度,用微孔滤膜滤过,进样10μL,测定含量,计算回收率。结果见表1。
2.4 样品含量测定
取本品10片,精密称定,研细,精密称取适量(约相当于平均片重),按2.2项下方法制备供试品溶液。按拟订的色谱条件进样10μL,按峰面积外标法测定含量。结果见表2。

表1 加样回收试验结果(n=6)
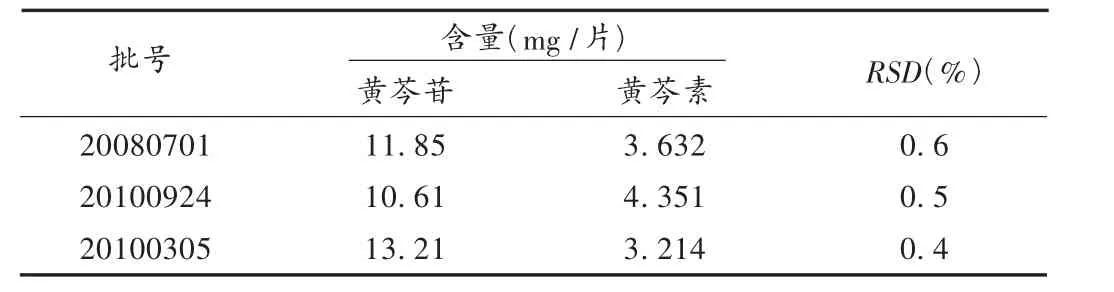
表2 样品含量测定结果(n=3)
3 讨论
分别取黄芩苷和黄芩素对照品适量,用流动相稀释到一定的质量浓度,照紫外分光光度法,在200~700 nm波长范围内扫描。结果黄芩苷、黄芩素的最大吸收波长分别是279 nm和277 nm,但在277 nm处黄芩苷和黄芩素分离效果好,故将测定波长确定为277 nm。
为在相对较短的时间内获得满意的分离效果,故采用梯度洗脱,色谱柱选用250 mm的长柱。流动相开始采用磷酸盐缓冲液-乙腈,黄芩苷和黄芩素分离效果不理想,采用甲醇和磷酸溶液定,梯度洗脱后取得了较好的分离效果。
在试验过程中,考察了单纯用甲醇超声30 min提取、70%乙醇超声30 min提取、70%乙醇加热回流3 h提取的效果,结果表明,用甲醇超声提取黄芩苷提取不完全,加热回流方法虽提取得彻底但比较费时费力,最终选用70%乙醇超声40 min提取。几种方法提取黄芩苷的差异较大。
本品的现行质量标准控制水平较低,仅对双黄消炎片中黄芩有显微鉴别,没有黄芩主要成分的定量检测。这给不法分子以可乘之机,以次充好,降低生产成本,但却影响了药品的疗效。而且在实际的监督中,药品检验部门按现行标准检验,只能出具合格报告书,不能定其为不合格产品。本含量测定方法的建立,对现行标准是有效的补充和提高。
[1]WS3-B-0235-90.中华人民共和国卫生部药品标准·中药成方制剂(第二册)[S].
[2]南京中医药大学.中药大辞典(下册)[M].第2版.上海:上海科学技术出版社,2006:2 806.
[3]莫海涛,刘 元,宋志钊.HPLC测定双黄消炎片中黄芩苷含量[J].中国民族民间医药,2009,18(17):24-25.
[4]宋吉莲,吕凤莲,袁明辉.HPLC测定双黄消炎片中黄芩苷含量[J].中国药事,2005,19(11):47-48.
[5]国家药典委员会.中华人民共和国药典(一部)[M].北京:化学工业出版社,2005:212.
