甲睾酮聚乳酸微球的制备及其释药性能研究
2012-11-01黄思玉吕竹芬陈燕忠林浩杰吴彩珍班俊峰孙美丽
黄思玉 吕竹芬 陈燕忠 林浩杰 吴彩珍 班俊峰 孙美丽
甲基睾酮素,英文名称:Methyltestosterone(MT)中文别名:甲基睾丸素、甲基睾丸酮,是一种人工合成的甾体激素类药物,具有促进男性性器官及副性征的发育成熟、对抗雌激素和促进蛋白质合成与骨质形成等作用[1]。现参照《中国药典》(第2010版)中甲睾酮的含量测定方法[2],采用RPHPLC法测定甲睾酮聚乳酸微球在释放介质中甲睾酮的含量。该法简便、快速、准确、适用于甲睾酮聚乳酸微球释放的质量控制。
1 仪器和试药
1.1 药品与试剂 甲睾酮(珠海远程医药化工有限公司,批号:20091120),甲睾酮对照品(中国药品生物制品检定所,批号:100172-200503),外消旋聚乳酸(Mx=110000,η =0.75,济南岱罡生物技术有限公司),聚乙烯醇(PVA-17s,广州市杰辅贸易有限公司),二氯甲烷、乙醇、十二烷基磺酸钠(广州化学试剂厂),甲醇(色谱纯,广州市铱能色谱材料有限公司),水为纯净水,其他试剂均为分析纯。
1.2 仪器 高效液相色谱仪(Dionex Ultimate 3000 Pump,Ultimate 3000 Photodiode Array Detector,德国 Dionex corp.),KQ-400型超声波清洗器(昆山市超声仪器有限公司),T25分散机(IKA公司),RW25搅拌机(IKA公司),THZ-82恒温水浴振荡器(江苏金坛市宏华仪器厂),HWS24型电热恒温水浴锅(上海一恒科技有限公司),LXJ-IIB离心机(上海安亭科学仪器厂)。
2 方法与结果
2.1 微球的制备 采用乳化-溶剂挥发法制备甲睾酮聚乳酸微球[3]。取适量聚乳酸和甲睾酮溶解于二氯甲烷中,超声3 min,将此溶液滴入PVA水溶液中,高速搅拌(3400 r/min)乳化3 min后,倾入大量蒸馏水中,在30℃继续搅拌(400 r/min)4 h。离心,收集微球,用蒸馏水洗涤,冷冻干燥即得白色粉末状固体微球。
2.2 微球体外释药试验 精密称取载药微球30 mg,置预先处理的透析袋中,加入1 ml释放介质(pH 3.4)扎紧袋两端,悬浮于50 ml具塞离心管中,离心管中加入29 ml释放介质(pH 3.4),将其置恒温水浴振荡器中,于一定时间取样5 ml,并加入5 ml新鲜释放介质保持“漏槽状态”,用高效液相色谱法测定释放介质中甲睾酮的浓度。
释放介质:0.25%SDS-5%乙醇(pH 3.4)缓冲液
介质温度:37±1℃
搅拌速度:100rpm/min
累积释放率=(累积载药量/总载药量)×100%=(∑CiV/总载药量)×100%
Ci-释放各时刻溶液中药物的浓度(μg/ml)
V-释放介质的体积
2.3 微球体外释药量的测定
2.3.1 色谱条件与系统适用性试验 色谱柱:Diamonsil-C18柱(250 mm ×4.6 mm,5 μm);流动相:甲醇-水(72∶28);检测波长 241 nm;流速:1.0 ml/min;进样量:10 μl;柱温:30℃;理论塔板数按甲睾酮峰计算为9352,睾酮峰与甲睾酮峰的分离度R=4.75,符合要求。结果见图1。
2.3.2 线性试验 精密称取经105℃干燥2 h的甲睾酮对照品10 mg置100 ml容量瓶中,加释放介质溶解并稀释至刻度,摇匀,制成100μg/ml的标准液。分别精密量取标准液0.1、0.5、1.0、1.5、2.0、2.5、3.0 ml置 10 ml容量瓶中,加释放介质至刻度,摇匀,即得不同浓度 1、5、10、15、20、25、30 μg/ml对照品溶液,依次进行HPLC分析,按“2.3.1.1”项色谱条件,注入液相色谱仪,记录甲睾酮色谱峰的面积。以峰面积(A)为纵坐标,甲睾酮进样浓度(X)为横坐标,制标准曲线,得回归方程为A=0.485X+0.262(r=0.9999),甲睾酮在1~30 μg/ml浓度范围内线性关系良好。
2.3.3 精密度试验 取低、中、高3种浓度(1、15、30 μg/ml)的甲睾酮对照品溶液,按“2.3.1.1”项色谱条件下连续进样6次,记录各峰面积,计算日内RSD。3种浓度的甲睾酮对照品日内RSD分别为:0.52%,0.37%,0.24%,表明本方法精密度良好。
2.3.4 回收率试验 在释放介质中分别加入一定量的甲睾酮标准液,分别配成高、中、低三种浓度,每个浓度3份,按“2.3.1.1”项色谱条件下进样。结果平均回收率为:100.2%,RSD为1.7%(n=9)见表1。

表1 回收率的结果
2.3.5 MT-PLA-MS释药量的测定 取3份不同批号(批号:20110510、20110512、20110515)的甲睾酮聚乳酸微球,按“2.2”项下进行操作,并分别于 1、2、4、6、8、12、24、48、72、168、336、720、1440、2160 h 取样,测定微球释药量并计算微球累积释药率,微球在0.25%SDS-5%乙醇(pH 3.4)缓冲液中7 d和3个月的累计释药量分别为(41.8±0.1)%和(83.8±0.2)%,表明甲睾酮微球具有良好的缓释性能,绘制曲线见图2;并将数据按零级动力学方程、一级动力学方程、Higuchi动力学方程和双相动力学方程拟合,得拟合优度、数学释药模型,结果见表2。
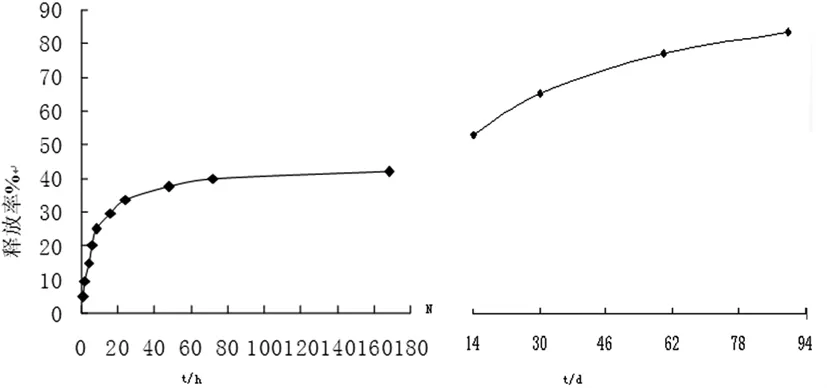
图2 MT-PLA-MS 3个月的体外释放曲线
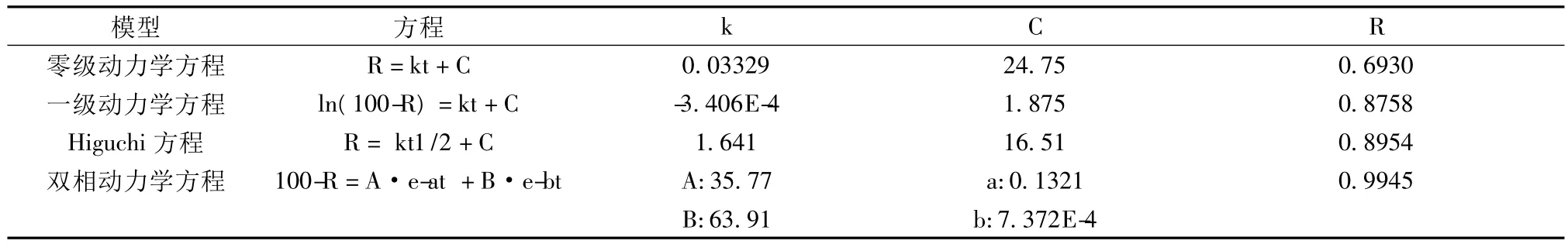
表2 MT-PLA-MS不同动力学释放模型
由表2可见:甲睾酮微球体外释放模型拟合接近程度依次为:双相动力学模型>Higuchi模型>一级模型>零级模型,说明微球的体外释放曲线可用双相动力学模型较好的拟合。
3 讨论
3.1 释放介质的选择[4]甲睾酮为脂溶性药物,不溶于水,溶于醇,实验中分别研究了甲睾酮在模拟人工胃液和人工肠液以及其他缓冲溶液中的溶出情况,在上述溶液中几乎都不溶出,故需加入适当的表面活性剂,来增大药物的溶出,最后选择用含0.25%SDS-5%乙醇(pH 3.4)缓冲液作溶出介质。
3.2 MT-PLA-MS体外释药机理探讨 MT-PLA-MS在最初12 h微球药物释放较快,累积释药率达29.49%,考虑为微球的药物突释作用所致,其后药物释放速度比较稳定,3个月内累积释药率达至83.8%;可能开始时微球的释药方式主要是表面的药物通过扩散方式释药,而后的释药方式主要是释放介质渗透入微球,使其中的药物溶解释放或微球的载体材料发生降解从而释放出药物[5]。因此微球释药呈现先快后慢的现象,具有明显的双相动力学释药特性,有利用甲睾酮发挥药物的疗效,即达到靶位后,较快的释放药物,达到药效浓度,再缓慢释放出剩余药物,维持药效。
[1] 姚莉蓓,冉兰,刘梅妍.HPLC测定甲睾酮喷雾剂中的甲睾酮.华西药学杂志,2008,23(2):235-236.
[2] 中华人民共和国国家药典委员会.中国药典.二部.北京化学工业出版社,2010:161.
[3] Pratap C Naha,Vibhu Kanchan,Amulya K,et al.Evaluation of Parenteral Depot Insulin Formulation using PLGA and PLA Microparticles.Journal of Biomaterials Applications,2009,9(4):309-324.
[4] 肖莉,张韵慧,崔颖,等.尼莫地平聚乳酸缓释微球的制备及其药剂学性质.中国医院药学杂志,2008,28(3):194-198.
[5] 吴珍珍,李馨儒,胡应生,等.辛伐他汀聚乳酸微球的制备及药剂学性质.中国新药杂志,2005,14(11):1312-1315.
