泰和乌骨鸡活性肽对5- 氟尿嘧啶诱导HSF细胞损伤的保护作用
2012-10-25田颖刚王春艳黄宇玫廖春艳乔娟娟
田颖刚,王春艳,黄宇玫,廖春艳,张 盼,朱 胜,乔娟娟
(1.南昌大学食品科学与技术国家重点实验室,江西南昌330047;
2.南昌大学科学技术学院,江西南昌 330029)
泰和乌骨鸡活性肽对5- 氟尿嘧啶诱导HSF细胞损伤的保护作用
田颖刚1,王春艳1,黄宇玫2,廖春艳1,张 盼1,朱 胜1,乔娟娟1
(1.南昌大学食品科学与技术国家重点实验室,江西南昌330047;
2.南昌大学科学技术学院,江西南昌 330029)
目的:用单细胞凝胶电泳技术(SCGE)研究泰和乌骨鸡活性肽对5-氟尿嘧啶(5-FU)损伤细胞DNA的保护作用。方法:传代培养人皮肤成纤维细胞(HSF),随机分为正常对照组,5-FU组,5-FU+泰和乌骨鸡活性肽组。应用MTT法检测细胞存活率,单细胞凝胶电泳法(SCGE)检测5-FU引起HSF细胞DNA损伤程度,羟脯氨酸试剂盒检测细胞培养液中羟脯氨酸含量。结果:与正常对照组比较:5-FU组HSF细胞DNA的损伤程度较严重,且尾长、尾距、Olive尾距和尾部DNA百分含量显著增加(p<0.001),细胞培养液中羟脯氨酸含量显著性减少(p<0.05)。与5-FU组比较,泰和乌骨鸡活性肽组细胞的尾长、尾距、Olive尾距和尾部DNA百分含量均显著性减少(p<0.001),而细胞培养液上清中羟脯氨酸含量升高(p<0.01)。结论:泰和乌骨鸡活性肽对HSF细胞DNA损伤具有保护作用,泰和乌骨鸡活性肽可以剂量依赖性地降低5-FU诱导的HSF细胞DNA的断裂损伤。
泰和乌骨鸡,活性肽,5-氟尿嘧啶,DNA损伤,单细胞凝胶电泳
5-氟尿嘧啶(5-fluorouracil,5-FU)为临床常用的抗代谢类肿瘤治疗药物,因其代谢转化为5-氟脱氧尿嘧啶核甘酸(FDUMP),抑制胸腺嘧啶核苷酸合成酶(TS),从而抑制肿瘤细胞DNA复制合成,造成DNA损伤,从而发挥抗肿瘤作用[1],该过程同样会作用于正常细胞,如抑制成纤维细胞的增殖和胶原的合成,延迟伤口愈合[2-5]。因此需要通过改变给药方式、修饰化疗药物结构或者给予适当的解毒剂配伍等方法来提高5-FU选择性且降低其临床毒副作用。研究表明,应用生长激素、谷氨酰胺能提高吻合口愈合强度,促进术后早期腹腔化疗条件下结肠吻合口愈合[6-7]。泰和乌骨鸡是我国特有的药食两用滋补鸡种,传统中医认为乌骨鸡能补虚劳羸弱,滋阴清热,治消渴心腹痛,益产妇,治女人崩中带下、一切虚损诸病,其临床疗效已被广为证实[8]。本课题组研究证明泰和乌骨鸡活性肽具有非酶糖基化抑制作用[9],良好的抗氧化作用[10]和一定程度的补血作用[11]。本文采用对DNA断裂损伤较敏感的单细胞凝胶电泳技术探讨泰和乌骨鸡活性肽对5-FU诱导人皮肤成纤维细胞DNA损伤的保护作用,以期为乌骨鸡功能活性的研究和临床应用提供一定的理论依据。
1 材料与方法
1.1 材料与仪器
泰和乌骨鸡活性肽 由新鲜的泰和乌骨鸡,经脱毛、去内脏、绞成肉泥,然后采用蛋白酶酶解制得(详见专利[12]);人皮肤成纤维细胞 美国标准菌种收藏所(ATCC)编号为842;胎牛血清 杭州四季青生物工程材料有限公司;DMEM培养基 美国Gibco公司;羟脯氨酸试剂盒 南京建成生物公司;四甲基偶氮唑蓝(MTT) sigma公司;5-氟尿嘧啶 上海旭东海普药业有限公司;胰蛋白酶 北京博大泰克生物基因技术有限责任公司;EDTANa2、Hepes 北京索莱宝科技有限公司;正常熔点琼脂糖、低熔点琼脂糖、溴化乙锭、Tris 生工生物工程(上海)有限公司; 96、6和12孔细胞培养板(平底) 美国Costor。
MK3型酶标仪 上海热电仪器有限公司; IDX-35B型高压灭菌锅 上海申安医疗器械厂;BHC-1300ⅡA/B3型生物安全柜 苏净集团安泰公司; BDS200型倒置显微镜 北京福凯仪器有限公司; WJ-80A-111型二氧化碳培养箱 上海新苗医疗器械制造有限公司;Ti-U型荧光倒置显微镜 日本尼康公司;SIMS00000型Milli-Q50超纯水净化系统
美国Millipore公司;DYY-Ⅲ2型稳压稳流电泳仪、DYCP-31B型电泳槽 北京市六一仪器厂;彗星图象分析软件(Casp-1.2.2)。
1.2 实验方法
1.2.1 人成纤维细胞的培养 将HSF细胞按5×105个/mL接种在DMEM高糖培养基中(pH7.4,含10% FBS、100U/mL青霉素、100μg/mL链霉素、10μmol/mL Hepes缓冲液、2μmol/mL L-谷氨酰胺),二氧化碳培养箱温育(37℃、5%CO2)。细胞为梭型贴壁生长,每2~3d传代1次,取对数生长期细胞用于实验。
1.2.2 5-FU损伤模型建立 取对数生长期HSF细胞以1×105个/孔密度接种于96孔板上,于37℃、5%CO2培养箱中培养24h后,加入5-FU使其终浓度为50、100、200、400、800μg/mL,继续培养24h。培养时间终止后,采用MTT法测定细胞存活率[13],每孔加入5mg/mL的MTT 20μL,温育4h,去除培养液及MTT,每孔加入150μL二甲基亚砜,用酶标仪测定各孔在波长490nm处吸光度。单细胞凝胶电泳法测定HSF细胞DNA损伤。
细胞存活率(%)=(正常组OD值-5-FU组OD值)/正常组OD值×100
1.2.3 实验分组及给药 实验分为5组,分别为正常对照组、5-FU模型组、泰和乌骨鸡活性肽低、中、高剂量组。泰和乌骨鸡活性肽组加入浓度为10、50、250μg/mL泰和乌骨鸡活性肽。正常对照组、5-FU模型组加入等量培养液;于37℃、5%CO2培养箱中培养24h后,泰和乌骨鸡活性肽组和5-FU模型组加入终浓度为100μg/mL 5-FU,正常对照组加入等量的培养液。
1.2.4 MTT法测定HSF细胞存活率 取同代的对数生长期HSF细胞以1×105个/孔密度接种于96孔板上,于37℃、5%CO2培养箱中培养24h后,按照1.2.3实验分组及给药处理。于37℃、5%CO2培养箱中培养24和48h后采用MTT法测定细胞存活率。
1.2.5 单细胞凝胶电泳法检测细胞DNA损伤
1.2.5.1 细胞处理及细胞悬液的制备 取同代的对数生长期HSF细胞以1×105个/孔接种于6孔板上,按1.2.3实验分组及给药处理。于37℃、5%CO2培养箱中培养24h后,去除培养液,4℃ PBS洗一次,加入0.25%胰蛋白酶和 0.02%乙二胺四乙酸二钠(EDTANa2)消化3min,1000r/min离心5min后收集细胞,用PBS重悬,密度为1×105个/mL。
1.2.5.2 制片 单细胞凝胶电泳方法采用Singh等的方法[14]稍加改进后进行。将加热溶解的0.75%正常熔点琼脂糖冷却至45~60℃时,取120μL铺于载玻片上,4℃凝固10min。取25μL单细胞悬液与37℃3倍体积0.75%的低熔点琼脂糖混匀液,铺于第二层胶上,4℃固定10min。
1.2.5.3 电泳 将胶板浸于4℃裂解液(含2.5mmol/mL NaCl,100μmol/mL EDTANa2,10μmol/mL Tris,pH10.0,临用前加10%的DMSO,1%的TritonX-100)中裂解1.5h。取出载玻片用蒸馏水轻柔漂洗2次,以免琼脂糖脱落,然后将胶板浸于4℃电泳缓冲液(1μmol/mL EDTANa2,300μmol/mL NaOH,pH13.0)解螺旋20min,电泳(25V,200mA)20min。
1.2.5.4 中和及染色 电泳结束后,胶板用中和缓冲液(0.4mmol/mL Tris,pH7.5)中和三次,每次5min,中和完全后用2μg/mL的EB 50μL染色1min,蒸馏水脱色10min。以上操作均在4℃暗处进行。
1.2.5.5 结果观察 荧光显微镜10×目镜,20×物镜下观察结果(激发光波长510~560nm)及拍照。每组随机选择100个细胞计数,使用CASP软件测量照片中尾长、尾矩、Olive尾矩等指标以反映细胞DNA的损伤程度。按照Kamer I的方法[15]利用彗星尾长将DNA损伤分为四级:A型(胞核清楚,尾长不超过10μm)、B型(胞核清楚,尾长在10~30μm之间)、C型(胞核荧光强度低,尾长在30~40μm之间)和D型(胞核和慧尾不能区分,尾长超过40μm)。计算公式如下:
尾长=彗星头的右边界到彗星尾部末端的距离
尾距=尾长×尾部DNA百分比
Olive尾距=从头光密度重心到尾光密度重心的距离×尾部DNA百分比。
1.2.6 羟脯氨酸含量的测定及胶原含量的计算 取处于对数生长期的HSF,制成细胞悬液,以1×10个/孔接种于12孔板。按1.2.3实验分组及给药处理,置于37℃、5%CO2培养箱中培养,作用终止时吸取上清液0.5mL测羟脯氨酸含量。具体操作按羟脯氨酸检测试剂盒说明书进行,测定上清液中羟脯氨酸在550nm处的吸光值(A值),并根据公式计算羟脯氨酸含量,间接反映HSF细胞胶原含量。计算公式如下:5
表1 5-FU对HSF细胞DNA损伤的作用(±S,n=100)Table 1 Effect of 5-FU on DNA damage in HSF(±S,n=100)
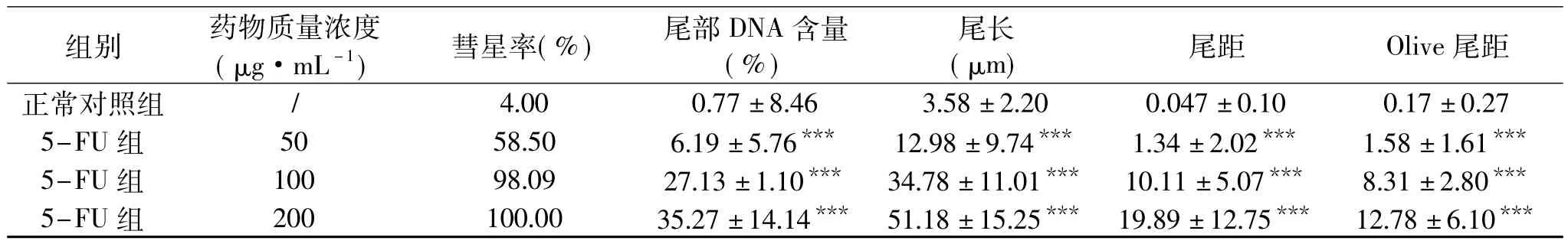
表1 5-FU对HSF细胞DNA损伤的作用(±S,n=100)Table 1 Effect of 5-FU on DNA damage in HSF(±S,n=100)
注:与正常对照组相比,***p<0.001。
组别 药物质量浓度(μg·mL-1) 彗星率(%) 尾部DNA含量(%)尾长(μm) 尾距 Olive 尾距正常对照组 / 4.00 0.77±8.46 3.58±2.20 0.047±0.10 0.17±0.27 5-FU组 50 58.50 6.19±5.76*** 12.98±9.74*** 1.34±2.02*** 1.58±1.61***5-FU组 100 98.09 27.13±1.10*** 34.78±11.01*** 10.11±5.07*** 8.31±2.80***5-FU组 200 100.00 35.27±14.14*** 51.18±15.25*** 19.89±12.75*** 12.78±6.10***
表2 泰和乌骨鸡活性肽对5-FU诱导HSF细胞增殖抑制的影响(±S,n=6)Table 2 Protective effect of bioactive peptides from TBSF on 5-FU-induced inhibition of proliferation in HSF(±S,n=6)
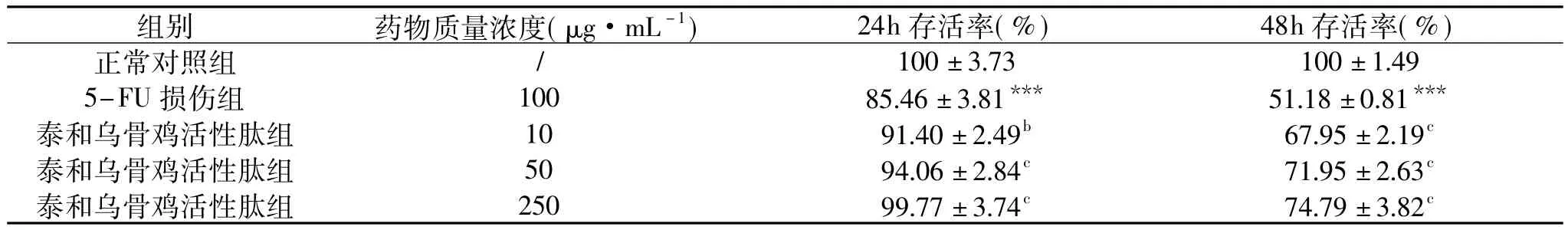
表2 泰和乌骨鸡活性肽对5-FU诱导HSF细胞增殖抑制的影响(±S,n=6)Table 2 Protective effect of bioactive peptides from TBSF on 5-FU-induced inhibition of proliferation in HSF(±S,n=6)
注:与正常对照组相比,*p<0.05,***p<0.001;与5-FU损伤组相比,ap<0.05,bp<0.001;表3~表4同。
组别 药物质量浓度(μg·mL-1) 24h存活率(%) 48h存活率(%) 100±3.73 100±1.49 5-FU损伤组 100 85.46±3.81*** 51.18±0.81***泰和乌骨鸡活性肽组 10 91.40±2.49b 67.95±2.19c泰和乌骨鸡活性肽组 50 94.06±2.84c 71.95±2.63c泰和乌骨鸡活性肽组 250 99.77±3.74c 74.79±3.82正常对照组/ c
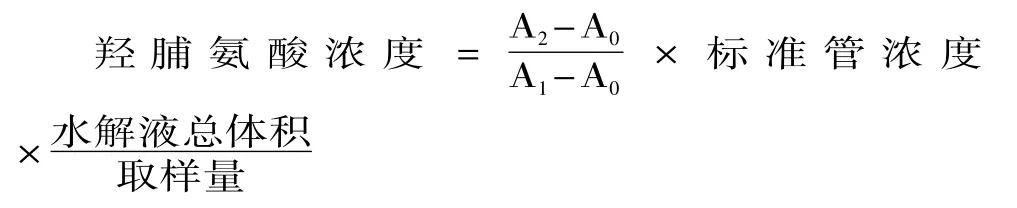
式中:A0为空白管吸光度;A1为标准管吸光度; A2为测定管吸光度。
1.2.7 统计分析 采用SPSS18.0统计软件对数据进行组间t检验。实验数据以平均值±标准差表示。
2 结果与分析
2.1 不同浓度5-FU对HSF细胞存活率的影响
如图1所示,不同浓度的5-FU作用于HSF细胞24h后,随着作用浓度增加细胞存活率与正常对照组相比显著降低。浓度50、100μg/mL作用细胞存活率与正常对照组有显著变化(p<0.01),但细胞存活率都在80%以上,浓度为大于等于200μg/mL 5-FU已出现明显的细胞毒性,细胞存活率为小于75%。由于单细胞凝胶电泳要求细胞存活率应在80%以上,因此选用浓度50、100、200μg/mL的5-FU筛选单细胞凝胶电泳最适作用浓度。
2.2 不同浓度5-FU对HSF细胞DNA损伤作用
如表1所示,不同浓度的5-FU作用HSF细胞24h后,与正常组比较,5-FU的各剂量组均可导致HSF细胞DNA出现不同程度的损伤,随着5-FU质量浓度增大,彗星率、尾长、尾距、Olive尾距和尾部DNA含量显著增加(p<0.001)。50μg/mL实验组对HSF细胞彗星率只有58.50%,属于B型损伤,该损失比较轻微不适合作为单细胞凝胶电泳模型作用浓度。100μg/mL实验组对 HSF细胞彗星率为98.09%,属于C型损伤。200μg/mL实验组对HSF细胞彗星率100%,且为D型损伤,对细胞的损伤非常严重,凋亡细胞比较多。故采用 100μg/mL的5-FU作为HSF细胞损伤模型。

图1 5-FU对HSF细胞存活率的影响(±S,n=6)Fig.1 Effect of 5-FU on HSF survival(±S,n=6)
2.3 泰和乌骨鸡活性肽对5-FU抑制HSF细胞增殖影响
如表2所示,泰和乌骨鸡活性肽对5-FU诱导HSF存活率降低具有保护作用。与对照组比较,5-FU组可显著性抑制HSF细胞的增长(p<0.001),与5-FU组比较,泰和乌骨鸡活性肽组细胞存活率具有显著性差异(p<0.05),且当5-FU作用48h时泰和乌骨鸡活性肽组与5-FU组相比具有极显著性差异(p<0.001),表明泰和乌骨鸡活性肽能抑制5-FU诱导的HSF存活率下降。
2.4 泰和乌骨鸡活性肽对5-FU所致HSF细胞DNA损伤保护作用
如表3所示,不同浓度的泰和乌骨鸡活性肽均能显著降低5-FU对HSF细胞DNA损伤作用,其中在10~250μg/mL浓度范围内,随着泰和乌骨鸡活性肽浓度的增加,抗损伤作用加强,泰和乌骨鸡活性肽组细胞的彗星率、尾长、尾距、Olive尾距和尾部DNA含量与5-FU组相比具有显著性差异(p<0.001)。与空白对照组相比,250μg/mL泰和乌骨鸡活性肽作用组没有显著性差异,表明该浓度下,泰和乌骨鸡活性肽可完全对抗5-FU诱导的DNA损伤。
表3 泰和乌骨鸡活性肽对5-FU诱导HSF细胞DNA损伤的保护作用(±S,n=100)Table 3 Protective effect of bioactive peptides from TBSF on 5-FU-induced DNA damage in HSF(±S,n=100)
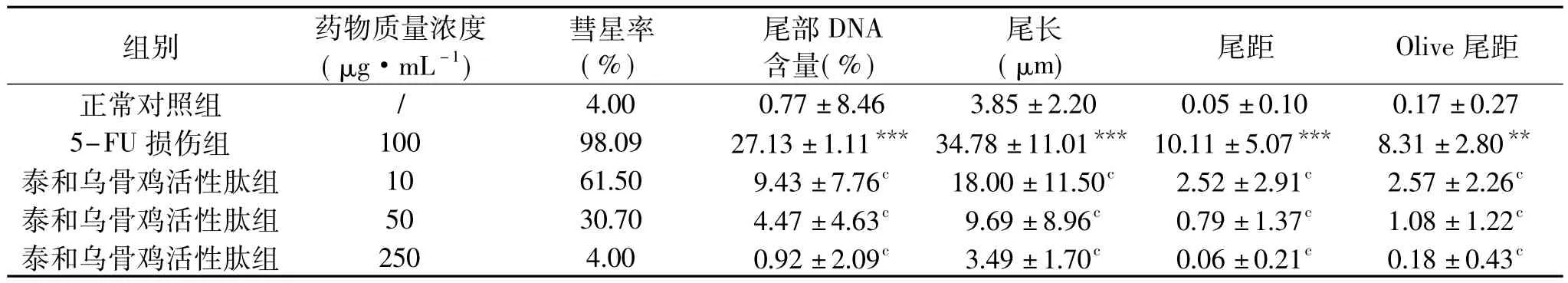
表3 泰和乌骨鸡活性肽对5-FU诱导HSF细胞DNA损伤的保护作用(±S,n=100)Table 3 Protective effect of bioactive peptides from TBSF on 5-FU-induced DNA damage in HSF(±S,n=100)
组别 药物质量浓度(μg·mL-1)彗星率(%)尾部DNA含量(%)尾长(μm) 尾距 Olive 27 5-FU损伤组 100 98.09 27.13±1.11*** 34.78±11.01*** 10.11±5.07*** 8.31±2.80**泰和乌骨鸡活性肽组 10 61.50 9.43±7.76c 18.00±11.50c 2.52±2.91c 2.57±2.26c泰和乌骨鸡活性肽组 50 30.70 4.47±4.63c 9.69±8.96c 0.79±1.37c 1.08±1.22c泰和乌骨鸡活性肽组 250 4.00 0.92±2.09c 3.49±1.70c 0.06±0.21c 0.18±0.43尾距正常对照组 / 4.00 0.77±8.46 3.85±2.20 0.05±0.10 0.17±0.c
表4 泰和乌骨鸡活性肽对5-FU抑制HSF细胞合成羟脯氨酸和胶原含量的保护作用(±S,n=3)Table 4 Protective effect of bioactive peptides from TBSF on 5-FU-induced inhibition of hydroxyproline and collagen synthesis in HSF(±S,n=3)
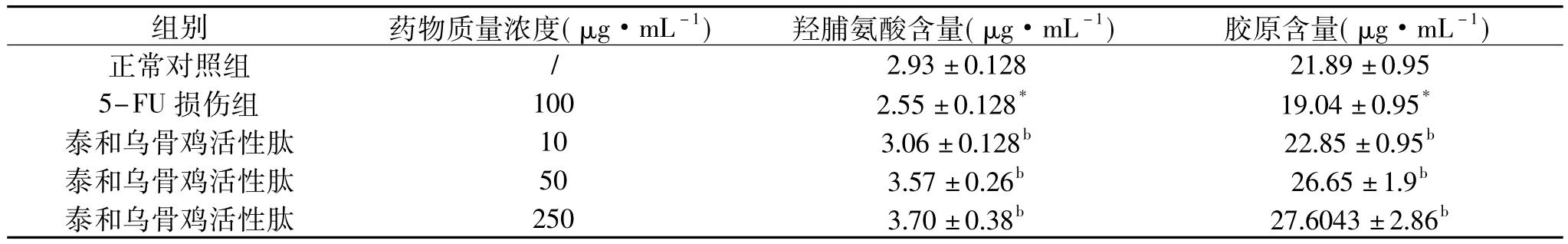
表4 泰和乌骨鸡活性肽对5-FU抑制HSF细胞合成羟脯氨酸和胶原含量的保护作用(±S,n=3)Table 4 Protective effect of bioactive peptides from TBSF on 5-FU-induced inhibition of hydroxyproline and collagen synthesis in HSF(±S,n=3)
组别 药物质量浓度(μg·mL-1) 羟脯氨酸含量(μg·mL-1) 胶原含量(μg·mL-1) 2.93±0.128 21.89±0.95 5-FU损伤组 100 2.55±0.128* 19.04±0.95*泰和乌骨鸡活性肽 10 3.06±0.128b 22.85±0.95b泰和乌骨鸡活性肽 50 3.57±0.26b 26.65±1.9b泰和乌骨鸡活性肽 250 3.70±0.38b 27.6043±2.86正常对照组/ b
制备好的凝胶片在荧光显微镜下观察时,可见DNA被EB染成红色,未发生DNA断裂的细胞表现为一圆形类核,即彗星头部,荧光强度均匀,边缘整齐(图2(a)),正常组未受5-FU损伤的HSF细胞成圆形亮团;而发生DNA断裂的细胞则表现为断片向阳极方向迁移,形成彗星样的拖尾(图2(b)),5-FU组的HSF细胞在5-FU作用下,DNA分子受损严重,呈明显的彗星样变化。而预先应用250μg/mL泰和乌骨鸡活性肽处理后的高剂量实验组的HSF细胞DNA分子完整,影像与正常对照组相似。应用10、50μg/mL的泰和乌骨鸡活性肽的低、中剂量组的HSF细胞虽仍有彗星样的形态,但其尾迹也较5-FU组短且呈现一定的量效关系。
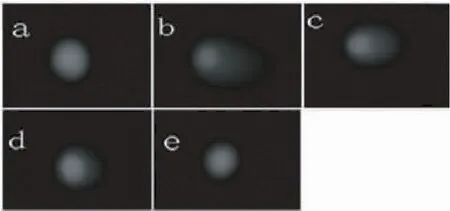
图2 泰和乌骨鸡活性肽对5-FU诱导HSF细胞DNA损伤保护作用的彗星图形(×200)Fig.2 Comet picture of the protective effect of bioactive peptides from TBSF on 5-FU-induced DNA damage in HSF(×200)
2.5 泰和乌骨鸡活性肽对5-FU诱导HSF细胞合成羟脯氨酸和胶原的影响
如表4所示,与正常组相比,5-FU损伤组可以显著抑制羟脯氨酸的合成(p<0.05),不同浓度的泰和乌骨鸡活性肽均能降低5-FU的抑制作用,与5-FU损伤组相比均可显著增加HSF细胞培养液中羟脯氨酸的含量(p<0.01)。表明泰和乌骨鸡活性肽在10~250μg/mL浓度范围内可以促进HSF细胞分泌羟脯氨酸。
3 讨论
目前直接或间接测定DNA损伤常用技术有单细胞凝胶电泳、环境诱变物短期筛选实验(SOS/umu实验)、微核实验(MN)和姐妹染色体交换实验(SCE)等[16]。单细胞凝胶电泳又称为彗星实验,是近年来发展起来的一种在单细胞水平上检测真核细胞DNA损伤的方法[17]。该方法具有所需样品量少,简便,快速,无需放射性标记等优点,广泛地应用于DNA放射损伤、DNA剪切损伤、DNA交联的检测、药物的毒性评价、细胞凋亡鉴定等工作中[18-20]。
尽管单细胞凝胶电泳已被应用20多年,但其检测单个细胞DNA损伤的确切机理还不清楚,一般认为真核细胞的DNA分子量较大,DNA呈负超螺旋结构附着在核基质上。当各种内源性和外源性DNA损伤因子诱发细胞DNA链断裂时,DNA的超螺旋结构受到破坏,在碱处理和碱性电解质的作用下,DNA发生解螺旋,损伤的DNA断链及片段被释放出来,由于这些DNA的分子量很小,所以在电泳过程中会离开核DNA向阳极移动,因而形成了彗星的尾部,而较大的一些碎段位置则靠近细胞核,因而形成彗星的头部。而未损伤的细胞,其核DNA仍停留在核基质中,经荧光染色后呈现圆形的荧光团,无拖尾现象。在一定条件下,彗星尾长和DNA含量分布与DNA损伤程度呈线性相关,因此尾矩被作为SCGE定量分析的主要依据[21]。本研究以HSF细胞为实验对象,以5-FU作为DNA攻击剂,造成HSF细胞DNA损伤。从表3和图2可以看出,正常对照组细胞成圆形,没有拖尾现象,5-FU组细胞呈现明显的彗星样,而泰和乌骨鸡活性肽预处理组随着药物浓度的增加,出现彗尾的细胞数越来越少,细胞彗尾越来越短,直至没有。提示泰和乌骨鸡活性肽对5-FU造成的HSF细胞损伤有一定的保护作用。
胶原是真皮细胞间质中的主要有形成分,由人皮肤成纤维细胞产生,对维持皮肤厚度、张力、缓冲外界创伤有重要作用。羟脯氨酸在胶原蛋白中具有高度特异性且含量稳定,其含量约为胶原蛋白的13.4%,在弹力纤维中含量甚微,而其它蛋白中不存在,因此羟脯氨酸的含量可大致反映胶原蛋白的含量。本研究发现与正常对照组HSF细胞比较,5-FU组HSF细胞增殖能力明显减退,胶原合成能力降低。泰和乌骨鸡活性肽在10~250μg/mL浓度范围内可促进HSF细胞增殖,增加胶原的合成,且在该剂量范围内呈量效关系。因此推测泰和乌骨鸡活性肽对HSF胶原合成影响的原因为:a.通过改变HSF的数量,促进HSF增殖从而提高胶原的合成。b.泰和乌骨鸡活性肽改变了HSF细胞某些生物学特性,提高了单个HSF细胞的胶原合成能力。
本文研究结果表明5-FU可显著性抑制HSF细胞的增殖,造成HSF细胞DNA的损伤。然而在5-FU作用体系中加入泰和乌骨鸡活性肽后,MTT法对细胞存活率的测定表明泰和乌骨鸡活性肽对5-FU诱导HSF细胞增殖抑制具有显著的保护作用,单细胞凝胶电泳结果显示泰和乌骨鸡活性肽组细胞彗星尾长、尾矩、Olive尾距和尾部DNA百分含量与5-FU组比较明显减少,泰和乌骨鸡活性肽可以有效地减少5-FU引起的HSF细胞DNA的断裂损伤和提高HSF细胞分泌胶原蛋白的能力。综上所述,体外实验表明泰和乌骨鸡活性肽可以有效对抗细胞DNA损伤,其作用机理还有待于进一步的研究。
[1]LONGLEY DB,HARKIN DP,JOHNSTON PG.5-flurouracil: mechanisms of action and clinical strategies[J].Nature Review Canner,2003(3):330-338.
[2]FERGUSON MK.The effect of antineoplastic agents on wound healing[J].Surgery,Gynecology&Obstetrics,1982,154(3): 421-429.
[3]SHAPIRO MS,THOFT RA,FRIEND J,et al.5-Fluorouracil Toxicity to the Ocular Surface Epithelium[J].Investigative Ophthalmology&Visual Science,1985,26(4):580-583.
[4]MOHAY J,MCLAUGHIN BJ.Corneal endothelial wound repair in normal and mitotically inhibited cultures[J].Graefe’s Arch Clin Exp Ophthalmol,1995,233(11):727-736.
[5]YILDIZKH,GEZEN F,ISM,etal.MitomycinC,5-fluorouracil,and cyclosporine A prevent epidural fibrosis in an experimental laminectomy model[J].European Spine Journal,2007,16(9):1525-1530.
[6]张松岩,曲宏岩.生长激素对术后早期腹腔化疗下结肠吻合口愈合的影响[J].哈尔滨医科大学学报,2008,42(3): 271-273.
[7]张松岩,徐海涛,肖敏,等.谷氨酰胺对术后早期腹腔化疗的结肠吻合口愈合的影响[J].实用肿瘤学杂志,2009,23(3): 235-237.
[8]田颖刚,谢明勇,王维亚,等.乌骨鸡鸡肉中肌肽的鉴定与测定[J].分析实验室,2007,26(1):1-8.
[9]吴光杰,田颖刚,谢明勇,等.乌骨鸡活性肽对体外非酶糖基化的抑制作用[J].南昌大学学报:理科版,2007,31 (5):456-45.
[10]林霖,田颖刚,谢明勇,等.乌骨鸡活性肽组成成分及体外抗氧化活性研究[J].食品科学,2007,28(10):41-45.
[11]王勇,刘建华,田颖刚,等.谢明勇泰和乌骨鸡活性肽补血作用研究[J].食品科学,2010(21):340-343.
[12]田颖刚.一种用于化疗减毒增效的乌骨鸡肽的制备方法及其应用[P].中国专利:201210097950.1,2012-04-09.
[13]司徒镇强,吴军正.细胞培养[M].西安:世界图书出版公司,2004:250-252.
[14]朱文文,王晓涛.DNA损伤检测-单细胞凝胶电泳技术的研究[J].微量元素与健康研究,2007,24(3):6-7.
[15]KAMER I,RINKEVICH B.In vitro application of the comet assay for aquatic genotoxicity:considering a primary culture versus a cell line[J].Toxicol In Virto,2002,16(2):177-184.
[16]马爱国,臧金林,宋风荣,等.SCGE,SCE和染色体畸变分析法用于DNA损伤与修复检测的对比研究[J].癌变.畸变.突变,2001,13(3):155-157.
[17]OLIVE PL,WLODEK D,BANáTH JP.DNA double-strand breaks measured in individual cells subjected to gelelectrophoresis[J].Cancer Res,1991,51(17):467l-4676.
[18]OLIVE PL.Impat of the comet assay in radiobillogy[J].Mutat RES,2009,681(1):13-23.
[19]MCKENNA DJ,MCKEOWN SR,MCKELVEY-MARTN VJ.Potential use of the comet assay in the clinical management of cancer[J].Mutagenesis,2008,23(3):183-190.
[20]薛同敏,郭忠.单细胞凝胶电泳技术应用进展[J].西北民族大学学报,2011,32(3):70-73.
[21]COLLINS AR,OSCOZ AA,BRUNBORG G,et al.The comet assay:topical issues[J].Mutagenesis,2008,23(3):143-151.
Protective effect of bioactive peptides from taihe black-bone silky fowls on human skin fibroblasts injured by 5-fluorouracil
TIAN Ying-gang1,WANG Chun-yan1,HUANG Yu-mei2,LIAO Chun-yan1,ZHANG Pan1,ZHU Sheng1,QIAO Juan-juan1
(1.State Key Laboratory of Food Science and Technology,Nanchang University,Nanchang 330047,China;
2.College of Science and Technology,Nanchang University,Nanchang 330029,China)
Objective:A DNA injury model was established by using 5-fluorouracil(5-FU)in this study.Methods:A series of experiments(MTT assay,single cell gel electrophoresis(SCGE),and hydroxyproline assay kits)were designed to investigate the effect of bioactive peptides from Taihe Black-Bone Silky Fowl(TBSF)on Human Skin Fibroblasts(HSF)against 5-FU-induced DNA damage.Cultured HSF were randomly divided into three groups:the control group,5-fluorouracil group and 5-fluorouracil+bioactive peptides from TBSF.Cell viability was measured by MTT assay,DNA damage was detected by SCGE assay,and hydroxyproline levels in HSF culture medium were measured by hydroxyproline assay kits.Results:compared with the control group,5-FU group exacerbated the DNA damage,in which the tail length,the tail moment,the Olive tail moment,and the tail DNA content significantly increased(p<0.001),whereas the content of hydroxyproline in HSF culture medium significantly decreased(p<0.05).Compared with 5-FU group,Bioactive peptides from TBSF attenuated 5-FU-induced DNA damage,in which the tail length,the tail moment,the Olive tail moment and the tail DNA content significantly decreased(p<0.05),whereas the content of hydroxyproline increased dramatically(p<0.01).Conclusion:Bioactive peptides from TBSF can protect HSF against 5-FU-induced DNA damage in a dose-dependent manner.
black-bone silky fowl;bioactive peptides;5-fluorouracil;DNA damage;single cell gel electrophoresis
TS201.4
A
1002-0306(2012)21-0356-05
2012-04-23
田颖刚(1972-),男,博士,副研究员,研究方向:食品化学与营养。
江西省青年科学家培养计划(2010)资助项目(赣科发计字[2010]209号)。
