(S)-2-苄氧基丙醛的合成及结构表征
2012-10-19徐东超曲敏杰姜殿平李成斌阮久勇
徐东超,曲敏杰,姜殿平,李成斌,郭 静,阮久勇
(1大连工业大学纺织与材料工程学院,辽宁 大连 116034;2大连奇凯医药科技有限公司,辽宁 大连 123000)
研究开发
(S)-2-苄氧基丙醛的合成及结构表征
徐东超1,曲敏杰1,姜殿平2,李成斌2,郭 静1,阮久勇1
(1大连工业大学纺织与材料工程学院,辽宁 大连 116034;2大连奇凯医药科技有限公司,辽宁 大连 123000)
(S)-2-苄氧基丙醛是有机合成及制药的重要中间体,本文以(S)-乳酸乙酯为原料,经四氢吡咯胺化、氯化苄醚化、红铝还原反应合成了(S)-2-苄氧基丙醛,考察了胺化的反应时间、反应温度和原料的摩尔比对反应收率的影响。结果表明:当胺化反应时间为75 h,最佳的反应温度为25 ℃,四氢吡咯与(S)-乳酸乙酯的摩尔比为1.4∶1时,胺化反应收率为94%,三步总收率为61.8%,采用GC-MS、IR、1H NMR表征确定了产物结构,研究结果为(S)-2-苄氧基丙醛的工业化生产奠定了基础。
(S)-乳酸乙酯;胺化反应;(S)-2-苄氧基丙醛;合成
碳青霉烯类抗生素为迄今抗菌谱最广、抗菌活性较强的一类抗生素,对多种β-内酰胺酶高度稳定,对头孢菌素耐药菌仍可发挥优良抗菌作用。细菌对该类药物不存在交叉耐药性,因而对革兰氏阳性菌、阴性菌及厌氧菌都有强大的抗菌活性[1-3]。(S)-2-苄氧基丙醛不仅是合成碳青霉烯类药物的关键化合物,同时又是有机合成和医药工业的重要中间体,因此,这类化合物的合成研究越来越受到人们的重视[4-7]。
目前传统的(S)-2-苄氧基丙醛的合成方法主要有以下两种:其一,以(S)-乳酸乙酯为原料在苄基化试剂氧化银的作用下直接苄基化生成(S)-2-苄氧基-丙酸乙酯,经四氢锂铝还原为(S)-2-苄氧基丙醇,(S)-2-苄氧基丙醇再氧化成(S)-2-苄氧基丙醛,该制备方法中所用原料氧化银和四氢锂铝价格昂贵,成本太高;其二,采用二甲胺将(S)-乳酸乙酯的酯基酰胺化,再与一般的苄基化试剂氢氧化钠或氢化钠反应合成(S)-2-苄氧基丙醛,但该方法所用原料中的二甲胺沸点过低,室温下为气态,要求反应装置必须密封,反应压力较高且操作危险性大[8-11]。本论文采用四氢吡咯代替二甲胺与(S)-乳酸乙酯反应,再经氯化苄醚化、红铝还原反应等3步反应完成了(S)-2-苄氧基丙醛的合成,同时对样品进行了红外和核磁共振波谱分析。其中四氢吡咯与(S)-乳酸乙酯的胺化反应条件温和,在室温下即能发生反应,并有效地降低了生产成本,更适于产品工业化,具有良好的实际应用和开发价值。反应原理如下:

1 实验部分
1.1 试剂与仪器
甲苯为工业品;四氢吡咯(化学纯),上海晶纯试剂有限公司;(S)-乳酸乙酯(化学纯),上海晶纯试剂有限公司;氢化钠,分析纯,天津光复科技发展有限公司;氯化苄,分析纯,天津光复科技发展有限公司;36%~38%盐酸,分析纯,天津市凯信化学工业有限公司;红铝-甲苯溶液,优级纯,罗门哈斯中国公司上海代理处;异丙醇,分析纯,天津科密欧化学试剂有限公司。
气相色谱/质谱联用仪,6890/5975C,美国安捷伦公司;精密增力电动搅拌器,JJ-1,江苏金坛市江南仪器厂;旋转蒸发仪,XMTF-6000,上海申生科技有限公司;数显智能油锅,ZKYY,巩义市予华仪器有限责任公司;核磁共振波谱仪,INOVA 400,美国Varian公司;红外光谱仪,SpectrumOne-B,美国泊金埃尔默公司。
1.2 合成方法
1.2.1 (S)-N,N-四亚甲基乳酸酰胺(产物1)的合成
将四氢吡咯100 g滴加到装有(S)-乳酸乙酯118 g的反应釜中,保温搅拌75 h,加入甲苯减压蒸出过量的四氢吡咯和乙醇,得到浅褐色油状液体(S)-N,N-四亚甲基乳酸酰胺138 g,收率为94%。
1.2.2 (S)-N,N-四亚甲基-2-苄氧基乳酸酰胺(产物2)的合成
控制釜温0 ℃,将(S)-N,N-四亚甲基乳酸酰胺138 g的甲苯溶液缓慢滴加到装有氢化钠44 g和甲苯435 g的反应釜中,剧烈搅拌4.5 h,然后滴加氯化苄128 g,搅拌15 h。酸洗反应液,甲苯萃取水层,用水洗有机层,合并有机层蒸出甲苯,然后加入石油醚重结晶、抽滤,得到浅黄色晶体200.4 g,收率为91.3%。
1.2.3 (S)-2-苄氧基丙醛(产物3)的合成
氮气保护下,向反应釜中加入(S)-N,N-四亚甲基-2-苄氧基乳酸酰胺甲苯溶液684 g,-10 ℃滴加红铝243.5 g和甲苯的稀释液,保温搅拌48 h,控制釜温-5~0 ℃滴加异丙醇,搅拌30 min,酸洗溶液,减压蒸馏,得到无色油状液体101.7 g,收率为72.1%,3步总收率为61.8%。
1.2.4 分析测试
采用气相色谱-质谱(GC-MS)联用仪分别测定了叔丁基苯基碳酸酯和肼基甲酸叔丁酯的出峰时间和离子的准确质量(色谱柱30 m×0.32 mm×0.25 μm;汽化温度260 ℃;起始温度80 ℃,12 ℃/min,程序升温到260 ℃;固定相聚硅氧烷;质谱70 eV),计算方法采用面积归一法定量,未考虑校正因子。
化合物1 MS(m/z):143 (M+),128,98,71,55,30。RT=9.540 min.
化合物2 MS(m/z):234(M+),188,160,142,127。RT=14.838 min
化合物3 MS(m/z):163(M+—1),135,107,91,77。RT=8.320 min
2 结果与讨论
在(S)-2-苄氧基丙醛制备过程中,主要考察了胺化反应中反应时间、反应温度和摩尔比对(S)-N,N-四亚甲基乳酸酰胺收率的影响。
2.1 反应温度对(S)-N,N-四亚甲基乳酸酰胺收率的影响
表1为反应时间为75 h,四氢吡咯和(S)-乳酸乙酯的摩尔比为1.4∶1,考察反应温度对(S)-N,N-四亚甲基乳酸酰胺收率的影响。

表1 反应温度对(S)-N,N-四亚甲基乳酸酰胺收率的影响
由表1可知,随着反应温度越高,收率先增大后减小。当反应温度高于25 ℃时,反应中的焦油逐渐增多,这可能是当反应温度高时,原料和生成物中含有的羟基相互聚合生成了大分子化合物。
2.2 反应时间对(S)-N,N-四亚甲基乳酸酰胺收率的影响
表2为反应温度为25 ℃、四氢吡咯和(S)-乳酸乙酯的摩尔比为1.4∶1时,反应时间对(S)-N,N-四亚甲基乳酸酰胺收率的影响结果。
由表2可见,随着反应时间的增加,产物的收率逐渐提高,当反应达到75 h时,收率达到94%,再延长反应时间,产物的收率提高幅度不大。因此,反应时间为75 h比较合理。
2.3 物料投料比对(S)-N,N-四亚甲基乳酸酰胺产物收率的影响
表3为反应温度为25℃、反应时间为75 h时,物料投料比对(S)-N,N-四亚甲基乳酸酰胺收率的影响结果。

表2 反应时间对(S)-N,N-四亚甲基乳酸酰胺收率的影响

表3 物料投料比对(S)-N,N-四亚甲基乳酸酰胺收率的影响
由表3可知,随着四氢吡咯的增加,产物的收率逐渐增加,当物料投料n(四氢吡咯)∶n[(S)-乳酸乙酯]= 1.4∶1时,再提高四氢吡咯的量,产物收率提高的幅度较小,并且会增加反应成本。因此,n(四氢吡咯)∶n[(S)-乳酸乙酯]= 1.4∶1较合理。
2.4 (S)-2-苄氧基丙醛的红外分析
反应产品经处理提纯后进行红外光谱分析,见图1,解析红外光谱图可知:在1454 cm-1处存在苯环骨架振动峰,在698 cm-1、738 cm-1两处存在苯环—CH面外弯曲振动峰,由此可证明苯环是单取代;在1094 cm-1处存在醚键C—O—C的伸缩振动峰;在1733 cm-1处存在羰基的伸缩振动峰;在1374 cm-1处存在的峰为C—H伸缩振动的倍频峰与羰基的C—H伸缩振动产生的基频费米共振的结果;在2870 cm-1处为甲基的伸缩振动峰。以上分析表明产物谱图中有(S)-2-苄氧基丙醛的特
征峰[12-13]。
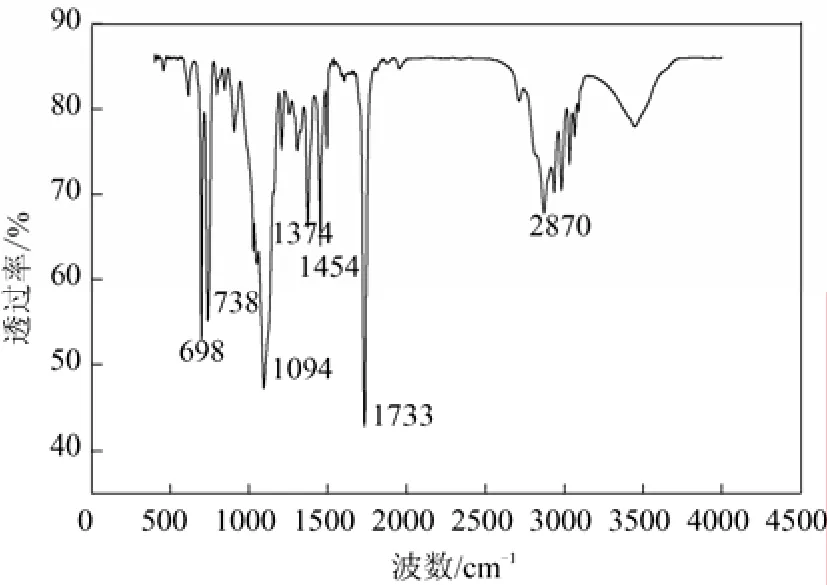
图1 (S)-2-苄氧基丙醛的红外谱图
2.5 (S)-2-苄氧基丙醛的核磁分析
产物的核磁分析见图2,由图2可知:δ=1.26附近的二重峰为3位置上氢的偶合吸收峰,δ=3.82附近的多重峰为2位置上氢的偶合吸收峰,δ=9.58附近的二重峰为1位置上氢的偶合吸收峰,δ=4.56附近的单峰为4位置上的氢,δ=7.24~7.31附近的峰为苯环5、6、7、8、9位置上的氢,结合红外谱图和气质分析表明该化合物为(S)-2-苄氧基丙醛。
3 结 论
以(S)-乳酸乙酯为原料,经四氢吡咯胺化、氯化苄醚化、红铝还原反应合成了(S)-2-苄氧基丙醛,当胺化反应时间为75 h、最佳的反应温度为25 ℃、四氢吡咯与(S)-乳酸乙酯的摩尔比为1.4∶1时,胺化反应收率最高达到94%,合成(S)-2-苄氧基丙醛总收率为61.8%。虽然反应时间较长,但总体反应对设备及温度均无非常苛刻要求,一个反应釜即能满足生产要求,适于工业化生产,颇具开发价值。
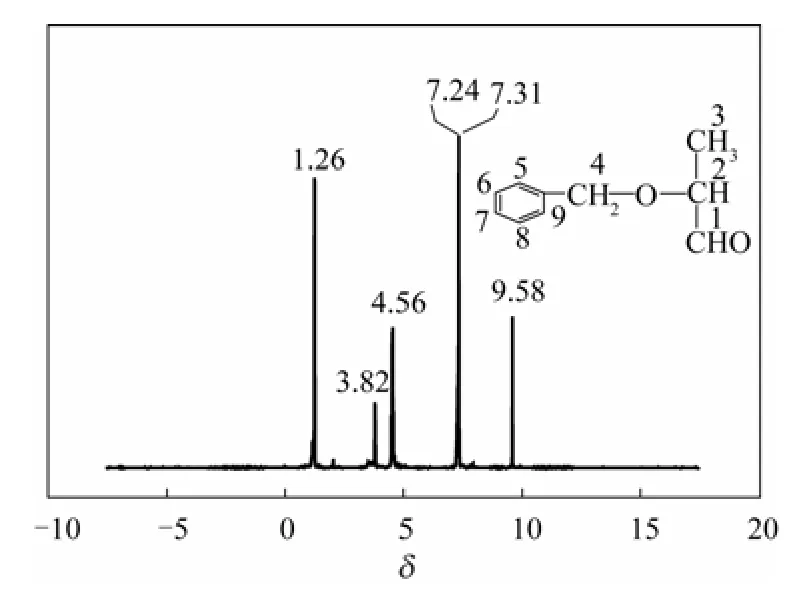
图2 (S)-2-苄氧基丙醛的1H NMR谱图
[1] 王辉,郭萍,孙宏莉,等. 碳青霉烯类耐药的不动杆菌分子流行病学及其泛耐药的分子机制[J]. 中华检验医学杂志,2006,29(12):1066-1073.
[2] Schwaber M J,Klarfeld-Lidji S,Navon-Venezia S. Predictors of carbapenem-resistant Klebsiella pneumoniae acquisition among hospitalized adults and effect of acquisition on mortality[J]. Antimicrobial Agents and Chemotherapy,2008,52(3):1028-1033.
[3] Fernando G Pasteran,Luis Otaegui,Leonor Guerriero,et al. Klebsiella pneumoniae carbapenemase:2,Buenos aires,argentina[J]. Emerg. Infect. Dis.,2008,14(7):1178-1180.
[4] Hans Gunter Aurich. Highly diastereoselective formation of bicyclic compounds by intramolecular cycloaddition of chiral thiaalkenyl nitrones[J]. Tetrahedron,1994,50(13):3929-3942.
[5] 范琦,程秀华,李美琴. 2-(3-苄基苯基)丙醛合成工艺的改进[J].合成化学,2002(5):468-470.
[6] Christophe Dubost,Bernard Leroy. Stereoselective synthesis of functionalised triol units by SnCl4promoted allylation of a-benzyloxyaldehydes:Crucial role of the stoichiometry of the Lewis acid[J]. Tetrahedron,2004,60:7693-7704.
[7] Sandip K Nayak,Lambertus Thijs,Binne Zwanenburg. Baylis-Hillman reaction of N-trityl aziridine-2-(S)-carboxaldehyde [J]. Tetrahedron,1999,40(5):981-984.
[8] Gianfranco Favi,Gianluca Giorgi. Regioselective synthesis of spiro-cyclpropanated 1-aminopyrrol-2-ones by Bi(OTf)3-catalyzed one-pot ‘Mukaiyama-Michael addition/cyclization/Ring-contraction’rections of 1,2-bis(trimethylsilyloxy)cyclobutene with 1,2-diaza -1,3-butadienes[J]. Tetrahedron,2009,65:5456-5461.
[9] Reda Mhidia,Aurlie Vallin,Nathalie Ollivier,et al. Synthesis of peptide-protein conjugates using N-succinimidyl carbamate chemistry[J]. Bioconjugate Chem.,2010,21(2):219-228.
[10] Varelis P,Johnson B L. Preparation of optically active (S)-2-(benzyloxy)propanal[J]. Australian Journal of Chemistry,1995,48(10):1775-1779 .
[11] Yuko Kobayashi. An improved synthetic method of (S)-2-alkoxypropanals from ethyl (S)-lactate[J]. Chem. Soc. Jpn.,1989,62(9):3038-3040.
[12] 谢品曦. 红外光谱在有机化学和药物化学中的应用[M]. 北京:科学出版社,1987.
[13] 薛松. 有机结构分析[M]. 合肥:中国科学技术大学出版社,2005.
Synthesis and characterization of(S)-2-benzyloxyl propanal
XU Dongchao1,QU Minjie1,JIANG Dianping2,LI Chengbin2,GUO Jing1,RUAN Jiuyong1
(1School of Textile and Material Engineering,Dalian Polytechnic University,Dalian 116034,Liaoning,China;2Dalian Qi-Chem Pharmaceutical Technology Company Limited,Dalian 123000,Liaoning,China)
Vanadium redox flow battery is a highly efficient storage energy installs. The electrolyte influence the battery capacity directly. (S)-2 - benzyloxy propanal was synthesized by the amination of pyrrolidine,the etherification of benzyl chlorine and sodium bisaluminiumhydride with ethyl(S)-lactate as raw material. The reaction time ,the reaction temperature and the mole ratio of raw material in the process of amination were investigated. The results showed that the yield of amination reaction was about 94% when amination reaction time was 72 h,the reaction temperature was 25 ℃ and the mole ratio of pyrrolidine to ethyl(S)-lactate was 1.4∶1. The overall yield was about 61.8%. The product structure was characterized and confirmed by GC-MS,IR and1H NMR. The results provided important theoretical base for the industrial production of(S)-2 - benzyloxy propanal.
ethyl(S)-lactate;amination reaction;(S)-2-benzyloxyl propanal;synthesis
TQ 460.3
A
1000-6613(2012)06-1318-04
2012-01-05;修改稿日期:2012-02-17。
徐东超(1984—),男,硕士研究生。E-mail dongchaoxx@126.com。联系人:曲敏杰,教授,主要从事高分子改性、有机中间体合成研究。E-mail minjiequ2005@126.com。
