R-(+)-α-硫辛酸的合成工艺
2012-10-19冷一欣牛锦森黄春香
冷一欣,牛锦森,黄春香
(常州大学石油化工学院,江苏 常州 213164)
研究开发
R-(+)-α-硫辛酸的合成工艺
冷一欣,牛锦森,黄春香
(常州大学石油化工学院,江苏 常州 213164)
以6,8-二氯辛酸为原料,S-(-)-α-苯乙胺为拆分剂进行拆分反应得到R-(+)-6,8-二氯辛酸;经酯化制得R-(+)-6,8-二氯辛酸乙酯;后经硫化水解一步合成R-(+)-α-硫辛酸。考察了投料比、溶剂、催化剂、温度等条件对产物收率、比旋光度的影响。结果表明:拆分反应较佳条件为n[S-(-)-α-苯乙胺]∶n(6,8-二氯辛酸)=0.45∶1,溶剂为乙酸乙酯;酯化反应较佳条件为催化剂为对甲苯磺酸,反应时间7 h;硫化反应较佳条件为温度为65 ℃;相转移催化剂用量0.4 g,总收率为44.3%。通过红外光谱、比旋光度、核磁共振等对产物和中间产物进行了表征。
6,8-二氯辛酸;拆分;酯化;硫化;R-(+)-α-硫辛酸
α-硫辛酸(α-lipoic acid),化学名为1,2-双硫环戊烷基-3-戊酸,有一个手性中心,两种对映异构体中R-(+)-α-硫辛酸的生理活性远高于S-(-)-α-硫辛酸。α-硫辛酸能够消除致病的自由基[1],属于维生素类药物[2],是唯一兼具脂溶性与水溶性的万能抗氧剂[3-4]。对于肝病、糖尿病、艾滋病、皮肤癌、帕金森氏征、风湿病等多种疾病有治疗功效[5-6]。
1983年,Golding等[7]成功确定了R-(+)-α-硫辛酸的构型。Elliott等[8]首次在手性辅助试剂的诱导下,进行了不对称合成[9],成功合成出R-(+)-α-硫辛酸,总收率37%,该反应所用的原料及试剂极其昂贵,反应条件苛刻,工业上难以操作。Gopalan等[10]首次利用微生物酶催化合成R-(+)-α-硫辛酸,总收率10%,但微生物法[11]中酶的纯度不高并具有弱致病性,至今未见有用于大规模工业生产的报道。
国内研究者普遍采用化学拆分法[12],但直接拆分外消旋α-硫辛酸法[13]得到的产品中含有残留的有毒拆分剂且总收率较低。本研究在此基础上改进,采用拆分外消旋6,8-二氯辛酸得到R-(+)-6,8-二氯辛酸,经酯化、硫化、水解合成R-(+)-α-硫辛酸。拆分后的S-(-)-6,8-二氯辛酸较稳定,可以消旋化再利用,此法反应条件温和、收率高、成本低,具有工业应用前景。
1 实验部分
1.1 试剂与仪器
6,8-二氯辛酸(江苏神州工业有限公司,纯度≥96%);S-(-)-α-苯乙胺(工业级,金坛华阳化工厂);二硫化钠(硫化钠法自制,含量≥95%);对甲苯磺酸(AR,国药集团化学试剂公司);四正丁基溴化铵(AR,国药集团化学试剂公司);无水乙醇(AR,国药集团化学试剂公司,含量≥99.7%),其余试剂均为国药,AR。
Avance 500 MHz核磁共振波谱仪 (德国Bruker公司);Waters-717高效液相色谱仪(美国Waters公司);PROTÉGÉ460型傅里叶红外光谱仪(美国Nicolet公司);WZZ-2B型数字式自动旋光仪(上海浦东物理光学仪器厂);X-4型显微熔点测定仪(北京第三光学仪器厂);RE-2000型旋转蒸发仪(上海亚荣生化仪器厂)。
1.2 合成路线
本研究的合成路线如图1所示。
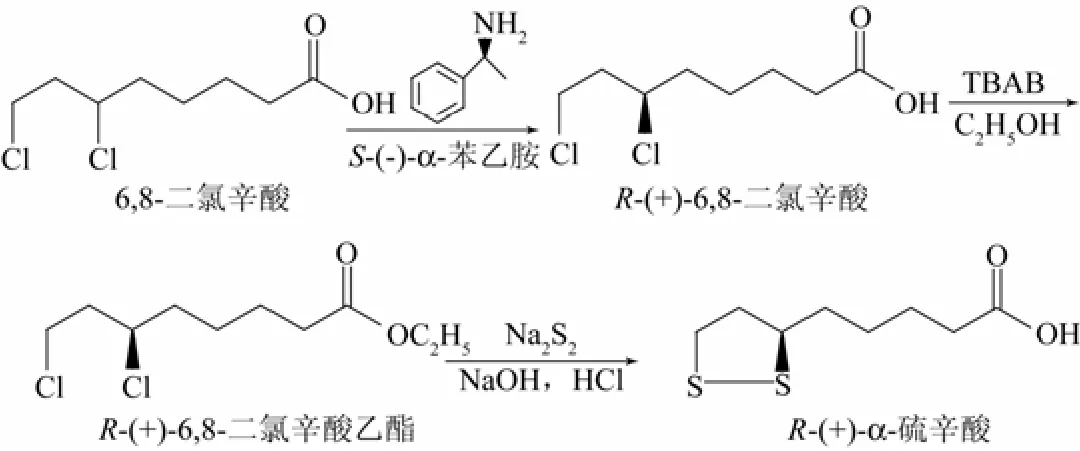
图1 R-(+)-α-硫辛酸的合成路线
1.3 实验方法
1.3.1 R-(+)-6,8-二氯辛酸的合成
将20.0 g(0.094 mol)6,8-二氯辛酸加入三口烧瓶中,20 mL乙酸乙酯作为溶剂,在温度35 ℃,搅拌条件下滴加S-(-)-α-苯乙胺5.5 g(0.045 mol),反应6 h。反应液冷却静置,得到乳白色的晶块,抽滤(母液保留),乙酸乙酯洗涤,真空干燥,得到白色的絮状固体。将其溶于水,经盐酸(5 mol/mL)酸化,乙酸乙酯萃取,干燥,脱溶,得到淡黄色的油状液体7.5 g。纯度(HPLC)97.0%,收率72.8%。比旋光度:[α]20D=26.4(c=1,EtOH),[文献[14]值[α]20D=26.7(c=1,EtOH)]。IR(cm-1):2947.9(νO-—H),2867.5(νC—H),1708.4(νC=O),665.1(νC—Cl)。1H NMR(CDCl3,500 MHz,δ),1.42~1.46(m,2H,4位CH2),1.50~1.62(m,2H,5位CH2),1.66~1.83(m,2H,3位CH2),2.01~2.16(m,2H,7位CH2),2.24~2.30(m,2H,2位CH2),3.66~3.74(m,2H,8位CH2),4.10~4.15(m,1H,6位CH)。
1.3.2 R-(+)-6,8-二氯辛酸乙酯的合成
将5.0 g(0.023 mol)R-(+)-6,8-二氯辛酸加入三口烧瓶中,加入80 mL无水乙醇和0.5 g对甲苯磺酸,充分搅拌,回流温度下反应8 h;乙酸乙酯萃取,20 mL水洗涤3次,干燥,脱溶得到淡黄色的油状液体5.5 g。纯度(HPLC)96.4%,收率93.7%。比旋光度:[α]20D=25.5(c=1,EtOH),[文献[14]值[α]20D=26.5(c=1,EtOH)]。IR(cm-1):2942.9(νO—H),2867.3(νC—H),1734.3(νC=O),665.1(νC—Cl)。1H NMR(CDCl3,500 MHz,δ),1.16~1.19(t,J=7.5 Hz,3H,乙基中的CH3),1.42~1.48(m,2H,4位CH2),1.51~1.63(m,2H,5位CH2),1.72~1.84(m,2H,3位CH2),2.05~2.18(m,2H,7位CH2),2.27(t,J=6.9Hz,2H,2位CH2),3.70~3.76(m,2H,8位CH2),4.02~4.05(q,J=7.4Hz,2H,乙基中的CH2),4.13~4.15(m,1H,6位CH)。
1.3.3 R-(+)-α-硫辛酸的合成
将5.0 g(0.021 mol)R-(+)-6,8-二氯辛酸乙酯加入三口烧瓶中,加入50 mL无水乙醇,0.3 g正四丁基溴化铵(TBAB),在温度65 ℃下,按n[R-(+)-6,8-二氯辛酸乙酯∶n(Na2S2)=1∶1加入Na2S2溶液,搅拌反应6 h;降温至55 ℃,滴加10.0 g NaOH(20%)溶液,水解反应2 h后停止。HCl(5 mol/mL)酸化,甲苯萃取、干燥、脱溶,得到黄色的油状液体,环己烷溶解重结晶,经抽滤得到淡黄色的粉末晶体3.7 g。熔点:46~51 ℃(文献[15]值46~48 ℃),纯度(HPLC)97.3%,收率71.4%。比旋光度:[α]20D=117.2(c=1,EtOH),[文献[16]值[α]20D=119.1(c=1,EtOH)]。IR(cm-1):2927.5(νO—H),2865.1(νC—H),1692.1(νC=O),1249.6和1201.9(νC—S),673.1(νS—S)。1H NMR(CDCl3,500 MHz,δ):3.60~3.55(m,1H,6位CH),3.21~3.10(m,2H,8位CH2),2.50~2.44(m,1H,7位CH2),2.39~2.37(t,2H,2位CH2),1.95~1.88(m,1H,7位CH2),1.75~1.60(m,2H,3位CH2),1.60~1.54(m,2H, 5位CH2),1.54~1.42(m,2H,4位CH2)。
1.3.4 产品的纯度分析条件
色谱条件:固定相Ultimate TM HPLC Column(XB-C18,5 μm,4.6mm×150 mm),柱箱温度25℃,UV检测波长330 nm,进样量20 μL;流动相为甲醇-水-乙酸(300∶200∶0.5,体积比),流速1.0 mL/min。
2 结果与讨论
2.1 R-(+)-6,8-二氯辛酸的合成
2.1.1 投料比对拆分反应的影响
20 mL乙酸乙酯作溶剂,S-(-)-α-苯乙胺缓慢滴加,温度35 ℃下,搅拌反应6 h,测定产物R-(+)-6,8-二氯辛酸的收率和比旋光度,得到其随S-(-)-α-苯乙胺与6,8-二氯辛酸摩尔比变化的曲线,结果见图2。

图2 投料比对拆分反应的影响
外消旋体6,8-二氯辛酸存在对映异构体,通过与S-(-)-α-苯乙胺作用形成非对映异构体[R-(+)-6,8-二氯辛酸·S-(-)-α-苯乙胺],酸处理得到R-(+)-6,8-二氯辛酸,投料比对其收率和比旋光度都有较大的影响。由图2可以看出,随着S-(-)-α-苯乙胺与6,8-二氯辛酸摩尔比的增加,反应收率呈线性增长,最后达到稳定;过量的S-(-)-α-苯乙胺会结合S-(-)-6,8-二氯辛酸形成另一种非对映异构体,产品的比旋光度则呈递减曲线,在0.45∶1后陡降,说明S-(-)-α-苯乙胺结合了相反构型的对映异构体,所以投料比以0.45∶1为宜。
2.1.2 溶剂对反应的影响
温度35 ℃下,以n[S-(-)-α-苯乙胺]:n(6,8-二氯辛酸)= 0.45∶1投料,加入20 mL溶剂,搅拌反应6 h,分别考察不同溶剂对R-(+)-6,8-二氯辛酸收率及比旋光度的影响,结果见表1。
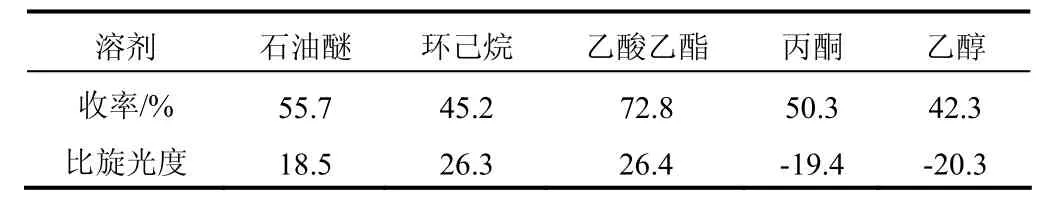
表1 溶剂对拆分反应的影响
手性拆分剂对相应构型的优先选择,与非对映异构体晶盐中的氢键网络结构变化有关系,而氢键网络是由溶剂的介电性决定的。溶剂分子通过填充非对映异构体盐的空间使其析出。表1中,丙酮和乙醇作溶剂时产物的比旋光度是负数,可能由于丙酮、乙醇的介电常数较大导致拆分试剂选择了S构型的对映体;石油醚和环己烷作溶剂时产物的收率不高,原因是溶剂化效果不好,晶盐不能很好析出;乙酸乙酯作溶剂,既可以对消旋混合物中的一种对映异构体进行手性识别[17];又可以通过溶剂化[18]作用使优先构型的微溶非对映异构体结晶析出。因此,乙酸乙酯作溶剂为宜。
2.2 R-(+)-6,8-二氯辛酸乙酯的合成
2.2.1 催化剂对反应的影响
投入5.0 g R-(+)-6,8-二氯辛酸和80 mL无水乙醇,回流温度下反应8 h,分别加入1.0 g不同种类的催化剂,考察其对R-(+)-6,8-二氯辛酸乙酯收率及比旋光度的影响,结果见表2。
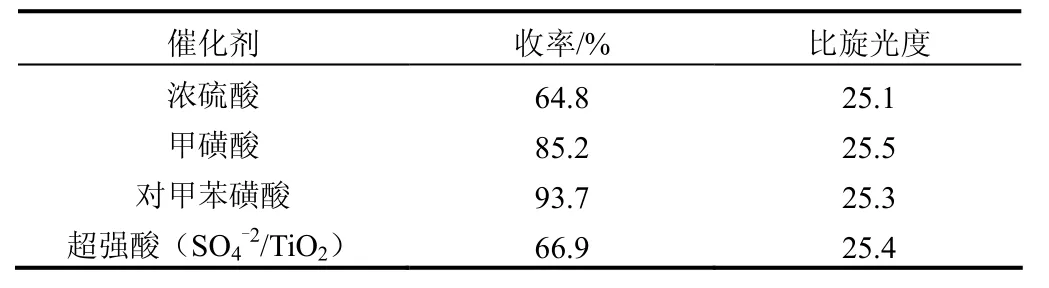
表2 催化剂种类对酯化反应的影响
在酯化反应中酸作为催化剂的作用是将羰基质子化,正电性较强的羰基更有利于亲核试剂醇的进攻。由表2可知,浓硫酸和甲磺酸为催化剂时收率较低,原因是其酸性较强,致使底物酸发生脱水、脱羟基等副反应。超强酸(SO4-2/TiO2)之所以能起催化作用,源于SO4-2在Ti表面配位吸附使Ti—O的电子云偏移,路易斯酸中心得到强化,同时Ti的空d轨道与醇中氧原子上的孤电子对发生配位作用产生质子酸中心。酯化反应中超强酸(SO4-2/TiO2)与C2H5OH中的氧原子配位,发生副反应,生成内酯使得收率降低。对甲苯磺酸由于酸性适中,不容易发生副反应,收率较高。催化剂种类对产物的比旋光度基本没有影响,因此,对甲苯磺酸作为酯化反应的催化剂较好。
2.2.2 反应时间对酯化反应的影响
投入5.0 g R-(+)-6,8-二氯辛酸和80 mL无水乙醇,加入0.5 g对甲苯磺酸作为催化剂,考察不同的反应时间对R-(+)-6,8-二氯辛酸乙酯收率及比旋光度的影响,结果见图3。
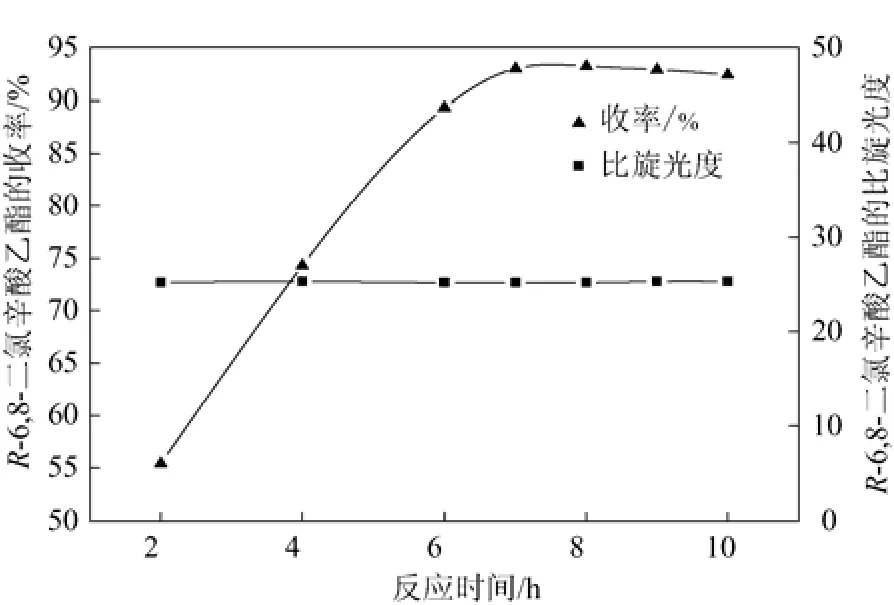
图3 反应时间酯化反应的影响
由图3可知,在反应7h时间内,随着反应时间的延长,R-(+)-6,8-二氯辛酸乙酯的收率不断提高,当反应时间为7 h时,收率达到最大93.2%。7 h以后反应收率趋于平衡且略有下降,可能是发生了一些副反应所致。整个时间段R-(+)-6,8-二氯辛酸乙酯的比旋光度呈平稳趋势,基本不受时间的影响。因此,反应时间确定为7 h为宜。
2.3 R-(+)-α-硫辛酸的合成
2.3.1 温度对硫化反应的影响
以50 mL无水乙醇为溶剂,0.3 g四丁基溴化铵(TBAB)为相转移催化剂,在投料比n[R-(+)-6,8-二氯辛酸乙酯]∶n(Na2S2)=1∶1,硫化反应6 h、55℃水解反应2 h条件下,考察温度对R-(+)-α-硫辛酸的收率及比旋光度的影响,结果见表3。
此反应属于亲核取代,—S—S—键先进攻位阻较小的8位碳原子,另一端随后进攻6位碳原子,形成了活化能较低的五元环,温度为其键断裂提供了必要的能量。由表3可知,在55~65 ℃内,R-(+)-α-硫辛酸的收率随着温度的升高而增加,比旋光度稳定;当反应温度达到65 ℃时,R-(+)-α-硫辛酸的收率最高达70.1%;反应温度超过65 ℃时,收率降低同时比旋光度减小,这是因为在较高温度下,双硫键聚合产生聚合物,同时产物发生一定程度的消旋化。因此,硫化反应的较佳温度为65 ℃。
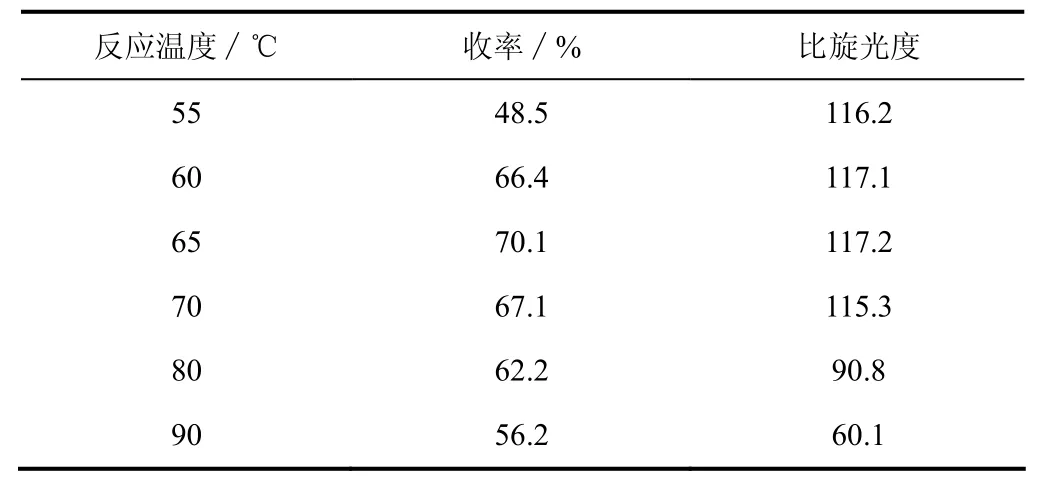
表3 温度对硫化反应的影响
2.3.2 相转移催化剂用量对硫化反应的影响
以50 mL无水乙醇为溶剂,在投料比n[R-(+)-6,8-二氯辛酸乙酯]∶n(Na2S2)=1∶1,硫化反应温度65 ℃、反应时间6 h、55 ℃水解反应2 h条件下,改变相转移催化剂四丁基溴化铵的用量,考察其对R-(+)-α-硫辛酸收率及比旋光度的影响,结果见表4。
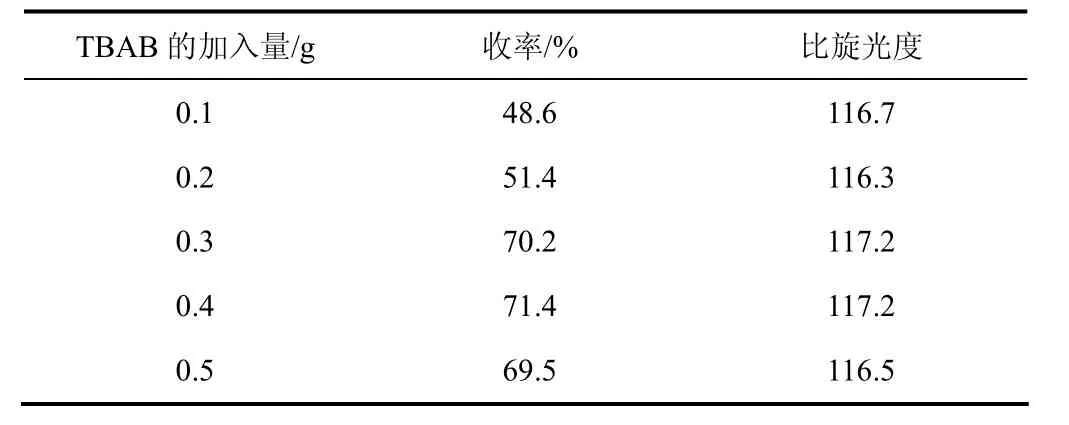
表4 相转移催化剂(TBAB)用量对硫化反应的影响
由表4可知,当相转移催化剂用量较小时,反应收率较低,随着相转移催化剂TBAB用量的增加,反应收率不断提高,这是因为TBAB的(C4H9)4N+与水相中的S2-结合形成盐,使得S2-更容易与R-(+)-6,8-二氯辛酸乙酯中的Cl-发生亲核取代,所以收率会提高。当用量超过0.4 g时收率开始降低,是由于TBAB过量,致使大量的S2-同时进攻R-(+)-6,8-二氯辛酸乙酯的6位和8位C原子,双硫键彼此产生聚合,生成了副产物,因此相转移催化剂的用量取0.4 g为最佳。
2.4 硫化反应机理的探讨
R-(+)-6,8-二氯辛酸乙酯与Na2S2发生的取代反应为合成R-(+)-α-硫辛酸的关键步骤,由于R-(+)-6,8-二氯辛酸乙酯中6位和8位碳上的杂原子Cl有未共享的电子对,使得其α-碳原子更容易被进攻,6位α-碳原子具有位阻效应,因此,其反应历程可以分两步:第一步,双硫基团的一端在8位碳原子上发生取代反应;第二步,另一端在6位碳原子上发生取代并且分子内环化[19]。反应历程如图4所示。
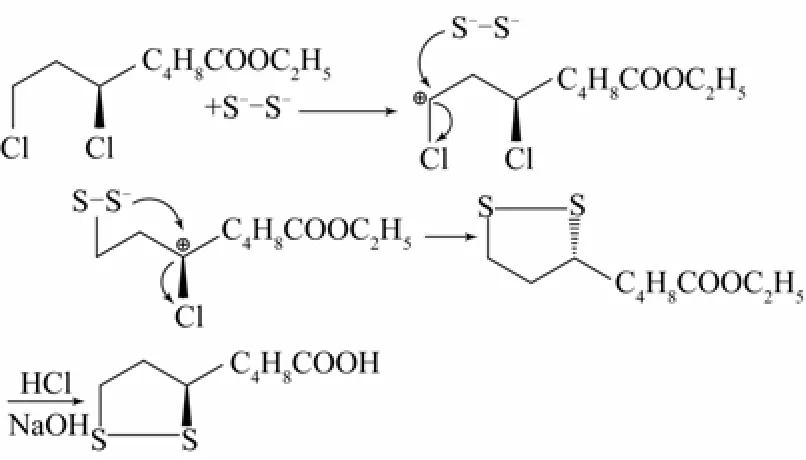
图4 R-(+)-6,8-二氯辛酸乙酯的硫化反应机理
实验证明,硫化反应得到的R-(+)-α-硫辛酸旋光性较好,这就排除了SN1机理,按照SN1机理,亲核试剂分别从两边进攻碳正离子,两种结合方式分别生成了构型保持和构型转化产物,得到的是外消旋产物。因此,推测此反应为SN2机理,即双硫基团一端的S-先从背面进攻位阻较小的8位碳,成键的同时造成Cl-离去。此时另一端没有成键的S-继续进攻手性6位碳,Cl-离去,构型翻转,形成了含有2个S杂原子的五元环,旋光性仍然为右旋。
3 结 论
(1)用S-(-)-α-苯乙胺拆分原料6,8-二氯辛酸,得到R-(+)-6,8-二氯辛酸;经酯化制得R-(+)-6,8-二氯辛酸乙酯;最后经硫化水解合成R-(+)-α-硫辛酸。以6,8-二氯辛酸计三步总收率为44.3%,高于其它文献值。拆分后的S-(-)-6,8-二氯辛酸经消旋化可再利用,此法条件温和,易于工业化推广。
(2)合成R-(+)-6,8-二氯辛酸的较佳条件:投料比为n[S-(-)-α-苯乙胺]∶n(6,8-二氯辛酸)= 0.45∶1,溶剂为乙酸乙酯,纯度97.0%,收率72.8%;合成R-(+)-6,8-二氯辛酸乙酯的较佳条件:催化剂为对甲苯磺酸,反应时间7 h,纯度96.4%,收率93.7%;合成R-(+)-α-硫辛酸的较佳条件:硫化温度65 ℃,相转移催化剂用量0.4 g,纯度97.3%,收率71.4%。
[1] Packer L,Kraemer K,Rimbach G. Molecular aspects of lipoic acid in the prevention of diabetes complication[J]. Nutrition,2001,17:888-895.
[2] 徐兆瑜. 维生素E的替代品——硫辛酸[J]. 精细与专用化学品,2000(16):15.
[3] Samantha B,Pirngruber G D,Roel P. Influence of the properties of zeolite BEA on its performance in the nitration of toluene and nitrotoluene[J]. J. Catal.,2004:297-303.
[4] Wincenty S Monika M. Nitration of toluene with 65% nitric acid over MoO3/SiO2as catalyst[J]. Przem. Chem.,2002,81(8):519-521.
[5] 田部浩三,小野嘉夫,等著. 郑禄彬,等译. 新固体酸和碱及其催化作用[M]. 北京:化学工业出版社,1992:64-65.
[6] Tanabe K. Application of niobium oxides as catalysis[J]. Catal. Today,1990(8):1-11.
[7] Golding B T,Brookes M H,Howes D A. Method for producing lipoic acid and dihydrolipoic acid[J]. J. Chem. Soc.,1983,19:1051-1053.
[8] Elliott J D,Steele J,Johnson W S. An efficient asymmetric synthesis of (R)-(+)-α-lipoic acid [J]. Tetrahedron Letters,1985,26(21):2535-2538.
[9] Sudalai A,Upadhya T T,NikalajeM D,et al. A symmetric dihydroxylation and hydrogenation approaches to the enantioselective synthesis of R-(+)-α-lipoic acid [J]. Tetrahedron Letters,2001,42(29):4891-4893.
[10] Gopalan A S,Jacobs H K.Bakers yeast reduction of alkyl 6-chloro-3-oxohexanoates:Synthesis of (R)-(+)-α-lipoic acid [J]. Journal of the Chemical Society,Perkin Trans.,1990,7:1897-1900.
[11] 韩丽,杨倩,孙志浩,等. 脂肪酶催化拆分外消旋6-羟基-8-氯辛酸乙酯[J]. 精细化工,2007,24(6):573-576.
[12] 曾松,狄延鑫,宋宝安,等.(R)-α-硫辛酸合成方法的研究进展[J]. 精细化工中间体,2007,37(5):1-5.
[13] 杨芹,冷一欣,林富荣,等. α-硫辛酸及其R型异构体的合成[J]. 江苏工业学院学报,2009,21(4):20-23.
[14] Flavio V P,Antonio N P D,Annibale F M,et al. Synthesis of R-(+)-α-lipoic acid:US,2004/0002610 A1[P]. 2004-01-01.
[15] Chavan S,Shivsankar K,Pasupathy K. Simplistic expedient and practical synthesis of (±)-α-lipoic acid [J]. Synthesis,2005,8(5):1297-1300.
[16] Chavan S,Praveen C,Ramakrishna G,et al. Enantioselective synthesis of R-(+)-α and S-(-)-α-lipoicacid [J]. Tetrahedron Letters,2004,45(31):6027-6028.
[17] 孙贤祥,高晓新,孙凌志. 非对映体结晶拆分中的溶剂效应[J]. 常州大学学报:自然科学版,2010,22(4):69-74.
[18] 赖卡特 C著. 唐培楚等译. 有机化学中的溶剂效应[M]. 北京:化学工业出版社,1987:175-176.
[19] 花文廷. 朱新邮译. 杂环化学[M]. 北京:北京大学出版社,1991:20-24.
Synthesis of R-(+)-α-lipoic acid
LENG Yixin,NIU Jinsen,HUANG Chunxiang
(School of Petrochemical Engineering,Changzhou University,Changzhou 213164,Jiangsu,China)
R-(+)-6,8-dichlorooctanic acid was obtained in chiral resolution of 6,8-dichlorooctanic acid by using chiral split agent S-(-)-α-phenylethylamine. R-(+)-α-lipoic acid was synthesized by sulfuration and hydrolysis from R-(+)-6,8-dichlorooctanic acid ethyl ester that was prepared through esterfication reaction. The conditions were investigated and the results showed that the yield and specific rotation were influenced by feed ratio,solvent,catalyst and reaction temperature. Proper experimental condition for chiral reaction was found as:n[S-(-)-α-phenylethylamine]∶n(6,8-dichlorooctanic acid)=0.45∶1,solvent was ethyl acetate. The optimal esterfication reaction conditions was found as:the catalyst was p-toluene sulfonic acid,reaction time 7 h. The optimum conditions of sulfuration reaction were found as:reaction temperature was 65 ℃,the amount of phase transfer catalyst was 0.4 g; The overall yield was 48.4%. The product and intermediate were characterized by IR,specific rotation and1H NMR.
6,8-dichlorooctanic acid;chiral resolution;esterfication;sulfuration;R-(+)-α-lipoic acid
O 626.2
A
1000-6613(2012)06-1325-05
2011-12-07;修改稿日期:2012-02-16。
及联系人:冷一欣(1961—),女,博士,教授,研究方向为绿色化学品和医药中间体的合成。E-mail rxslyxcn@yahoo.com.cn。
