一种合成锂离子电池正极材料LiNi1/3Co1/3Mn1/3O2的新方法
2012-09-25叶乃清钟卓洪
闫 芳, 叶乃清, 田 华, 钟卓洪
(桂林理工大学材料科学与工程学院有色金属及材料加工新技术教育部重点实验室,广西桂林541004)
锂离子电池是20世纪90年代发展起来的一种新型绿色环保电池。它具有工作电压高、能量密度高、自放电小、工作温度范围宽及使用寿命长等许多优点[1-2]。它一诞生就以其它电池不可比拟的优势迅速占领了移动电话、笔记本电脑、小型摄像机、数码照相机、商务通等应用领域。它还将作为主要备选电源应用于混合动力电车 (HEV)、加插式混合动力电车(PHEV)和纯电动车(EV)等领域[3-4]。
目前,商业锂离子电池主要采用钴酸锂(LiCoO2)作为正极材料,这是因为LiCoO2具有比容量较高、放电电压平稳、循环性能好、制备工艺简单和电化学性能稳定等优点。但由于钴资源缺乏、价格昂贵及毒性较高,开发能够替代钴酸锂的新型正极材料成为锂离子电池的重要发展方向[4-5]。
LiNi1/3Co1/3Mn1/3O2是一种极具应用前景的新型正极材料,它集中了LiCoO2、LiNiO2和LiMnO2各自的优点,具有成本低、比容量高和倍率放电性能好、结构稳定性好、安全性高等优点[6]。但其电化学性能受制备工艺的影响很大[4]。采用现有的合成方法来制备LiNi1/3Co1/3Mn1/3O2都存在一些不足。固相合成法[7-8]由于混合均匀性差,需要在较高温度下长时间煅烧,且易形成杂相,很难得到单相的LiNi1/3Co1/3Mn1/3O2。共沉淀法[9-11]是合成均相LiNi1/3Co1/3Mn1/3O2普遍使用的方法,但由于很难通过某种沉淀剂使过渡金属离子完全沉淀下来,在过滤、洗涤过程中易造成过渡金属离子损失。氢氧化物共沉淀法合成前驱体时需要在气氛保护下进行,对设备要求较高,且合成时间较长。探索方便易行、环境友好、成本低的制备方法,对促进其实用化具有重要意义。
本实验采用一种新的合成方法—共沉淀-燃烧法成功合成了具有α-NaFeO2型层状有序结构和良好电化学性能的Li-Ni1/3Co1/3Mn1/3O2。此方法采用草酸作沉淀剂,缩短了共沉淀过程的时间,防止了Mn2+在溶液中被氧化成Mn3+或Mn4+;在共沉淀工序之后采用直接烘干工艺,节约了大量的洗涤用水,且避免了洗涤过程中造成的有效成份损失;之后引入流变相工艺,保证了前驱体与硝酸锂的均匀混合;利用前驱体中的有机成份与后期混入原料中的硝酸根发生燃烧反应,简化了实验过程,缩短了反应时间,节省了能源。总之,该合成方法具有工艺简单、容易操作、节水节能、绿色环保等优点,已获得国家发明专利[12]。所合成的LiNi1/3Co1/3Mn1/3O2比容量高、循环性能好。
1 实验
以 Ni(CH3COO)2·4 H2O、Co(CH3COO)2·4 H2O 和 Mn(CH3-COO)2·4 H2O 为原料,按 Ni∶Co∶Mn(摩尔比)=1∶1∶1 准确称量物料,加入适量去离子水制成1 mol/L的Ni-Co-Mn醋酸盐混合溶液。按n(NH3·H2O)∶n(Ni+Co+Mn)=5∶1往上述混合溶液中加入氨水,制成络合溶液。按n()∶n(Ni+Co+Mn)=1.1∶1向上述络合溶液中加入碾成粉末的H2C2H2O,在40~60℃的水浴中剧烈搅拌下反应0.5 h,使之沉淀出Ni-Co-Mn复合草酸盐。将Ni-Co-Mn复合草酸盐和反应母液一起在90℃下烘干,得到Ni-Co-Mn复合草酸盐和醋酸铵的混合物。按n(Li)∶n(Ni+Co+Mn)=1.1∶1比例往上述混合物中加入LiNO3,并加少量水调成流变相并搅拌均匀,放入加热到500℃并恒温的马弗炉中,使之发生燃烧反应。将燃烧反应产物收集,在800℃回火处理15 h。最后将回火后的产物研磨,并过300目筛,得到LiNi1/3Co1/3Mn1/3O2粉末。
采用北京普析通用仪器有限公司生产的TAS-990型原子吸收光谱仪分析合成样品中金属元素的含量。
采用荷兰帕纳科公司生产的X'Pert PRO型X射线衍射仪分析合成样品的物相与结构。采用离位XRD技术研究正极材料在充电过程中的结构变化。实验条件为:CuKα(λ=0.15406 nm)辐射,石墨单色器,管电压45 kV,扫描范围10°~70°,扫描速度15(°)/min。
采用日本电子株式会社(JEOL)生产的JSM-5610LV型扫描电子显微镜观察合成产物的形貌。
将合成的正极材料、乙炔黑和聚偏氟乙烯(PVDF)按质量比为8∶1∶1准确称量,与1-甲基-2-吡咯烷酮混合研磨均匀制成浆料并均匀地涂在铝箔上。将涂好的电极片在120℃的真空干燥箱中干燥24 h以上,用专用冲具冲出直径为16 mm的工作电极。以工作电极为正极,同样大小的金属锂片为负极,Celgard2400聚丙烯微孔膜为隔膜,1 mol/L的LiPF6/(EC+DEC+DMC)有机溶液(EC、DEC和DMC的体积比为2∶2∶1)为电解液,在充满高纯氩气的手套箱中组装成扣式电池作为实验电池。
用深圳市新威尔电子有限公司生产的BTS-5V-10mA型锂离子电池测试仪测定实验电池的充放电容量。恒流充放电倍率为0.1C,截止电压为2.5~4.35 V。
2 结果与讨论
2.1 合成产物的化学组成

?
表1是合成产物的原子吸收光谱分析结果。从表中可以看出,合成产物中过渡金属元素的实际组成与配料组成几乎完全相同。这说明通过草酸共沉淀法制备前躯体并采用直接烘干的办法能够准确控制合成产物的组分。
因为锂是在前驱体烘干后再引入的元素,其含量变化与烘干前的处理方式没有关系,其实际组成与配料组成的偏差主要是由于Li在燃烧反应和回火处理过程中挥发,使合成的正极材料中Li含量有所降低所致。这也说明,配料时适当增加锂的含量,使原料中的锂过量是有必要的。
2.2 合成产物的结构与形貌
图1是合成产物的XRD图。从图中可以看出,合成产物可按α-NaFeO2型结构进行指标化,衍射数据与LiNiO2(PDF卡85-1966)非常接近,无杂相峰,表明合成产物与LiNiO2的结构相同,是具有 α-NaFeO2型层状结构的固熔体 LiNi1/3Co1/3-Mn1/3O2;衍射峰强度大而且尖锐,说明所合成的正极材料结晶良好;(006)/(012)和(018)/(110)两对衍射峰分裂明显,说明所合成的正极材料LiNi1/3Co1/3Mn1/3O2层状结构特征明显。
Chang Chun-Chieh等[13]曾对 Li1-zNi1+zO2的 X 射线衍射花样进行过模拟,结果显示,(003)与(104)衍射峰的强度比值(R=I003/I104)与Li位上混入的Ni2+的数量z成反比,占据Li位的Ni2+离子越多则R值越小。R值反映了镍酸锂中阳离子的有序度。当R>1.3时,说明占据Li位的Ni2+离子很少,阳离子的有序度高,预示材料有良好的电化学活性。因此,可以用衍射峰强度比值(R=I003/I104)定性分析含镍的层状嵌锂过渡金属氧化物的阳离子有序度及其电化学活性[14-15]。
从图1可以看出,合成产物的衍射峰强度比值R为1.58>1.3,说明所合成的正极材料LiNi1/3Co1/3Mn1/3O2阳离子有序度较高,预示着材料有较高的电化学活性。

图2是合成产物的扫描电镜照片。从图中可以看出,合成产物的颗粒大小均匀,轮廓清晰,粒径在0.5~2 μm左右,说明采用共沉淀-燃烧法能够合成粒度适中、大小均一的正极材料LiNi1/3Co1/3Mn1/3O2。

2.3 合成产物的电化学性能
图3是合成产物在2.5~4.35 V范围内0.1C倍率的首次、第20次和第50次充放电曲线,从图中可以看出合成产物具有稳定的充放电平台,充放电过程中电压变化平稳,充放电比容量较高,首次放电比容量达到169.05 mAh/g。
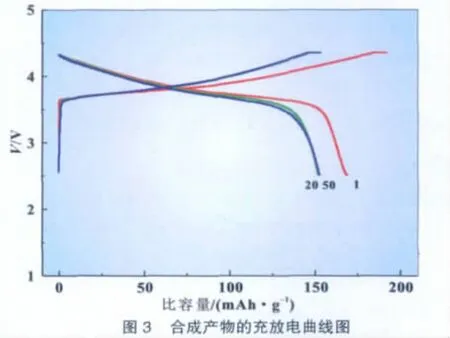
图4是该样品50次循环的充放电比容量与循环次数的关系曲线图。从图中可以看出,前3次循环充放电比容量衰减较快,此后充放电比容量衰减很小。经过20次循环后,充放电比容量基本稳定在152 mAh/g左右。第50次循环的放电比容量仍保有152.83 mAh/g。由此可知,采用共沉淀-燃烧法合成的LiNi1/3Co1/3Mn1/3O2具有良好的循环性能。

2.4 合成产物的结构稳定性
为了研究不同充电状态下的合成产物的结构稳定性,采用离位XRD分析技术对不同充电状态下的合成产物LiNi1/3Co1/3Mn1/3O2进行了测试。图5为不同充电状态下合成产物LiNi1/3Co1/3Mn1/3O2的XRD图,从图中可以看出随着充电电压的升高,衍射峰略向高角度方向漂移且逐渐变宽。这是由于随着充电电压的升高、锂离子的脱出,正极活性材料LiNi1/3Co1/3Mn1/3O2的晶胞略有收缩,材料内部产生了一定的应力所造成的。充电到4.5 V甚至4.8 V时,正极材料仍然保持着α-NaFeO2型层状结构。这说明合成产物在充放电过程中的结构是相当稳定的。
美国Brookhaven国家实验室的X.Q.Yang等人[16]曾对LiNiO2和LiNi0.75Mg0.125Ti0.125O2在充放电过程中的结构变化进行过深入的研究。研究发现,当充电电压升高到4 V以上,LiNiO2会从原来的六方相H1向六方相H2转变,再从六方相H2向H3转变,如图6(a)所示。而六方相H3在放电过程中不能转变为H2和H1。因此,LiNiO2的抗过充能力是很差的。镁钛复合掺杂的镍酸锂LiNi0.75Mg0.125Ti0.125O2却大不一样,充电电压从3.4 V升高到5.2 V只出现第二个六方相H2,没有出现第三个六方相H3,如图6(b)所示。放电过程中LiNi0.75Mg0.125-Ti0.125O2的结构可以恢复到充电前的六方相H1,因此LiNi0.75Mg0.125Ti0.125O2具有良好的抗过充能力。


图7是本实验合成的正极材料在不同充电状态下衍射峰(003)的X射线衍射图。从图中可以看出,当充电电压达到4.35 V时,正极材料中已出现少量的六方相H2,衍射峰明显宽化。随着充电电压的进一步升高,六方相H2逐渐增多,衍射峰进一步变宽,并向高角度方向漂移。但直到4.8 V也没有出现不可逆的六方相H3。将其与图6(b)比较可以看出,随着充电电压的升高,其结构变化与LiNi0.75Mg0.125Ti0.125O2的结构变化比较接近,而与LiNiO2的结构变化差别较大。由此认为,所合成的正极材料LiNi1/3Co1/3Mn1/3O2的结构稳定性较好,深度充电时结构变化较小,具有较强的抗过充能力。
3 结论
(1)以 LiNO3、Ni(CH3COO)2·4 H2O、Co(CH3COO)2·4 H2O和Mn(CH3COO)2·4 H2O为原料,采用共沉淀-燃烧法可以合成具有α-NaFeO2型层状有序结构的LiNi1/3Co1/3Mn1/3O2正极材料。
(2)所合成的LiNi1/3Co1/3Mn1/3O2结晶良好、粒度适中、大小均匀,并具有良好的电化学性能。首次放电比容量达到169.05 mAh/g,经过20次循环后放电比容量基本稳定在152 mAh/g左右,第50次循环放电比容量仍有152.83 mAh/g。
(3)所合成的LiNi1/3Co1/3Mn1/3O2在深度充电状态下结构变化较小,具有良好的结构稳定性。
[1]马荣骏.锂离子电池及其正极材料的研究进展[J].有色金属,2008,60(1):1-6.
[2]吴宇平,戴晓兵,马军旗,等.锂离子电池——应用与实践[M].北京:化学工业出版社,2004:9-10.
[3]陈立泉.混合电动汽车及其电池[J].电池,2000,30(3):98-100.
[4]SANTHANAM R,RAMBABU B.High rate cycling performance of Li1.05Ni1/3Co1/3Mn1/3O2materials prepared by sol-gel and co-precipitation methods for lithium-ion batteries[J].Journal of Power Sources,2010,195:4313-4317.
[5]RITCHIE A G.Recent developments and likely advances in lithium rechargeable batteries[J].Journal of Power Sources,2004,136:285-289.
[6]BELHAROUAK I,SUN Y K,LIU J,et al.Li(Ni1/3Co1/3Mn1/3)O2as a suitable cathode for high power applications[J].Journal of Power Sources,2003,123:247-252.
[7]YABUUCHI N,OHZUKU T.Novel lithium insertion material of Li-Co1/3Ni1/3Mn1/3O2for advanced lithium-ion batteries[J].Journal of Power Sources,2003,119-121:171-174.
[8]WANG Z X,SUN Y C,CHEN L Q,et al.Electrochemical characterization of positive electrode material Li(Ni1/3Co1/3Mn1/3)O2and compatibility with electrolyte for lithium-ion batteries[J].J Electrochem Soc,2004,151(6):A 914-A 921.
[9]LUO X F,WANG X Y,LIAO L,et al.Effects of synthesis conditions on the structural and electrochemical Li(Ni1/3Co1/3Mn1/3)O2cathode material via the properties of layered hydroxide co-precipitation method LIB SCITECH[J].Journal of Power Sources,2006,161:601-605.
[10]ZHANG S C,QIU X P,HE Z Q,et al.Nanoparticled Li(Ni1/3Co1/3-Mn1/3)O2as cathode material for high-rate lithium-ion batteries[J].Journal of Power Sources,2006,153:350-353.
[11]DENG C,ZHANG S,FU B L,et al.Synthetic optimization of nanostructured Li(Ni1/3Mn1/3Co1/3)O2cathode material prepared by hydroxide coprecipitation at 273 K[J].Journal of Alloys and Compounds,2010,496:521-527.
[12]田华,叶乃清,刘丹.镍钴锰酸锂的共沉淀-燃烧合成方法:中国,CN101215011[P].2008-07-09.
[13]CHANG C C,SCARR N,KUMTA P N.Synthesis and electrochemical characterization of LiMO2(M=Ni,Ni0.75Co0.25)for rechargeable lithium ion batteries[J].Solid State Ionics,1998,112:329-344.
[14]杨清河,马晓华,宋庆梅,等.锂离子二次电池阴极材料LiNi0.8-Co0.2O2的研究[J].化学世界,2000,41(S1):122-125.
[15]LIU Z L,YU A S,LEE JIM Y,et al.Synthesis and characterization of LiNi1-x-yCoxMnyO2as the cathode materials of secondary lithium batteries[J].Journal of Power Sources,1999,81-82:416-419.
[16]YANG X Q,SUN X,BREEN J M.Structural changes and thermal stability:in situ X-ray diffraction studies of a new cathode material LiMg0.125Ti0.125Ni0.75O2[J].Electrochemistry Communications,2000,2:733-737.
