应用遗传学和分子生物学分析评价伊马替尼和常规化疗治疗慢性粒细胞白血病的疗效
2012-09-17闫金松康志杰武克宇
李 莉,闫金松,康志杰,武克宇
(大连医科大学附属第二医院血液科,辽宁大连 116027)
应用遗传学和分子生物学分析评价伊马替尼和常规化疗治疗慢性粒细胞白血病的疗效
李 莉,闫金松,康志杰,武克宇
(大连医科大学附属第二医院血液科,辽宁大连 116027)
[目的]比较伊马替尼和常规化疗治疗慢性粒细胞白血病的疗效。[方法]收集20例慢性粒细胞白血病患者,其中11例应用伊马替尼治疗,9例应用常规化疗。采用常规染色体显带技术和半定量RT-PCR技术对细胞遗传学及分子遗传学进行动态监测,评价两种不同治疗方法的血液学、遗传学、分子生物学缓解率。[结果]应用伊马替尼治疗的患者均达血液学缓解,其中9例患者Ph染色体和bcr-abl融合基因消失,遗传学缓解率为81%。应用常规化疗的患者均能达到血液学缓解,但无一例达遗传学缓解。[结论]伊马替尼治疗慢性粒细胞白血病能达到部分或完全细胞遗传学缓解及分子生物学水平的缓解,优于常规化学药物治疗。
慢性粒细胞白血病;Ph染色体;bcr-abl融合基因;伊马替尼
慢性粒细胞白血病(chronic myeloid leukemia,CML)是一种起源于造血干细胞的血液系统恶性疾病,细胞遗传学特征是具有Ph染色体,即t(9;22)(q34;q11),其分子水平上形成bcr-abl mRNA。细胞遗传学和分子生物学分析对于慢性粒细胞白血病的发病机制、诊断分期、治疗监测以及预后判断都具有很重要的价值。既往慢性粒细胞白血病患者多以干扰素联合羟基脲控制白血病细胞数量,只能达到血液学缓解[1],而新的靶向治疗药物甲磺酸伊马替尼(简称伊马替尼)是针对Ph染色体阳性(Ph+)白血病致病基因产物(P210bcr-abl或 P190bcr-abl)的分子靶向药物,可使患者达到遗传学甚至分子生物学缓解[2]。本文对大连医科大学附属第二医院近4年分别应用干扰素联合羟基脲和应用伊马替尼治疗的慢性粒细胞白血病患者的临床效果进行了观察。
1 资料与方法
1.1 临床资料
选择2007年10月—2011年10月于对大连医科大学附属第二医院住院和门诊随诊的CML慢性期(CP)患者,男11例,女9例,年龄12~81岁,中位年龄45岁,患者初发时外周血白细胞数在22×109/L~410×109/L 间,中位数为 223.2×109/L,CML诊断分期标准参照张之南主编的《血液病诊断及疗效标准》[3]。
1.2 治疗方案
20例患者,初发时根据外周血白细胞数调整羟基脲用量,2~6 g/d,待白细胞降至20×109/L以下,9例患者应用羟基脲联合干扰素治疗,应用羟基脲0.5~1 g/d,干扰素300万单位隔日1次肌注,维持白细胞至5~10×109/L,11例患者单用伊马替尼400~600 mg/d治疗,上述患者在初发时均检查染色体核型和bcr-abl基因表达,每3个月复查染色体核型,直至Ph+染色体消失,每3个月复查bcrabl融合基因表达,连续观察3年。
1.3 染色体核型分析
全部病例染色体标本取自患者骨髓。采用骨髓细胞直接培养法[4],取新鲜肝素抗凝骨髓3 mL,在含20%小牛血清的1640培养基的标本瓶中按2×106/mL的细胞密度接种,37℃温箱中持续培养24 h,加入终浓度0.05 μg/mL秋水仙碱,孵育1 h收获细胞。常规G显带技术进行核型分析,全部病例分析细胞数均在20~30个。核型异常参照《人类细胞遗传学国际命名体制(ISCN2005)》[5]的有关规定进行描述。
1.4 巢式逆转录聚合酶链反应(RT-PCR)检测bcr-abl融合基因
RNA提取采取新鲜骨髓或血液标本经肝素或EDTA抗凝,用相对密度为1.077的淋巴细胞分层液分离单个核细胞。经Trizol试剂(美国Invitrogen公司)、氯仿以及异丙醇等提取细胞总RNA。RNA为模板应用反转录试剂盒(Promega)反转录cDNA第1链,以cDNA为模板行巢式PCR,bcr-abl融合基因根据断裂点位置不同,最常见拼接方式为Major型和minor型。Major型第1轮扩增引物为BCRA1:5’-GCTTCTCCCTGACATCCGTG -3’,ABLB:5’-CGAGCG GCTTCACTCAGACC -3’,第2轮扩增引物为 BCR-C1:5’-CTCCAGACTGTCCACAGCATTCCG-3’,ABL-D:5’-CAGACCCTGAGGCTCAAAGTCAGC-3’。minor型第1轮扩增引物为 BCR-A2:5’-CGCATGTTCCGGG ACAAAAGC-3’,ABL-B:5’-CGAGCGGCTTCACTCAGACC-3’,第2轮扩增引物为BCR-C2:5’-AACAGT CCTTCGACAGCAGCAGTC -3’,ABL-D:5’-CAGACCCTGAGGCTCAAAGTCAGC -3’。第2轮扩增均取5 μL第1轮的扩增产物为模板,两轮 PCR 反应条件均为:94℃,30 s,58℃,30 s,72℃,45 s,共 36 个循环,72℃ 5 min,4℃。同时设阳性及阴性对照。
1.5 疗效标准
血液学疗效:完全血液学缓解(CHR)标准:WBC<10×109/L,BPC <450×109/L,外周血中无幼稚细胞;外周血中嗜碱粒细胞<0.05;无髓外浸润,需持续≥4周。
细胞遗传学疗效:完全细胞遗传学缓解(CCyR)为骨髓中 Ph+细胞为0;主要细胞遗传学缓解(MCyR)为Ph细胞≤35%。
分子学疗效:完全分子学缓解(CMoR)为骨髓中实时定量RT-PCR方法检测bcr-abl与abl比值为0;主要分子学缓解(MMoR)为治疗后骨髓中bcr-abl与abl比值较治疗前下降≥3个对数级。
2 结 果
2.1 血液学疗效
20例患者在中位治疗 0.8(0.2 ~2.3)个月时均获CHR。羟基脲联合干扰素组有1例22个月进入加速期,应用化疗未回到慢性期,2个月后转为加速期,27个月时死亡。1例伊马替尼组患者在治疗22个月时丧失CHR(但未进入加速或急变期),经改用达沙替尼25个月时再次获得CHR,已持续40个月。其余10例均在治疗中,并持续CHR。
2.2 细胞遗传学疗效
9例羟基脲联合干扰素组患者,7例染色体核型为46,t(9,22)(q34,q11),2 例染色体核型为 46,XY。7例Ph+患者治疗后每年复查染色体核型,均未达CyR。11例伊马替尼组患者染色体核型均为46,t(9,22)(q34,q11),有 2 例随诊 2 年未达 CyR,其余9例(81%)于中位6(2~33)个月时获得CCyR,1例患者在治疗第3个月时获得CCyR,22个月时丧失CHR及CCyR,经改用达沙替尼27个月时再次获得CCyR至今。
2.3 分子学疗效
羟基脲联合干扰素组患者,有2例在染色体核型分析时无Ph+染色体,在bcr-abl扩增时为阴性,其他7例均为bcr-abl Major型阳性,治疗2年后再次检测,7例阳性者无一例转阴。伊马替尼组中初发时行融合基因检测,bcr-abl Major型均为阳性,见图1,与染色体核型分析符合率100%,2年分子学随诊评估结果为11例患者巢式RT-PCR检测3例转阴(27%)。其中1例于外院行实时定量PCR,证实拷贝数为0,达 CMoR,其余8例 bcr-abl融合基因未转阴,但RT-PCR检测显示有5例患者扩增条带明显减弱,见图2。其中3例于外院行实时定量PCR,证实bcr-abl/abl的比值明显下降,下降幅度>3个对数级,故可判定为MMoR,其中1例患者在伊马替尼治疗2.5个月、6个月、9.5个月时bcr-abl/abl的比值分别为 0.062%、0.082%、0.14%,达到MMoR,但在随诊过程中bcr-abl拷贝数有增高趋势,现继续随诊过程中。
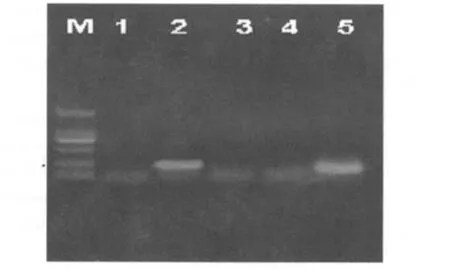
图1 1例慢性粒细胞白血病患者发病时的bcr-abl融合基因扩增结果Fig 1 Bcr-abl fusion gene expression in a onset CML patient

图2 8例慢性粒细胞白血病患者治疗前后的bcr-abl融合基因扩增结果Fig 2 Bcr-abl fusion gene expression in 8 CML patients before and after imatinib treatment
3 讨论
慢性粒细胞白血病(CML)是一种累及造血干细胞的恶性克隆增殖性疾病[7]。在患者肿瘤细胞中可以检测到t(9;22)(q34;q11)染色体易位和bcr-abl融合基因。临床上,CML患者在平均3~5年的慢性期后进入加速或急变期,此时常伴有bcrabl基因在DNA水平扩增和mRNA及蛋白水平表达的上升。
既往治疗慢性粒细胞白血病多采用羟基脲联合干扰素控制白细胞数量,控制病情进展[8],大宗病例的国际临床试验证实,伊马替尼治疗CML慢性期的有效性与安全性明显优于以往的药物[9]。对早慢性期(1年以内)和IFN-α治疗失败的晚慢性期患者的远期疗效两项研究结果均为CHR率96%;MCyR率分别为88%,73%;CcyR率分别为81%和63%,CcyR患者中 MMoR率和 CMoR率分别为75%、49%和36%、24%,预计42个月或48个月,PFS率和OS率分别为84%、80%和91%、86%[10]。本组11例慢性粒细胞白血病患者伊马替尼治疗后遗传学缓解率(包括完全遗传学缓解和主要遗传学缓解)为90%。9例应用羟基脲联合干扰素控制白细胞数量的患者,7例Ph染色体阳性,无一达遗传学缓解,证明伊马替尼治疗遗传学疗效优于传统的化学药物治疗。
虽然伊马替尼已被大量研究证实是一种安全、能有效治疗慢性粒细胞白血病的药物,但部分患者已在用药过程中出现耐药,从而发生疾病的进展,目前研究者们提出解决伊马替尼耐药的策略主要有[11]:增加伊马替尼剂量、使用其他更强烈可抑制bcr-abl的药物如第二代酪氨酸激酶抑制剂达沙替尼和尼洛替尼[12],异基因干细胞移植[13]等。本组中1例伊马替尼组患者在治疗22个月时丧失CHR(但未进入加速或急变期),经伊马替尼剂量增高至600 mg/d,无效,改用达沙替尼后2个月达血液学缓解,25个月时再次获得CHR,已持续40个月,提示二代酪氨酸激酶抑制剂可有效逆转伊马替尼耐药。
探讨应用伊马替尼的慢性粒细胞白血病患者在获得CCyR后停用药物治疗的可能性的临床试验正在进行中[14],在应用伊马替尼3年后开始停止服药,停药12个月时,仍然CyR的占41%,复发患者再次应用伊马替尼,38%的患者bcr-abl水平下降,61.9%的患者取得持久PCR阴性,显示停药后部分患者仍可维持一段时间的缓解,提高了生活质量,复发患者再次应用依然有效。
伊马替尼治疗慢性粒细胞白血病的临床疗效肯定,明显优于传统化疗,第二代药物仍在不断改进中。因此,酪氨酸激酶抑制剂类药物有望成为根治慢性粒细胞白血病的特效药物,药物的耐药、剂量调整及长期用药的停药指证探讨可有望延长缓解时间,提高生存质量,为挽救更多慢性粒细胞白血病患者的生命带来希望。
:
[1]O’Brien SG,Guilhot F,Larson RA,et al.Imatinib compared with interferon and low dose cytarabine for newly diagnosed chronic - phase chronic myeloid leukemia[J].N Engl J Med,2003,348(13):994 -1004.
[2]Buchdunger E,Matter A,Dmker BJ.Bcr- Abl inhibition as a modality of CML thempeutics[J].Biochim Biophys Acta,2001,1551(1):M11 - M18.
[3]张之南,沈悌.血液病诊断及疗效标准[M].第3版.北京:科学技术出版社,2007.134.
[4]陈苏宁,薛永权,吴亚芳,等.急性髓系白血病患者染色体异常核型检出方法的改进[J].中华血液学杂志,2004,25(3):181 -183.
[5]Shaffer LG,Tommerup N.SCN:An International System for Human Cytogenetic Nomenclature[S].Karger S Basel,2005.
[6]王慧萍,李国霞,乔振华,等.联合应用细胞遗传学,巢式RT-PCR和FISH技术检测慢性髓系白血病治疗过程中的肿瘤负荷[J].中国实验血液学杂志,2007,15(2):237-241.
[7]Gallipoli P,Abraham SA,Holyoake TL.Hurdles toward a cure for CML:the CML stem cell[J].Hematol Oncol Clin North Am,2011,259(5):51 -66.
[8]Hochhaus A,Druker B,Sawyers C,et al.Favorable long -term follow up results over 6 years for response,survival,and safety with imatinib mesylate therapy in chronic-phase chronic myeloid leukemia after failure of interferon-alpha treatment[J].Blood,2008,111(3):1039 - 1043.
[9]Druker BJ,0’Brien SG,Guilhot F,et al.Five - year followup of patients receiving imatinib for chronic myeloid leukemia[J].N Engl J Med,2006,355(7):2408 -2417.
[10]Martin Henkes,Heiko van der Kuip,Walter E Aulitzky.Therapeutic options for chronic myeloid leukemia:focus on imatinib(Glivec®,GleevecTM)[J].Ther Clin Risk Manag,2008,4(1):163-187.
[11]Quint s- Cardama A,Kantarjian HM,Coaes JE.Mechanisms of primary and secondary resistance to imatinib in chronic myeloid leukemia[J].Cancer Control,2009,16(2):122-131.
[12]le Coutre P,Ottmann OG,Giles F,et al.Nilotinib(formerly AMNl07),a highly selective BCR -ABL tyrosine kinase inhibitor,is active in patients with imatinib—resistant or intolerant accelerated-phase chronic myelogenous leukemia[J].Blood,2008,111(4):1834 -1839.
[13]Fernandez HF,Kharfan-Dabaja MA.Tyrosine Kinase lnhibitors and Allogeneic Hematopoietic Cell Tramplantation for Chronic Myeloid Leukemia:Targeting Both Therapeutic Medalities[J].Cancer Control,2009,16(2):153-158.
[14]Mahon FX,Réa D,Guilhot J,et al.Discontinuation of imatinib in patients with chronic myeloid leukaemia who have maintained complete molecular remission for at least 2 years:theprospective,multicentreStop Imatinib(STIM)trial[J].Lancet Oncol,2010,11(11):1029 -1035.
Efficiency evaluation of imatinib and traditional chemical therapy in patients with chronic myeloid leukemia by analysis of cytogenetics and molecular genetics
LI Li,YAN Jin - song,KANG Zhi- jie,WU Ke - yu
(Department of Hematology,the Second Affiliated Hospital of Dalian Medical University,Dalian116027,China)
Abstract:[Objective]To compare the efficiency of imatinib mesylate(imatinib)and traditional chemical therapy in patients with chronic myeloid leukemia(CML)in chronic phase.[Methods]Collecting 20 patients with chronic myeloid leukemia in chronic phase,11 patients were treated with imatinib,while the other 9 were treated with traditional chemical therapy.Karyotypes were analyzed by chromosome G banding in 20 cases who were monitored the level of bcr-abl fusion gene by RT-PCR before and after administrating imatinib or traditional chemical therapy.Evaluate the rates of CHR,CyR,MoR.[Results]All the patients treated with imatinib got complete hematological response(CHR),9 of which had negative ph chromosome and bcr-abl fusion gene.The cytogenetic response(CyR)response rate is 81%.To patients with traditional chemical therapy,CHR rate is 100%,but no one got CyR.[Conclusion]Imatinib significantly improves cytogenetic and molecular response rates of patients with chronic myeloid leukemia,which is better than traditional chemical therapy.
Key words:chronic myeloid leukemia;Philadelphia chromosome;bcr-abl fusion gene;Imatinib
R733.7
A
1671-7295(2012)05-0465-04
2012-05-15;
2012-08-28
李 莉(1972-),女,辽宁丹东人,副教授。E-mail:lilydlmu@hotmail.com
闫金松,教授。E-mail:yanjsdmu@gmail.com
