血清高迁移率族蛋白B1在糖尿病视网膜病变患者中的表达水平和临床意义
2012-09-07杨宏伟黄永刚陈晓隆刘洁底煜陆岩
杨宏伟,黄永刚,陈晓隆,刘洁,底煜,陆岩
(1.中国医科大学附属盛京医院眼科,沈阳 110004;2.东北大学机械与自动化学院,沈阳 110003;3.中国医科大学实验设备处,沈阳110001)
糖尿病视网膜病变(diabetic retinopathy,DR)是糖尿病的严重并发症之一,严重影响人类健康和生活质量。据报道,经济发达国家DR致盲率已经位居致盲性眼病的前列。随着经济发展和生活水平提高,糖尿病的患病率正迅速升高。因此预防和治疗DR减少糖尿病患者的致盲率已成为目前眼底病医生的重要任务。
DR发病机制的基础为高糖诱导的微血管和神经组织损伤[1]。近来研究表明在DR的微血管损伤机制中存在着炎性因子的作用[2]。高迁移率族蛋白B1(high mobility group box-1,HMGB1)作为晚期炎性介质,在糖尿病组织中诱导炎性反应和促进血管的生成[3]。本研究拟通过检测患者血清HMGB1水平,探讨HMGB1与糖尿病视网膜病变患者各临床指标之间的关系,以明确HMGB1在DR发病机制中的作用和意义。
1 材料与方法
1.1 临床资料
在我院眼科2011年6月至2012年1月住院患者中选取糖尿病视网膜病变患者37例,其中增殖性糖尿病视网膜病变患者(proliferative diabetic retinopathy,PDR)12例、非增殖性糖尿病视网膜病变患者(nonproliferative diabetic retinopathy,NPDR)14例和无视网膜病变的糖尿病患者(DRO)11例,以及正常人9例设为正常对照组(NORMAL)。所有入选对象均已排除急慢性感染、炎性疾病、严重肝肾疾病等。各组入选者性别、年龄等基本情况无统计学差异。
1.2 方法
入选者清晨空腹采静脉血,离心(3 000 r/min)分离血清,-70℃存贮,测定糖化血红蛋白(HbAC1)(美国BIO-RAD,D10)、空腹血糖、高密度脂蛋白、低密度脂蛋白、甘油三酯和总胆固醇(美国亚培C16000),ELISA法检测HMGB1含量(美国R&D公司)。
1.3 统计学处理
用SPSS 19.0软件包进行统计学分析。计量资料结果以±s表示,行单因素ANOVA分析和Pearson相关分析。P<0.05为差异有统计学意义。
2 结果
2.1 各组血清HMGB1水平
正常对照组血清HMGB1水平为(7.54±0.68)mmol/L,HMGB1在糖尿病患者血清中比正常人明显增高,差异具有统计学意义(P<0.01)。在PDR组[(16.39±1.70)mmol/L]和 NPDR 组[(11.79±1.15)mmol/L]均显著高于NDR的糖尿病患者(9.34±0.78)(P<0.01),且PDR组HMGB1水平显著高于NPDR组(P<0.01)。各组间差异均具有统计学意义(表 1)。
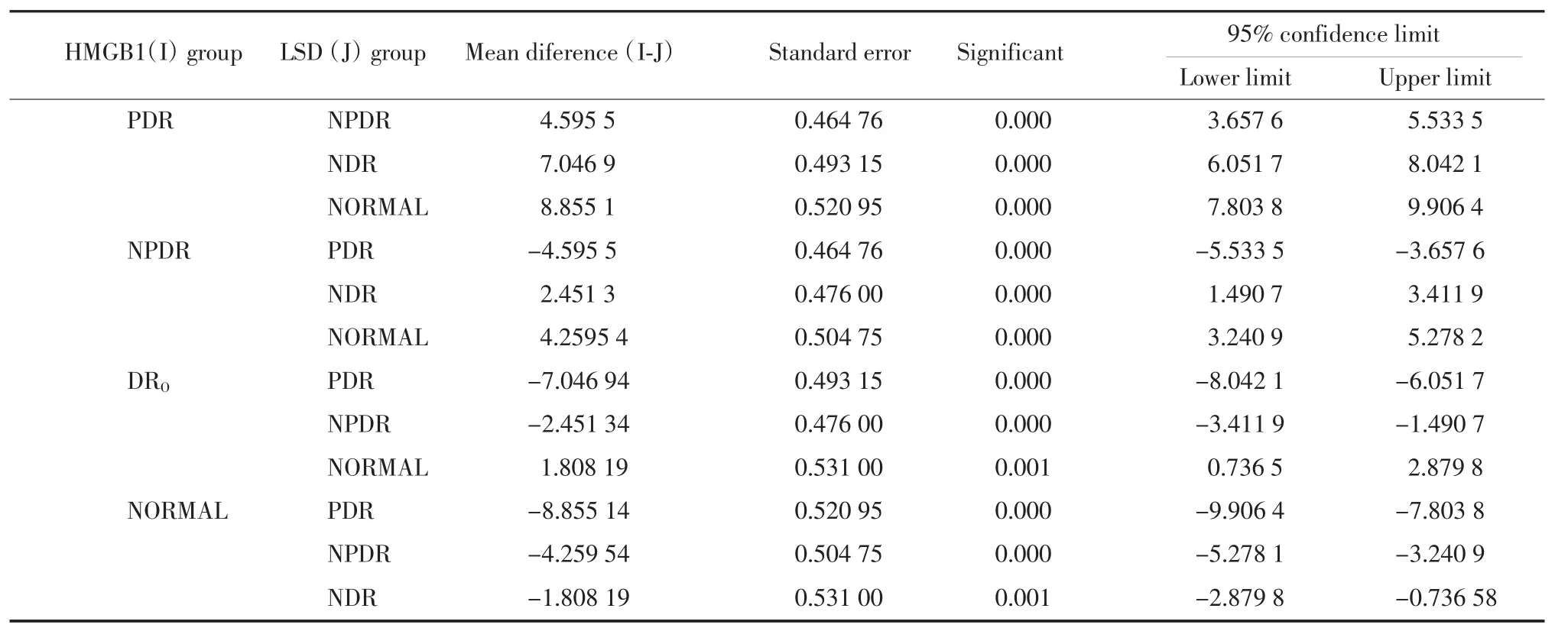
表1 各组HMGB1单因素ANOVA分析——样本多重比较Tab.1 One-ANOVA analysis of HMGB1 in different groups
2.2 血清HMGB1的水平与各临床指标的相关性研究
应用Pearson相关性分析,HMGB1与HbAC1具有明显正相关,差异有统计学意义(r=0.736,P<0.01);与空腹血糖、高密度脂蛋白、低密度脂蛋白、甘油三酯和总胆固醇无显著相关性。
3 讨论
本研究检测了PDR、NPDR和DRO的糖尿病患者,以及正常人血清HMGB1的水平。初步结果显示糖尿病患者血清内HMGB1水平高于正常人。随着DR的出现及病情的发展DR患者的血清HMGB1水平逐渐增高。这表明HMGB1在DR的发展过程中发挥了一定的作用。
HMGB1是广泛存在于真核细胞核中,高度保守的非组蛋白核蛋白,具有稳定核酸结构,调节转录和基因表达等多种功能[4,5]。它可被受刺激的单核巨噬细胞主动分泌或由坏死的细胞被动释放到细胞外,细胞外的HMGB1可诱导细胞分化、触发及调节炎症等作用[6]。动物实验[7]也显示糖尿病组织内HMGB1高表达。在增殖性DR患者的玻璃体内HMGB1和炎症标记物明显增高[8],这表明炎症反应在DR的进展中发挥了重要作用。Biscetti等[9]发现在糖尿病病例的组织中,HMGB1可促进缺血组织内的新生血管生成,这一过程有VEGF的参与。应用HMGB1抗体可明显减轻炎性损伤。HMGB1合成抑制剂正丁酸钠可降低组织HMGB1表达,同时组织TNF-α表达明显下调,组织炎性反应减轻,抗炎介质IL-10表达增强。高糖诱导的HMGB1释放可诱导糖尿病大鼠肾损伤,其机制可能是RAGE参与的NF-κB的活化作用[10]。我们前期研究显示在急性缺血再灌注损伤的视网膜中存在着HMGB1和ROS的表达增高[11]。与早期炎性介质相比,HMGB1虽变化较晚,但持续时间明显延长。
以上研究提示,DM患者血清HMGB1高于正常人,作为晚期致炎因子的HMGB1有可能参与了DR的炎性反应。而PDR患者血清HMGB1水平明显高于NPDR患者,这提示HMGB1的升高可能在一定程度上反映在DR的发展过程中炎性反应的轻重。HMGB1有可能成为预测及评估DR病情的重要炎症标志物。另外,HbAC1作为血糖控制的主要监测指标之一,对DR的监测和治疗有着重要的意义[12],本文发现HMGB1与Hb具有显著的相关性,提示HMGB1可能与糖尿病患者糖代谢异常有关,控制HMGB1的表达有可能对DR的发生发展具有一定的保护作用,但其具体机制还需进一步证实。
目前,HMGB1靶向治疗研究逐渐为人们所关注。抗HMGB1抗体、丙酮酸乙脂等在急性损伤型动物实验中用来拮抗晚期炎症HMGB1的表达,能明显拮抗HMGB1所致的急性损伤。因此,在本研究的基础上,进一步寻找出对视网膜炎性反应进行拮抗、具有视网膜保护作用的方法,将会对DR的预防和治疗具有重要的临床意义。
[1]Yang H,Huang Y,Chen X,et al.The role of CTGF in the diabetic rat retina and its relationship with VEGF and TGF-beta,elucidated by treatment with CTGFsiRNA [J].Acta Ophthalmol,2010,88(6):652-659.
[2]Oh IK,Kim SW,Oh J,et al.Inflammatory and angiogenic factors in the aqueous humor and the relationship to diabetic retinopathy[J].Curr Eye Res,2010,35(12):1116-1127.
[3]El-Asrar AM,Nawaz MI,Kangave D,et al.High-mobility group box-1 and biomarkers of inflammation in the vitreous from patients with proliferative diabetic retinopathy[J].Mol Vis,2011,17(6):1829-1838.
[4]Kawabata H,Setoguchi T,Yone K,et al.High Mobility Group Box 1 Is Upregulated After Spinal Cord Injury and Is Associated With Neuronal Cell Apoptosis[J].Spine,2010,35(11):1109-1115.
[5]Volz HC,Seidel C,Laohachewin D,et al.HMGB1:the missing link between diabetes mellitus and heart failure [J].Basic Res Cardiol,2010,105(6):805-820.
[6]Ulloa L,Messmer D.High-mobility group box 1 (HMGB1)protein:friend and foe[J].Cytokine Growth Factor Rev,2006,17(3):189-201.
[7]Soro-Paavonen A,Watson AM,Li J,et al.Receptor for advanced glycation end products(RAGE)deficiency attenuates the development of atherosclerosis in diabetes [J].Diabetes,2008,57 (9):2461-2469.
[8]El-Asrar AM,Nawaz MI,Kangave D,et al.High-mobility group box-1 and biomarkers of inflammation in the vitreous from patients with proliferative diabetic retinopathy[J].Mol Vis,2011,17:1829-1838.
[9]Biscetti F,Straface G,De Cristofaro R,et al.High-mobility group box-1 protein promotes angiogenesis after peripheral ischemia in diabetic mice through a VEGF-dependent mechanism [J].Diabetes,2010,59(6):1496-1505.
[10]Kim J,Sohn E,Kim CS,et al.The role of high-mobility group box-1 proteininthedevelopmentofdiabeticnephropathy[J].AmJNephrol,2011,33(6):524-529.
[11]Yang H,Hirooka K,Liu Y,et al.Deleterious role of anti-high mobility group box 1 monoclonal antibody in retinal ischemia-reperfusion injury[J].Cur Eye Res,2011,36(11):1037-1046.
[12]马金力,朱成义.糖尿病视网膜病变与糖化血红蛋白的关系[J].首都医科大学学报,2011,32(4):1006-1007.
