生态湖水中氨氮含量的测定*
2012-08-29冯秀芳
冯秀芳
(河南机电高等专科学校,河南 新乡 453000)
氨氮(NH3- N)是以游离氨(NH3)或铵盐(NH4+)形态存在于水中,氨氮是水体中的营养素,可导致水富营养化现象产生,是水体中的主要耗氧污染物,对鱼类及某些水生生物有毒害。当水中氨氮含量增高时,提示可能存在人畜粪便的污染,且污染时间不长。水中氨氮的来源主要为生活污水中含氮有机物受微生物作用的分解产物、某些工业废水以及农田排水。氨氮的测定方法通常有纳氏试剂分光光度法、气相分子吸收法,苯酚-次氯酸盐(或水杨酸-次氯酸盐)比色法和电极法等[1]。纳氏试剂分光光度法具有操作简便、灵敏等特点,方法检测限为:0.025mg/L~2mg/L。选取我校生态湖为监测对象,用纳氏试剂分光光度法测定湖水中氨氮的含量。
1 实验部分
1.1 主要实验仪器和设备
722N 分光光度计(20mm 比色皿);科析80-1电动离心机;梅特勒电子天平AB54-S;有机玻璃定深采水器;1L 全玻璃蒸馏器。
1.2 试剂
所用的试剂均使用分析纯,实验用水为无氨水。
1)无氨水,在无氨环境中用下述方法制备:
将1000mL 的蒸馏水,加0.1mL 硫酸(ρ=1.84g/mL),在全玻璃蒸馏器中重蒸馏,弃去前50mL 馏出液,然后将约800mL 馏出液收集在带有磨口玻璃塞的玻璃瓶内。每升馏出液加10g 强酸性阳离子交换树脂(氢型)。
2)纳氏试剂按下列方法配制[2]
称取15.0g 氢氧化钾(KOH),溶于50mL 水中,冷却至室温。
称取5.0g 碘化钾,溶于10mL 水中,在搅拌下,将2.50g 二氯化汞粉末多次加入碘化钾溶液中,直到溶液呈深黄色或出现淡红色沉淀溶解缓慢时,充分搅拌混合,并改为滴加二氯化汞饱和溶液,当出现少量朱红色沉淀不再溶解时,停止滴加。
在搅拌下,将冷却的氢氧化钾溶液缓慢加入到上述二氯化汞和碘化钾的混合液中,并稀释至100mL,于暗处静置24h,倾出上清液,贮于聚乙烯瓶中,用橡皮塞或聚乙烯盖子盖紧,存放暗处,可稳定1个月。
3)酒石酸钾钠溶液,ρ=500g/L
4)硫酸锌溶液,ρ=100g/L
5)氢氧化钠溶液,c(NaOH)=1mol/L
6)氢氧化钠溶液,ρ=250g/L
7)盐酸溶液,c(HCl)=1mol/L
8)硼酸溶液,ρ=20g/L
9)溴百里酚蓝指示剂,ρ=0.5g/L。
10)淀粉-碘化钾试纸
11)氨氮标准溶液
①氨氮标准贮备溶液,ρN=1000ug/mL
称取3.8190g 氯化铵,优级纯,在100℃~105℃干燥2h,溶于水中,移入1000mL 容量瓶中,稀释至标线。
②氨氮标准工作溶液,ρN=10ug/mL。
吸取5.00mL 氨氮标准贮备溶液于500mL 容量瓶中,稀释至标线刻度。临用前配制。
1.3 标准曲线的绘制
在8 个50 mL 比色管中,分别加入0.00、0.50、1.00、2.00、4.00、6.00、8.00 和10.00mL 氨氮标准工做溶液,其所对应的氨氮含量分别为0.0、5.0、10.0、20.0、40.0、60.0、80.0 和100ug,加水至标线。加入1.0mL 酒石酸钾钠溶液,摇匀,再加入纳氏试剂1.5mL,摇匀。放置10min 后,在波长420nm 下,用20mm 比色皿,以水做参比,测量吸光度。绘制曲线如图1 所示。
1.4 样品的采集与保存
采集湖面下0.5 米处的水样于玻璃试剂瓶并加硫酸使水样酸化至pH≤2,同时做样品空白,填写采样记录单。一周内尽快分析。
1.5 样品的预处理
采用絮凝沉淀法。100mL 样品中加入1mL10%硫酸锌溶液和0.1mL~0.2mL 氢氧化钠溶液,调节pH 约为10.5,混匀,放置使之沉淀。用高速离心机离心处理10min,取上清液分析测试。
1.6 样品测定
取经预处理的水样50mL,按与校准曲线相同的步骤测量吸光度,测定3 份平行样,同时做空白实验。
2 结果与讨论
2.1 标准曲线
氨氮标准曲线测定结果见表1。
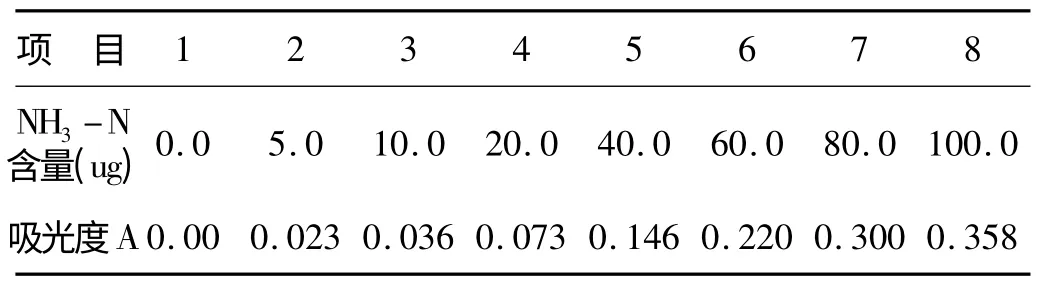
表1 氨氮标准曲线测定结果

将a、b 代入回归方程,得出线性回归方程式为y=0.0036x+0.0017 。
相关系数

经计算求得回归线相关系数r=0.9999,说明x和y 之间相关性显著,并有较好的线性关系,绘制标准曲线见图1。
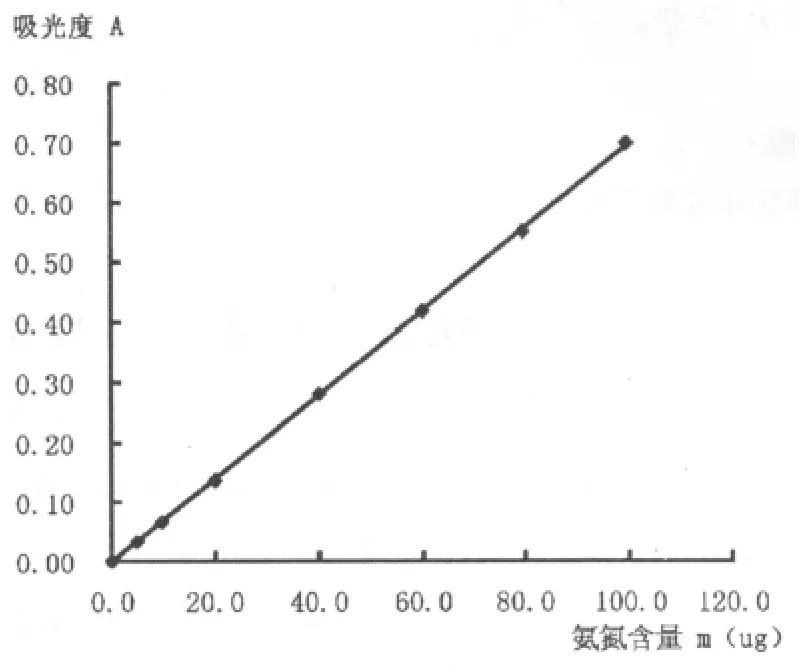
图1 氨氮标准曲线
2.2 结果计算与讨论
按与校准曲线相同的步骤测量水样的吸光度,同时做空白实验,测定结果为:A1=0.040 A2=0.041 A3=0.041 空白样吸光度A0=0.005。
地表水环境质量标准(GB 838—002)规定Ⅱ类水质中氨氮(NH3-N)含量应不大于0.50 ㎎/L,Ⅰ类水质标准规定应不大于0.15 ㎎/L,该人工湖水中氨氮含量为0.20 ㎎/L,符合Ⅱ类水质标准。
3 注意事项
在实验的过程中,响测定结果的主要因素除了温度、显色时间和显色剂的加入量外[3],还需要特别注意以下几点:
3.1 纳氏试剂的配制
为了保证纳氏试剂有良好的显色能力,配制时务必控制氯化汞的加入量,至微量氯化汞红色沉淀不再溶解时为止。配制100mL 纳氏试剂所需HgCl2与KI 的用量之比约为2.3∶ 5。在配制时为了加快反应速度、节省配制时间,可低温加热进行,防止红色沉淀的提前出现。
3.2 酒石酸钾钠的配制
酒石酸钾钠试剂中铵盐含量较高时,仅加热煮沸或加纳氏试剂沉淀不能完全除去氨。此时采用加入少量氢氧化钠溶液,煮沸蒸发掉溶液体积的20%~30%,冷却后用无氨水稀释至原体积。
3.3 絮凝沉淀
滤纸中含有一定量的可溶性铵盐,定量滤纸中含量高于定性滤纸,建议采用定性滤纸过滤,过滤前用无氨水少量多次淋洗。这样可减少或避免滤纸引入的测量误差。
[1]水和废水监测分析方法[M].第4 版.北京:中国环境科学出版社,2002.
[2]邓鹂,顾晓燕,陈静,等.纳氏试剂分光光度法测定氨氮的质量控制[J].广州化工,2011,39(19):84-87.
[3]高春燕.纳氏试剂比色法测定水中氨氮的影响因素分析[J].环境科学导刊,2010,29(5):92-94.
