尤瑞克林治疗进展性脑梗死的Meta分析
2012-08-21郑续金露王小同陈永青邵蒙蒙
郑续,金露,王小同,陈永青,邵蒙蒙
(温州医学院附属第二医院 康复、脑科中心,浙江 温州 325000)
进展性脑梗死是卒中的原发性神经系统症状及体征在正规治疗后仍进行性加重的一种临床过程,一般认为在发病后6 h至1周内进展,多数在起病48 h内出现[1-2]。经常规治疗后病情仍难以控制,多有病灶扩大、新发和出现并发症等,使致残率和病死率明显增加。对此目前尚缺乏有效的治疗手段。注射用尤瑞克林是由广东天普生化医药股份有限公司研制的一种新药,经国家食品药品监督管理局批准,已于2000年开始用于临床研究。本研究应用Meta分析法对以往尤瑞克林治疗进展性脑梗死的研究结果进行综合分析,探讨尤瑞克林对改善进展性脑梗死患者的功能缺损及日常生活能力是否有效。
1 资料和方法
1.1 资料来源 通过计算机检索中国生物医学文献数据库(CBM)、中国期刊全文数据库(CNKI)、万方、维普、Pubmed等数据库,结合参考文献追溯、手工检索神经及康复科相关杂志、网上查询(scholar.google.com)等方法,收集国内外自1978年1月至2011年6月间发表的有关尤瑞克林治疗进展性脑梗死的文献。中文检索词:进展性脑梗死、尤瑞克林、人尿激肽原酶、凯力康;英文检索词:progressive cerebral infarction,progression in acute ischemic stroke,Urinary Kallidinogenase。
1.2 纳入语种 纳入语种为中文。
1.3 文献的纳入与排除 纳入标准:①进展性脑梗死的诊断符合全国第四届脑血管病学术会议修订的诊断标准[3],经颅脑CT或MRI检查证实,起病6 h后经正规治疗在1周以内病情仍有进行性加重。②提供治疗前、后患者NIHSS评分、ADL评分、CSS评分、恶化数中一项或多项的结果(均数、标准差等)。③临床疗效的评定参照脑卒中患者的临床神经功能缺损程度评分标准和临床疗效评定标准[4]进行。基本痊愈:功能缺损评分减少90%~100%,病残程度0级;显著进步:功能缺损评分减少46%~89%,病残程度1~3级;进步:功能缺损评分减少18%~40%;无变化:功能缺损评分减少或增加18%以内;恶化:功能缺损评分增加18%以上;死亡。其中将恶化加上死亡的人数除以总人数求得恶化率作为分析。④治疗组加用尤瑞克林,尤瑞克林的治疗疗程为7~21 d,选取第14天患者的各项指标进行评分。
排除标准:①除常规用药外,治疗组联用其他药物的;②综述、基础研究等相关文献;③重复文献。
1.4 文献筛选、质量评价与数据提取 根据纳入和排除标准通过阅读文献题目和摘要进行初筛,再阅读全文进一步筛选出相关文献;从入选的文献里提取的数据信息包括治疗前后患者恶化及死亡的人数、NIHSS评分、ADL评分、CSS评分的结果(均数、标准差等);患者的临床资料(例数、年龄、性别、病程等);尤瑞克林的治疗方法(用量、给药方式、疗程等)。文献筛选和数据的收集由2名研究者独立完成,若有分歧,再通过讨论或由另一位研究者协助解决。
1.5 统计学处理方法 采用Cochrane协作网提供的RevMan5.0.25软件进行数据处理。①Meta分析方法:对计量资料应用连续变量(均数)分析方法进行分析;对计数资料应用Mantel-Haenszel法计算其相对危险度(relative risk,RR)进行分析。②异质性检验(Q):应用x2检验分析各研究间异质性。若P>0.05,表明各研究间同质,使用固定效应模型分析;若P≤0.05,则说明各研究间异质,分析其异质性来源并去除异质性。如异质性仍存在,使用随机效应模型分析。③效应大小:对固定效应模型计算合并效应,对随机效应模型计算加权平均效应,用d值表示。对于测量单位相同的连续性变量使用加权均数差(weighted mean difference,WMD),当各研究结局指标单位不一致,或均数差异较大,则使用标准化均数差(standardized meandifference,SMD)。④计算效应:计算95%可信区间(confidence interval,CI)并做统计推断,只有当95%CI不包含零时,效应大小才具有统计学意义。
2 结果
2.1 文献检索及质量评价 共检索到中文文献26篇,英文文献0篇,经过初筛和再次筛选共有11篇文献符合标准入选,其中有文献[6]、[11]由于纳入的患者为同一医疗单位存在部分重复,相关结局指标只纳入其中一篇的文献结果。共纳入11个研究中有10个研究明确指出为随机对照试验,其中有2个研究指出随机产生方法为随机数字表法,其余研究随机方法不明确。所有研究均未明确指出是否采用分配隐藏。见表1。
2.2 Meta分析 对文献[6]、[9]、[14-15]中共175例尤瑞克林组及172例对照组的NIHSS评分进行Meta分析,结果显示其同质性检验x2=1.82,P>0.05,具有同质性,故使用固定效应模型分析;其综合效应量d=-1.88,95%CI(-2.56,-1.19),z=5.37,P<0.05,尤瑞克林组与对照组之间NIHSS评分的差异具有统计学意义。见图1。

表1 入选文献的特征

图1 尤瑞克林组和对照组NIHSS评分的Meta分析
对文献[5]、[7]、[10]、[12-13]中共150例尤瑞克林及153例对照组的CSS评分进行Meta分析,结果显示其同质性检验x2=11.67,P<0.05,具有异质性,故使用随机效应模型分析;由于各组均数差异较大,故使用SMD计算其综合效应量d=-1.18,95%CI(-1.61,-0.75),z=5.35,P<0.05,尤瑞克林组与对照组之间CSS评分的差异具有统计学意义。见图2。

图2 尤瑞克林组和对照组CSS评分的Meta分析
对文献[7-8]、[11]、[13]中共229例尤瑞克林及208例对照组的ADL评分进行Meta分析,结果显示其同质性检验x2=8.70,P<0.05,具有异质性,故使用随机效应模型分析;其综合效应量d=14.79,95%CI(7.54,22.05),z=3.99,P<0.05,尤瑞克林组与对照组之间ADL评分的差异具有统计学意义。见图3。
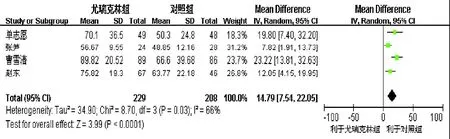
图3 尤瑞克林组和对照组ADL评分的Meta分析
对文献[5]、[7]、[10-11]、[13-15]中281例尤瑞克林组及279例对照组的恶化率(恶化+死亡的人数/总人数)进行Meta分析,结果显示其同质性检验x2=1.56,P>0.05,具有同质性,故使用固定效应模型分析;其综合效应量d=0.32,95%CI(0.15,0.70),z=2.87,P<0.05,尤瑞克林组与对照组之间恶化率的差异具有统计学意义。见图4。

图4 尤瑞克林组和对照组恶化率的Meta分析
3 讨论
进展性脑梗死的发病机制目前尚不清楚,多数学者认为其是多种危险因素及病理机制共同作用的结果,主要与不稳定血栓的形成、再灌注损伤、脑血管狭窄、高血压、糖尿病、高血脂及药物使用不当等因素有关。
动物实验已证实,脑缺血后激肽系统被激活,导致内源性激肽释放增加,一方面可致一些炎症细胞因子和氧化自由基在局部脑组织内的产生和释放增加,扩张脑血管、损害内皮细胞、增加毛细血管通透性,从而破坏血脑屏障[16];另一方面又可通过抑制局部神经细胞凋亡、抑制炎症反应及促进血管和神经再生等机制发挥神经保护效应[17]。尤瑞克林是自人尿液中提取得到的蛋白水解酶,能将激肽原转化为激肽和血管舒张素。激肽系统是通过B1及B2二类受体发挥其活性,尤瑞克林作用于激肽原后形成胰激肽,后者及其进一步降解产物能与B1受体结合发挥其扩张微动脉的活性;而B1受体仅在组织经受缺血等损伤后,由损伤的组织血管内皮细胞诱导而生成;因此,它只选择性地扩张缺血区的脑血管,从而提高缺血部位脑血流量及改善脑组织对葡萄糖及氧的摄取[18-19]。尤瑞克林对脑梗死的疗效确切且具有较好的安全性,这已被许多临床试验所证实[20]。
Meta分析是指对某一个特定的研究问题的多项研究结果进行综合分析的一系列过程,目的在于增加样本含量,减少随机误差所造成的假阴性、假阳性的可能性,增大检验效能,进而提供较为可靠的结论[21]。本Meta分析旨在探讨尤瑞克林对进展性脑梗死患者的功能缺损的改善是否有效,共纳入11个研究,分别对其中的NIHSS评分、CSS评分及恶化率进行Meta分析,结果显示尤瑞克林治疗组相较对照组,NIHSS评分、CSS评分、恶化率降低,差异均具有统计学意义。其作用机制可能是由于尤瑞克林选择性地扩张缺血脑组织的微动脉,改善脑局部血供,加快缺血半暗带的恢复和缩小脑梗死范围[22],从而改善脑组织对葡萄糖和氧的摄取;通过抑制炎症反应及神经细胞和神经胶质细胞的凋亡[23],一定程度上减轻脑再灌注损伤;同时它还能抑制血小板的聚集,减轻血液黏稠,增强红细胞的变形能力和氧解离能力。另外,还对纳入的4篇文献中共229例尤瑞克林及208例对照组的ADL评分进行Meta分析,结果显示尤瑞克林组较对照组ADL评分升高,差异具有统计学意义;因此,尤瑞克林对改善患者的日常生活能力也具有一定疗效。
但是,Meta分析属于观察性研究,因而其结果可能会受到偏移、混杂等因素的影响。本Meta分析所纳入的11个研究中有10个研究为随机对照试验,其中只有有2个研究明确指出随机产生方法为随机数字表法,所有研究均未明确指出是否采用分配隐藏,其研究设计及质量可能存在部分不足;另外,本Meta分析中尤瑞克林组与对照组的CSS评分及ADL评分的同质性检验显示各研究之间存在异质性,可能是由于各研究之间未对进展性脑梗死进行明确分型,如梗死部位、梗死程度等不一样所致;采用倒漏斗图评价发表偏移,显示部分倒漏斗图不对称,可能存在发表偏倚,研究样本量少及阴性结果发表较少可能是其原因之一;由于英文文献检索到0篇,其他语种未检索,也可能存在语种偏倚。
总之,本Meta分析结果显示尤瑞克林对改善进展性脑梗死患者的功能缺损有效,为进展性脑梗死的治疗提供了一种新的可能的选择。同时,尤瑞克林对进展性脑梗死患者的日常生活能力也有一定的改善作用,早期使用可以提高患者的生存质量,使患者能够更好地回归社会。但是,鉴于目前对尤瑞克林治疗进展性脑梗死的临床研究均存在不同程度的设计及质量上的问题,故尚需开展更多的大样本、多中心随机对照临床试验以获得进一步的证据,并对其安全性作进一步的评估。
[1] 黄如训.进展性脑卒中的发病机制和危险因素[J].国外医学:脑血管疾病分册,2003,1(3):3-6.
[2] 王维治.神经病学[M].5版.北京:人民卫生出版社,2004:135.
[3] 各类脑血管病疾病诊断要点[J].中华神经科杂志,1996,29(6):379.
[4] 全国第四届脑血管学术会议.脑卒中患者临床神经功能缺损程度评分标准及临床疗效评定标准[J].中华神经科杂志,1996,29(6):381-383.
[5] 黄健康,柯将琼,胡蓓蕾.尤瑞克林治疗进展性脑梗死疗效观察[J].实用医学杂志,2007,23(23):3753-3754.
[6] 温德树,吴志武,罗日向,等.尤瑞克林治疗急性进展性脑梗死近期疗效观察[J].中国卒中杂志,2009,4(2):113-116.
[7] 张笋,冯连元,王雪笠,等.尤瑞克林治疗进展性脑梗死的临床观察[J].华北国防医药,2009,21(3):22-23.
[8] 赵东,付志新,张津华.尤瑞克林治疗进展性脑梗死疗效观察[J].中国实用神经疾病杂志,2010,13(11):77-79.
[9] 尹琳,王丹.尤瑞克林治疗急性进展性脑梗死临床疗效观察[J].神经疾病与精神卫生,2010,10(6):589-591.
[10] 王夏红,何文龙,赵建民.尤瑞克林治疗进展性脑梗死的疗效观察[J].中华脑血管病杂志(电子版),2010,4(5):367-370.
[11] 曹血清,温德树,卢叶玲.尤瑞克林治疗急性进展性脑梗死的疗效观察及护理[J].中国实用护理杂志,2010,26(6):25-26.
[12] 苏建,裘丽红,张保华,等.尤瑞克林针治疗急性进展性脑梗死疗效观察[J].中国误诊学杂志,2011,11(10):2324.
[13] 单志愿.尤瑞克林治疗急性进展性脑梗死疗效观察[J].中国医药导报,2011,8(17):78-79.
[14] 卢静,王涛.注射用尤瑞克林治疗进展性脑梗死的疗效观察[J].吉林医学,2011,32(17):3434-3436.
[15] 张灏,殷国聪,牛国忠.注射用尤瑞克林治疗进展性脑梗死疗效分析[J].心脑血管病防治,2011,11(2):150-151.
[16] Storini C, Bergamaschini L, Gesuete R, et al. Selective inhibition of plasma kallikrein protects brain from reperfusion injury[J]. J pharmacol Exp Ther,2006,318(2):849-854.
[17] Xia CF, Yin H, Borlongan CV, et al. Kallikrein gene transfer protects against ischemic stroke by promoting glial cell migration and inhibitingapoptosis[J]. Hypertension,2004,43(2):452-459.
[18] Nagano H,Suzuki T,Tomogufi T,et a1. Pharmacological studies on human urinary kallidinogenase(SK-827):efects on cerebral metabolism[J]. Yakugaku Zasshi,1993,113(11):825-828.
[19] Campbell DJ.The kallikrein-kinin system in humans[J].Clin Exp pharmacol physiol,200l,28(12):l060-1065.
[20] 丁德云,吕传真,丁美萍,等.人尿激肽原酶治疗急性脑梗死多中心随机双盲安慰剂对照试验[J].中华神经科杂志,2007,40(5):306-310.
[21] 袁海,金露,王小同,等.经颅磁刺激对帕金森病运动功能康复疗效的Meta分析[J].中华物理医学与康复杂志,2010,32(12):932-934.
[22] Nagano H,Suzuki T,Nakamuru S,et a1.Pharmacological studies on human urinary kallidinogenase(SK-827):cerebral protective efects[J]. Yakugaku Zasshi,l993,1l3(11):803-809.
[23] Ling L, Hou Q, Xing S, et al.Exogenous kallikrein enhances neurogenesis and angiogenesis in the subventricular zone and the peri-infarction region and improves neurological function after focal cortical infarction in hypertensive rats[J].Brain Res,2008,1206:89-97.
