电解质的微区熔浸
2012-06-29郭永全赵晋峰邢永慧
郭永全,赵晋峰,邢永慧,郑 毅
(中国电子科技集团公司第十八研究所,天津 300384)
热电池电解质为熔融盐,目前常用的有氯化钾-氯化锂二元电解质、氟化锂-氯化锂-溴化锂三元全锂电解质、氯化锂-溴化锂-溴化钾三元氯化锂电解质和氟化锂-溴化锂-溴化钾三元氟化锂电解质等几种,以适应电池对不同指标的需求。应用中可根据电池输出功率、寿命等使用要求,选择合适的电解质;如文献[1]分析了各种熔盐电解质性能差异,并详细论述了热电池研制中,基于电池性能需求,对电解质的一般选取规律。文献[2]则介绍了多种电解质的化学组成及主要理化参数。
从理论上看,电解质的共熔点的高低、电导率的大小决定了电解质的基本特性,但在实际情形中却很复杂;许多文献对此有过专门的讨论,如氧化镁用量对电解质保持力的影响[3],混料方式对熔盐电解质粒径、形貌、孔隙率的影响[4],电解质的吸湿性能[5]等等。
在单体电池的制备过程中,粉末的成型性和单体电池的绝缘性是影响成品率的重要因素。粉末的成型性能决定于各材料的颗粒特性,如粒度和形貌特征;单体的绝缘性除了受电解质的固态电导率与纯度的影响外,亦与材料的颗粒特性有关。对负极、电解质、正极三者而言,三种材料的颗粒特性都与单体成品率密切相关,而影响最大的为电解质。当电解质材料中存在较大的颗粒时,会严重影响到单体的绝缘性能。
在熔盐电解质的研究工作中,一般利用粒度分布和松装密度来描述电解质的颗粒特性。但究竟是什么因素影响了电解质的粒度和松装密度,影响的机制又是什么,本文对此做了初步研究。
1 实验
1.1 电解质制备
按化学计量比配制好共晶盐,在一定温度下焙烧,保温,出炉,冷却后,使用粉碎机碎料,过80目或120目筛。
将熔盐与氧化镁按固定配比混合,在设定温度下恒温一定时间,出炉,冷却,球磨,过筛,干燥后制得电解质。
1.2 材料测试
在相对湿度小于4%的干燥间中,用斯柯特容量计法测定材料的松装密度;采用日立公司的S-4800扫描电子显微镜观察材料的表面形貌;采用马尔文公司的MS2000激光粒度分析仪测试材料的粒度分布。
2 结果与讨论
2.1 熔盐对电解质颗粒特性的影响
一般认为,电解质熔浸时,熔盐液化,渗入氧化镁微粒中,所以熔盐的颗粒大小并不重要;为了方便液化,熔浸均匀,习惯将熔盐粉碎,过一定目数筛网,用以配制电解质。为了验证熔盐粒径对电解质颗粒特性的影响,以不同粒度的熔盐(过筛目数不同)为原料,在相同条件下制备了三批全锂电解质,其松装密度和粒度分布中位径如表1所示。
由表1中数据可知,在其他条件相同的情形下,配制电解质所用熔盐的粒度与制得电解质的松装密度、粒径的大小呈正相关。熔盐粒度越大,对应电解质的粒径越大,松装密度越大。因此我们可以得出结论,熔盐颗粒的大小是影响电解质粒径的关键因素。
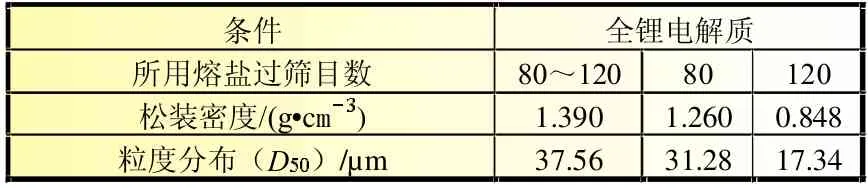
表1 不同粒度熔盐所制备电解质松装密度及粒度
电解质是由熔盐和MgO的混合物经高温烧制而成。图1为氧化镁的形貌照片,从图中可以看出,氧化镁的粒径在50 nm左右,这与文献[3,6]报道的结果基本一致。图2为过120目筛熔盐颗粒的形貌照片,其粒径大小约为6~7 μm。

图1 氧化镁形貌图
由文献[2-3]报道得知,氧化镁的密度为3.39 g/cm3,LiF-Li-Cl-LiBr熔盐的密度为2.92 g/cm3,假设电解质配制时,MgO与熔盐的质量比为1∶1,我们可以近似推导出,每个熔盐颗粒将紧密包裹至少30层的氧化镁,包裹层的厚度在1.5 μm以上。在电解质熔浸过程中,熔化了的熔盐液滴浸润周围的氧化镁粒子,同时氧化镁粒子向熔盐液滴中浸陷,但熔盐颗粒仍然保持原有独立性,熔浸作用在各微区相对独立进行。图3为微区熔浸后形成的电解质颗粒。
图4给出了微区熔浸的示意图,(A)为熔盐颗粒被氧化镁微粒包裹的示意图;(B)为不完全微区熔浸图,亦即氧化镁

图2 熔盐颗粒图

图3 电解质颗粒图
2.2 电解质中的微区熔浸
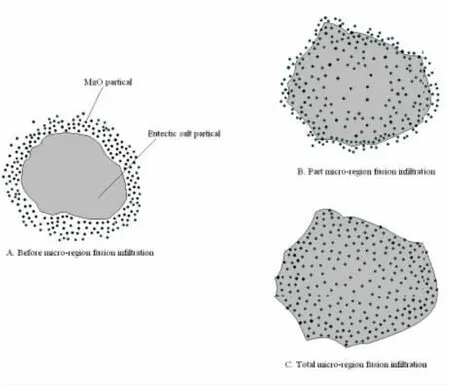
图4 微区熔浸示意图
层未能被相邻的熔盐颗粒完全熔浸吸收;(C)为完全微区熔浸示意图,氧化镁被周围的熔盐颗粒完全熔浸吸收,相邻熔浸微区相互粘连。
在完全微区熔浸的条件下,相对于各微区间不紧密的粘连,单个熔盐颗粒微区熔浸后形成的电解质颗粒较难破碎,所以,这从理论上验证了2.1中的结论,即熔盐颗粒越大,微区熔浸后电解质的粒径越大。
2.3 不完全微区熔浸对电解质组成的影响
在电解质的制备过程中,MgO过量或者熔盐颗粒过大是导致不完全微区熔浸的重要因素。如果氧化镁用量过多,熔浸时会有部分氧化镁不能与熔盐浸润结合,图5即为氧化镁过量时微区浸润的界面图。从图中可以清晰看到最外层粘附的氧化镁颗粒。与此同时,熔盐颗粒的增大,将使未被浸润的氧化镁颗粒增多,加剧电解质的不完全微区熔浸。

图5 熔浸微区界面图
以大颗粒的熔盐为原料,将熔浸后的电解质进行粉碎过筛处理,测量过筛粉与未能过筛粉的氧化镁含量,测试结果如表2所示。经对比可得,未能过筛粉中的MgO含量明显低于过筛粉。这是因为大颗粒熔盐导致不完全微区熔浸,使电解质中存在纯粹的氧化镁微粒,这些微粒很容易过筛;另外,在难于破碎的大熔盐颗粒所形成的熔浸微区中央,浸裹的氧化镁颗粒偏少,最终导致过筛粉与未能过筛粉中MgO含量的差异。
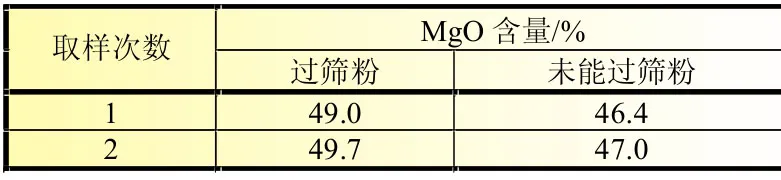
表2 过筛粉与未能过筛粉成分分析结果
基于上述分析,在配制电解质时,不仅要考虑粘结剂氧化镁的用量,还应严格控制熔盐粒径的大小。表3给出了熔盐破碎后的粒度分布和松装密度数据。由表可知,在相同的破碎条件下,LiCl-KCi熔盐颗粒粒径明显大于LiF-LiCl-LiBr熔盐。同为LiF-LiCl-LiBr熔盐,分别经球磨和机械粉碎处理,粒径差异也较大。

表3 熔盐粒径分布与松装密度
所以,在熔盐制备过程中,不能以筛网目数作为控制熔盐粒径大小的主要方法,应准确测量其粒度分布,通过控制熔盐的粒径,避免电解质制备过程中的不完全微区熔浸。
3 结论
在熔盐电解质的制备过程中,熔浸作用是以单个熔盐颗粒及其周围包裹的氧化镁层为单元的微区浸润,熔盐颗粒越大,熔浸后形成的单个电解质颗粒越大,且较难破碎,所以,熔盐颗粒的大小是影响电解质粒径的决定因素。配制电解质时,应考虑到熔盐粒径对氧化镁用量的影响,以减少不完全微区熔浸的产生。
[1]高俊丽.热电池用熔融盐电解质性能实验研究[J].上海航天,2000(4):62-64.
[2]MASSET P,GUIDOTTI R A.Thermal activated(thermal)battery technology PartⅡ.Molten salt electrolytes[J].Power Sources,2007,164:397-414.
[3]MASSET P,SCHOEFFERT S,POINSO J Y,et al.Retained molten salt electrolytes in thermal batteries[J].Power Sources,2005,139:356-365.
[4]SCHISSELBAUER P F,BOTT E,LIU L S.Lithium silicon/iron disulfide(LiSi/FeS2)thermal battery for sensor and fuze applications[C]//42ndPower Sources Conference.[S.l.]:42ndPower Sources Conference,2006:285-288.
[5]MASSET P,POINSO J Y,POIGNET J C,et al.Water update by salts during the electrolyte processing for thermal batteries[J].Power Sources,2004,137:140-144.
[6]MASSET P.Iodode-based electrolytes:A promising alternative for thermal batteries[J].Power Sources,2006,160:688-697.
