利拉鲁肽对糖尿病前期大鼠胰岛海马胆碱能神经刺激肽前体蛋白的影响*
2012-06-27郭南京徐艳花蔡德鸿
高 飞,陈 宏,张 桦,郭南京,徐艳花,蔡德鸿
糖尿病前期是介于正常血糖和糖尿病之间的糖代谢紊乱状态,发病机制与胰岛β细胞受损[1]及胰岛素抵抗有关[2]。多项研究证实[3-4],糖尿病前期发生糖尿病、心血管疾病及卒中的风险较高,总死亡率也明显增加,因此对糖尿病前期的干预至关重要。促丝裂原活化蛋白激酶(mitogen-activated protein kinase,MAPK)信号转导途径和胆碱能神经受体系统,分别在胰岛β细胞增殖与胰岛素分泌中起重要作用。作为MAPK信号转导途径的特异性抑制剂,海马胆碱能神经刺激肽前体蛋白(HCNP-pp)可抑制MAPK信号转导途径,减少细胞增殖;HCNP-pp氨基末端经类糜蛋白酶裂解为含11个氨基酸残基的多肽,即海马胆碱能神经刺激肽(HCNP),HCNP在中枢神经系统可促进乙酰胆碱合成,影响胆碱能神经受体系统[5]。胰高血糖素样多肽(glucagon-like peptide-1,GLP-1)为一种肠促胰岛激素,不但可结合自身受体,作用于cAMP-PKA途径引起胰岛素分泌,还可与乙酰胆碱协同活化胆碱能神经受体而引起胰岛素分泌[6]。此外,细胞培养及动物实验均已证实,GLP-1可激活MAPK信号转导途径,促进胰岛β细胞增殖[7]。然而,GLP-1引起的上述作用是否与HCNP-pp和HCNP相关,目前尚无文献报道。本研究中,对糖尿病前期OLETF大鼠腹腔注射不同剂量的GLP-1类似物利拉鲁肽,探究了利拉鲁肽影响胰岛β细胞增殖和促胰岛素释放的可能机制。
1 材料和方法
1.1 动物分组与处理
OLETF大鼠(日本大冢制药株式会社德岛研究所惠赠)为胆囊收缩素-A受体基因敲除鼠,因进食量大、体重增加迅速、伴有高胰岛素血症及血糖升高等,可自发2型糖尿病。LETO大鼠是OLETF大鼠同品系自然生长鼠,可作为OLETF大鼠阴性对照组(LETO组)。所有雄性4周龄大鼠均在南方医科大学实验动物中心清洁级饲养室普通饲料饲养,温度(21±2)℃,光照14 h,湿度(60±15)%。所有动物饲养8~10周后,禁食15 h,行口服葡萄糖耐量试验(葡萄糖2 g/kg,胃管灌入),以葡萄糖氧化酶法(雅培血糖仪,美国)分别检测30,60,90,120 min时鼠尾静脉血糖,糖尿病诊断标准按国际大鼠糖尿病标准,符合血糖峰值大于16.8 mmol/L或餐后2 h血糖大于11.1 mmol/L即为糖尿病前期。分别于给药2,4,6,8,10,12 周末再次行口服葡萄糖耐量试验,测各组大鼠体重,并应用酶联免疫吸附试剂盒(武汉中美科技有限公司)检测空腹血清胰岛素。将处于糖尿病前期的OLETF大鼠随机分为L-100组、L-200组和 PBO组(安慰剂组),每组 8只。L-100组和L-200组大鼠分别给予100μg/kg和200μg/kg利拉鲁肽(丹麦诺和诺德公司,剂型为预填充注射笔,规格为3 mL∶18 mg)及0.9%氯化钠注射液1.0 mL/kg,每日2次,腹腔内注射。LETO组和PBO组大鼠给予0.9%氯化钠注射液腹腔内注射。每两周行口服葡萄糖耐量试验,12周后以50%戊巴比妥钠腹腔麻醉,提取胰腺组织,行免疫组化染色及蛋白印迹、实时定量PCR等试验。
1.2 方法
免疫组织化学染色:取经10%甲醛固定的标本,24 h内石蜡包埋,酒精梯度脱水后,行胰岛素免疫组化染色,光镜下观察胰岛细胞形态,应用Image J软件分析胰岛素阳性表达细胞密度值(positivecell denisity,PCD)。
胰腺组织相关基因荧光定量分析:应用Trizol液(Invitrogen公司,美国)裂解胰腺组织,按说明书提取总RNA,-80℃保存。将 HCNP -pp、胆碱乙酰转移酶(Choline acetyltransferase,ChAT)、3型毒蕈碱受体(type 3 muscarinic receptor,M3R)和GLP-1R基因mRNA序列进行分析,设计特异性引物:HCNP-pp上游引物序列为5'-TGGTGTATGAGCAGGAGCAG-3',下游引物序列为5'-TCCCAGGTGGTA CTTCTTGC-3',扩增片段长度116 bp;ChAT上游引物序列为5'-TTCCAA GACACCAAT GACCA-3',下游引物序列为5'-AGT GGCTGT CCA GCA GAGTT-3',扩增片段长度85 bp;M3R上游引物预序列为5'-CAT CATTGGCAA CAT CCT TG-3',下游引物序列为5'-AGGCCA GGCTTA AGA GGA AG-3',扩增片段长度89 bp;GLP-1R上游引物序列为5'-CCT GAG GAA CAGCTCCTG TC-3',下游引物序列为 5'-CTG GTG CAG TGCAAG TGT CT-3',扩增片段长度119 bp。引物均由上海生工生物工程技术服务有限公司合成。应用ABI 7500 Real-time PCR 仪(Applied Biosystems Inc,美国)和 Syber Green RNA扩增试剂盒(Takara生物技术公司,中国),采用一步法进行RT-PCR反应,反应方案依据试剂盒操作步骤。实时定量PCR体系(20μL):实时荧光定量试剂2×SYBR Premix Ex TaTM 10μL,ROXReference DyeⅡ0.4μL,10μmol/μL 上、下游引物各 0.4μL,cDNA模板 1.0μL,双蒸水 17.8μL。反应条件:94℃预反应5 min;94℃ 30 s,60℃ 30 s,72℃ 30 s,40个循环,于每个循环延伸反应最后时刻收集荧光信号。
胰腺组织HCNP-pp和GLP-1R蛋白表达分析:采用Western印迹方法,以增强化学发光法显示蛋白条带,用Universal hoodⅡ凝胶成像系统(捷达科技发展有限公司,中国)成像,ImageJ软件分析条带灰度值,β-actin作为内参照。一抗购于美国Santa Cruz公司,辣根过氧化物酶标记的二抗、增强化学发光试剂盒和硝酸纤维素膜购于美国Amersham公司。
1.3 数据处理及统计分析
数据均采用SPSS13.0软件进行统计学处理分析,计量资料用X±s表示,对结果进行正态性及方差齐性检验,组间比较用单因素方差分析检验。P<0.05为差异有显著性意义。
2 结果
2.1 大鼠体重、口服葡萄糖耐量试验及空腹胰岛素
经12周药物处理,PBO组大鼠体重、血糖、空腹血清胰岛素均明显高于L-100组,L-200组及LETO组,差异具有统计学意义。见表1。
2.2 胰岛免疫组化形态学分析
光镜光镜下观察,LETO组胰岛形态规则、结构完整,胰岛内PCD分布均匀;PBO组胰岛内PCD明显减小,分布不均匀;L-100组胰岛内PCD较PBO组无明显改善,L-200组胰岛形态明显改善,胰岛内PCD较PBO组明显增加。见图1和表1。
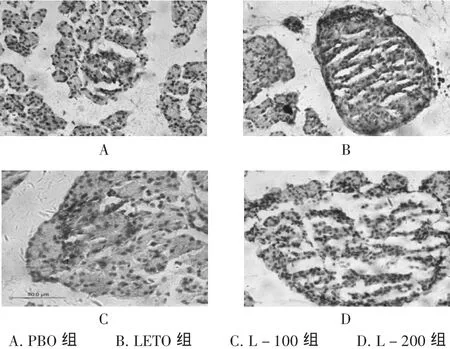
图1 光镜下胰腺胰岛素免疫组化染色(×400)
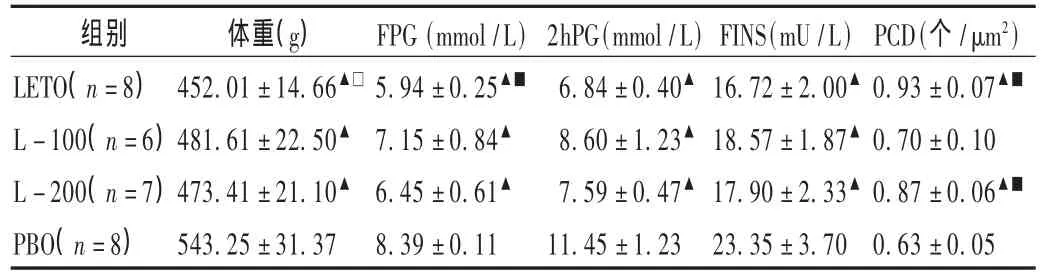
表1 4组大鼠体重、血糖、胰岛素抵抗指数及胰岛素阳性细胞密度(X±s)
2.3 大鼠胰腺组织相关基因表达情况
与 PBO组比较,LETO组、L-100组、L-200组 HCNP-pp相对表达水平下降,ChAT,M3R,GLP-1RmRNA相对表达水平均明显增高,差异具有统计学意义。见图2和表2。
2.4 大鼠胰腺组织HCNP-pp和GLP-1R蛋白表达情况
与 PBO组比较,L-100组、L-200组、LETO组 CTHCNP-pp和NT-HCNP-pp蛋白相对含量均明显减低,GLP-1R蛋白相对含量均明显增高,差异具有统计学意义。见图3和表3。
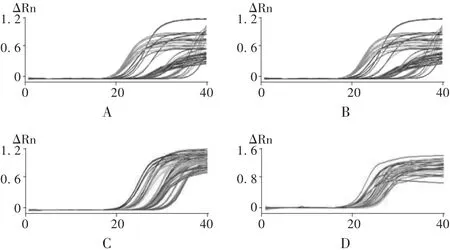
图2 大鼠胰腺 HCNP-pp,ChAT,M3R,GLP-1RmRNA表达
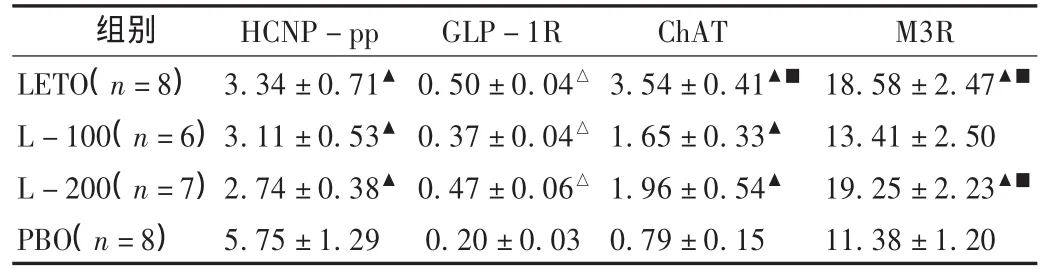
表 2 4组大鼠 HCNP-pp,ChAT,M3R,GLP-1RmRNA相对含量(×105拷贝,X±s)

图3 大鼠胰腺HCNPpp和GLP-1R蛋白含量表达
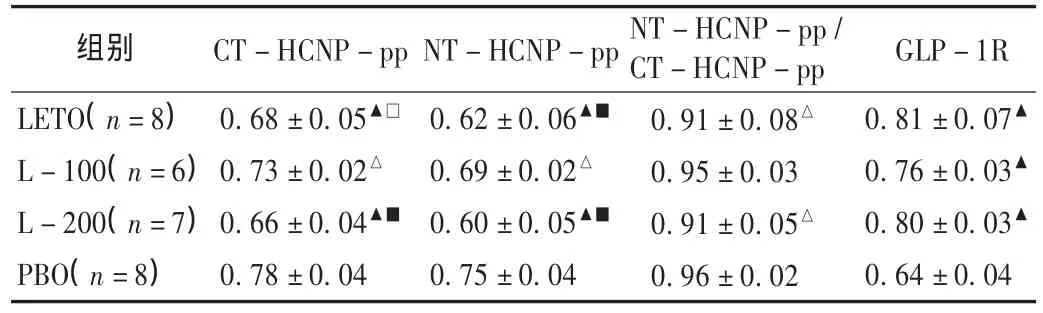
表3 4组大鼠HCNP-pp,GLP-1R蛋白水平相对含量(X±s)
3 讨论
利拉鲁肽作为人GLP-1类似物,因增加了脂肪酸侧链,可阻止二肽基肽酶Ⅳ(DPP-Ⅳ)的降解,延长对胰岛β细胞的作用。利拉鲁肽不但显著提高β细胞功能,还可增加β细胞体积及数量[8-9]。本研究结果显示,对糖尿病前期OLETF大鼠腹腔注射不同剂量的利拉鲁肽,具有改善胰岛增殖及分泌功能的作用,从而延缓糖尿病的发生。HCNP-pp可与Raf-1蛋白激酶结合,干扰Raf-1对MAPKK的磷酸化和激活,进一步抑制MAPK途径,阻止细胞增殖[10]。Zhang等[11]通过荧光双染、免疫组化染色等技术显示,HCNP-pp特异存在于胰岛细胞,可抑制MAPK信号途径,抑制胰岛β细胞增殖。因HCNP分子量较小,蛋白印迹技术不能表达其含量,故将其增强发光,以硝酸纤维素膜洗脱羧基端HCNP-pp蛋白抗体后,重新加用氨基端HCNP-pp蛋白特异抗体,应用氨基端与羧基端HCNP-pp蛋白相对含量的比值间接表示其含量。
本研究结果显示,IGT-OLETF大鼠GLP-1R,CT-HCNP-pp,NT-HCNP-pp蛋白表达水平增高、氨基及羧基末端HCNP-pp比值增高,GLP-1R,ChAT,M3R基因表达水平明显下降,HCNP-pp基因表达水平上升,表明糖尿病前期OLETF大鼠肠促胰岛激素作用下降、胰岛细胞HCNP-pp增多,出现血糖升高、胰岛β细胞增殖能力下降,胆碱能神经受体系统受损,进而导致血糖升高、胰岛素抵抗、胰岛细胞PCD显著下降;经过12周利拉鲁肽干预,OLETF大鼠不仅进食量、体重、血糖显著降低,HCNP-pp蛋白、基因表达水平以及NT-HCNP-pp/CT-HCNP-pp比值均相应下降,GLP-1R蛋白表达水平及GLP-1R基因表达水平升高,ChAT和M3R基因表达水平升高。因此推测,利拉鲁肽不但可减少HCNP-pp产生、活化MAPK信号转导途径、促进β细胞增殖,而且可促进HCNP-pp裂解,使HCNP增多,进一步作用于胆碱能神经系统,促进胰岛素释放。
本研究还显示,不同剂量利拉鲁肽干预的OLETF大鼠在胰岛形态学方面有所差异,L-100组大鼠胰岛细胞形态及胰岛素阳性细胞数同安慰剂组比较均无明显改善,结合L-100组大鼠M3R基因表达水平无明显升高,推测利拉鲁肽(100μg/kg)对处于糖尿病前期的OLETF大鼠胰岛β细胞增殖无改善,可能仅通过对GLP-1受体的作用提高胰岛素分泌,改善糖尿病前期状态。
[1]Ryden L,Standl E,Bartnik M,et al.Guidenlines on diabetes,pre - diabetes,and cardiovascular diseases:executive summary.The Task Force on Diabetes and Cardiovascular Diseases of the European Society of Cardiology(ESC)and of the European Association for the Study of Diabetes(EASD)[J].Eur Heart J,2007,28:88 - 136.
[2]李华婷,包玉倩,贾伟平.糖调节受损不同亚型胰岛素敏感性和胰岛素分泌的特点[J].中华内分泌代谢杂志,2008,24:229-231.
[3]Barr EL,Zimmet PZ,Welborn TA,et al.Risk of cardiovascular and all-caucse mortality in individuals with diabetes mellitus,impaired fasting glucose,and impaired glucose tolerance:the Australian Diabetes,Obesity,and Lifestyle Study(AusDiab)[J] .Circulation,2007,116:151-157.
[4]Matz K,Keresztes K,Tatschl C,et al.Disorders of glucose metabolism in acute stroke patients:an underrecongnise problem[J].Diabetes Care,2006,29:792 -797.
[5]Ojika K,Mitake S,Tohdoh N,et al.Hippocampal cholinergic neurostimulating peptides(HCNP)[J].Prog Neurobiol,2000,60(1):37 -83.
[6]Joao C,Yasser HA,Brian D,et al.Cooperative enhancement of insulinotropic action of GLP-1 by acetylcholine uncovers paradoxical inhibitory effect of beta cell muscarinic receptor activation on adenylate cyclase activity[J].Biochemical Pharmacology,2003,65:283-292.
[7]Sumara G,Formentini I,Collins S,et al.Regulation of PKD by the MAPK p38 in Insulin Secretion and Glucose Homeostasis[J].Cell,2009,136:235 -248.
[8]Sturis J,Cotfredsen CF,Romer J,et al.GLP - 1 derivative liraglutide in rats withβ-cell deficiencies:influence of metabolic state onβcell mass dynamics[J].Br J Pharmacol,2003,140:123 - 132.
[9]Matthews D,Marre M,Le-Thi TD,et al.Liraglutide,a once-daily human GLP-1 analog,significantly improves beta-cell function in subjects with type 2 diabetes.ADA 68th Scientific Sessions[J].Diabetes,2008,57(Suppl 1):505.
[10]Yeung K,Seitz T,Li S,et al.Suppression of Raf- 1 kinase activity and MAP kinase signalling by RKIP[J].Nature,1999,401(6 749):173-177.
[11]Lizhi Zhang,Zheng Fu,Charles Binkley.Raf kinase inhibitory protein inhibits- cell proliferation[J].Surgery,2003,136:708 -715.
