287份中成药说明书内容的调查分析
2012-06-27文随生徐玉红
文随生 ,徐玉红 ,李 东
药品说明书是指药品包装附有的,由国家食品药品监督管理局核准的,包含药品安全性、有效性的重要科学数据、结论和信息的技术资料,用以指导安全、合理使用药品。药品说明书的内容是否规范、完整,直接关系到患者的健康及生命安全。为规范中药、天然药物处方药说明书的书写和印制,国家食品药品监督管理局(SFDA)颁发了《药品说明书和标签管理规定》(以下简称《管理规定》)《关于中药、天然药物处方药说明书格式内容书写要求及撰写指导原则的通知》(以下简称《通知》)[1],发布了《中药、天然药物处方药说明书格式》(以下简称《说明书格式》)《中药、天然药物处方药说明书内容书写要求》(以下简称《内容书写要求》)以及《中药、天然药物处方药说明书撰写指导原则》(以下简称《指导原则》)。为了解中成药说明书内容的现状,笔者对287份中成药说明书内容进行了统计和分析,现报道如下。
1 资料与方法
收集医院目前使用的中成药说明书共287份。中成药的判别以药品批准文号为“国药准字Z+年号+顺序号”为准。同一制药企业的同一品种只入选1次,同一制药企业生产的不同品种各自入选,同一品名的药品不同剂型各自入选。对入选中成药说明书进行分类,根据《说明书格式》规定的项目进行标示情况统计和分析。数据分析主要采用频数分析等描述性统计方法。
2 结果与分析
2.1 调查结果
剂型分类:按照287份说明书相对应的中成药分为9种剂型,其中胶囊剂86份,丸剂47份,片剂44份,颗粒剂34份,合剂23份,注射剂20份,栓剂6份,外用剂型23份和其他剂型4份。
说明书项目标示情况:统计结果见表1。
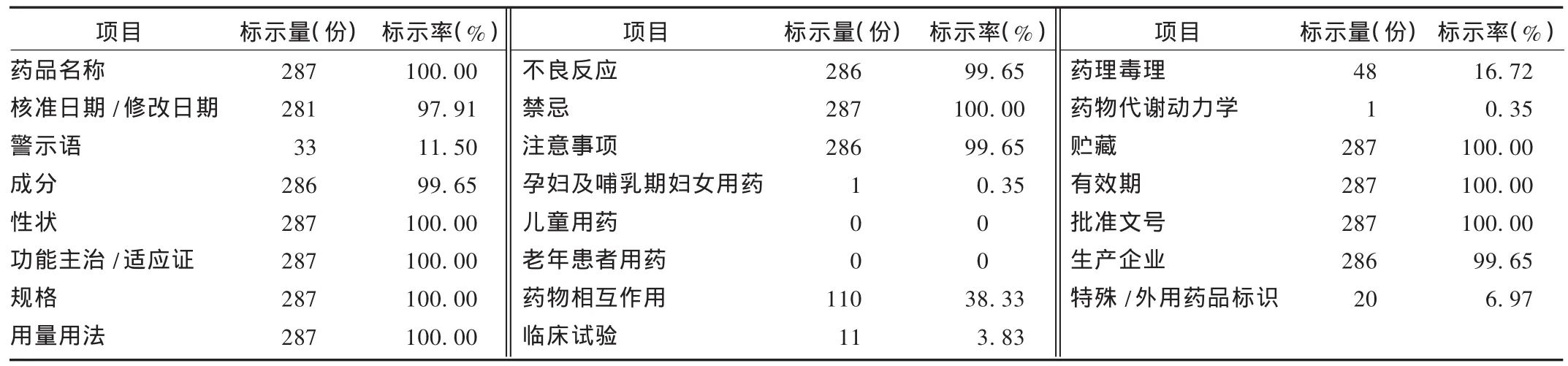
表1 287份中成药说明书项目标示情况
安全性项目内容标示情况:药物安全性内容包括不良反应、禁忌、注意事项和药物相互作用,其对患者安全用药有直接影响,其规范性尤其重要。其中“尚不明确”“如与其他药物同时使用可能会发生药物相互作用,详情请咨询医师或药师”“尚无本品与其他药物相互作用的信息”等描述内容,可归类为无实质性内容,其余有具体相关性描述内容的归类为有实质性内容,提示停药措施或用药治疗内容的归类为提示急救措施。统计结果见表2,大部分药物安全性内容描述都为无实质性内容。

表2 中成药说明书安全性项目内容调查[份(%)]
2.2 存在的问题
外用药品标识低:在23种中成药外用药中,有外用药品标识的16种,占69.57%。《内容书写要求》规定,需标注外用药品标识,起警示作用,以免发生误食等意外。
警示语标示率低:在287份中成药说明书中,只有33份有警示语项,且其中3份警示语项无内容。警示语是指对药品严重不良反应及其潜在的安全性问题的警告,还可以包括药品禁忌、注意事项及剂量过量等需提示用药人群特别注意的事项。有该方面内容的,应当在说明书标题下以醒目的黑体字注明;无该方面内容的,可不列此项。
功能主治项表述不规范:中成药的功能是指药品的治疗作用,是在中医理论的指导下,根据疾病的性质和特点等,遵循一定的治疗原则,确定相应的治法后选药组方,则该方药具有与治法相应的治疗作用;主治是指该药所适用的病机及证候表现。功能主治是以中医理论为依据而制订的,使用的语言是在系统方法指导下发展而成的中医学术语,是从整体信息角度认识人体生理病理状态及药物对人体信息调控作用的概念[2]。在287份中成药说明书中,49份功能主治项表述不规范,主要表现为用词生僻、措辞不易理解、中西医概念混乱、使用现代医药理论描述等。功能主治的表述不当,极易导致药不对证,结果是轻者无效,重者出现不良反应;同时说明书过于笼统,不利于药物的正确使用。因此,在中成药说明书的功能主治项中,用词需严谨,让患者明白易懂。
用法用量项标准不详细:用法用量是药品说明书的重要部分之一,是指导患者用药的依据。《指导原则》明确指出:详细列出该药品的临床应用方法,包括给药途径、方式、时间,使用前需加入溶剂稀释才能应用的静脉注射或滴注用的注射剂,应含稀释、配制溶剂、方法、浓度、溶剂用量以及使用中注射、滴注的速度等内容的说明。用量须说明临床推荐使用的剂量或常用剂量范围、给药间隔及疗程,提供特殊患者群用药所需剂量,应准确列出用药的剂量、计量方法、用药次数,并应特别注意用药剂量与制剂规格的关系。在287份中成药说明书中,用法用量项标示齐全,但内容不够详细。如小儿用量应根据年龄大小适量用药,不宜用“小儿酌减或遵医嘱”等语言表示。用法用量项中应使用通俗易懂、意思明确的文字表示,为患者合理用药提供更详细、明确的信息。
不良反应项标示内容不完整:《指导原则》指出,不良反应项下应实事求是地详细列出应用该药品时发生的不良反应,包括毒副作用、过敏反应等,可按其累及器官系统损害、反应的严重程度、发生频率或症状的系统性列出。尚不清楚有无不良反应的,可在该项下以“尚不明确”来表达。在286份中成药说明书中,只有68份(23.69%)有不良反应项的具体内容,218份(75.96%)使用“尚不明确”或“轻微的胃肠道反应”“偶有皮疹现象”“过敏反应”“不良反应轻微”等过于简单、笼统的描述。近几年,中成药的不良反应报告越来越多,如果使用不当或不引起重视,也会导致严重后果。药品说明书标注明确的不良反应,能促使医师、药师注意该药品谨慎应用,减少患者不按规定用药行为,从而降低药品不良反应的发生率。
禁忌项无实质内容:禁忌项必须阐述药品不能应用的各种情况,根据中药临床应用、“十八反”“十九畏”、妊娠禁忌等相关资料和文献进行科学分析,明确规定哪些特殊人群(老、幼、孕妇及哺乳期妇女等)和哪些疾病患者(肝、肾功能不全、高血压、糖尿病等)应慎用或禁用。尚不清楚有无禁忌的,可在该项以“尚不明确”表述。287份中成药说明书中,详细列出禁忌项的仅有98份(34.15%),其余均使用“尚不明确”表述。这种描述易导致患者用药混乱,有潜在的危险,更不能指导合理用药。
注意事项不完善:本次调查结果显示,注意事项的标示率达99.65%,其中有详细内容的占73.08%,描述为“尚不明确”的占25.87%,提示急救措施的仅有13.99%。注射剂药品说明书中多有强调不可与其他注射剂配伍使用、性状发生改变时不宜使用等详细内容,但对于给药速度却未过多提及。口服药药品说明书中,饮食与药物的禁忌描述最详细,服用时需慎用的情况也有说明,但有些还是过于简单或不明了。提示急救措施的仅有40份,也只是简单提示做停药处理,并无详细的急救治疗方案,使患者在用药期间发生不良反应时,无法据此选择正确有效的急救措施。
药物相互作用项缺乏研究资料:药物相互作用项应该列出与该药品产生相互作用的药品,并说明相互作用的结果及合并用药的情况。注射剂应明确有无药品相互作用的研究结果,如果没有研究资料,应注明“尚无本品与其他药物相互作用的信息”。本次调查中,该项标示率仅达38.33%,且该项内容下大多描述为“如与其他药物同时使用可能会发生药物相互作用,详情请咨询医师或药师”。这样极易让患者因联合用药而发生其他突发的不良反应。
特殊人群用药项缺乏研究资料:特殊人群包括老年人、儿童、孕妇及哺乳期妇女。根据《指导原则》规定,孕妇及哺乳期妇女用药、儿童用药、老年患者用药项均要求列入中药说明书。特殊人群由于生理、心理不同于成年人,药物在吸收、分布、代谢、排泄的过程与成人有差异,进而会影响到用药的安全性和有效性。本次调查中,药品说明书基本上没有特殊人群用药项,可见生产厂家对特殊人群使用中成药的研究还十分薄弱。
3 结语
药品说明书具有指导安全、合理使用药品的作用。通过对不同剂型中成药说明书的调查分析发现,我国中药说明书在书写和印制上明显存在不足,尤其是用药安全性项目和特殊人群用药方面。制药企业在这方面也明显有缺陷,对某些应该标注的项目根本不标注,或擅自删除某些不良反应内容,对药品的各项安全性缺乏深入的研究,导致中成药说明书极不规范。因此,应引起重视,并予以改进,使中药制剂的应用更加安全。
[1]唐春燕,陈大建,曾立威,等.药品说明书在药品风险管理中的地位与作用[J].医药导报,2008,27(7):869 -870.
[2]陈冬裕.对现行中成药说明书的调查和思考[J].中国药房,2009,20(9):718-720.
