大段同种异体骨移植治疗股骨干骨肉瘤的临床体会
2012-04-24冯毅吕智马全平李立志
冯毅 ,吕智,马全平 ,李立志
(山西医科大学第二医院骨科,山西 太原 030001)
骨肉瘤好发生于青少年长骨的干骺端,目前将病变位于骨干的骨肉瘤称为骨干骨肉瘤,其发病率很低,仅占所有骨肉瘤的 0.52%[1],国内文献报道不足 30例,因为病例少,经验积累不足,临床上易导致误诊。在治疗上 ,骨干骨肉瘤通常侵袭范围较大,传统治疗首选截肢[2]。随着技术进步,现在多采取保肢治疗,多数情况下行瘤段股骨全切除并人工全股骨假体置换术 ,手术治疗较彻底,但是术后功能较差,且假体的使用寿命对于长期生存患者而言无疑是一大隐患。我们采用大段同种异体骨移植治疗股骨干骨肉瘤 1例,术后短期效果较好,获得一些体会,现报告如下。
1 资料与方法
1.1 一般资料 患者女性,36岁。因间歇性右大腿疼痛7个月,加重3个月入院。早期间歇性疼痛,没有明显规律性,多以活动后出现 ,休息后缓解,后期疼痛逐渐频繁且逐渐规律,晨起疼痛明显 ,常被痛醒,疼痛持续至午后自行缓解,可一直至夜间不发作。查体:一般情况好,心肺腹未见异常。左大腿轻度肿胀,局部皮肤不红,无浅表静脉怒张,皮温不高 ,未触及明显肿物及包块,但中段有压痛,髋、膝关节活动正常,腹股沟淋巴结未触及肿大。X线片示:右股骨中段局部骨皮质反应性增生,髓腔变窄,髓腔内密度不均 ,伴散在钙化 ,骨膜呈葱皮样增厚(见图1)。 MRI见右股骨中段16cm范围骨髓异常信号,T1呈中等偏短的混杂短信号,T2呈长信号,局部骨皮质明显增厚 ,周围软组织有侵蚀 (见图2~3)。血沉20mm/h,碱性磷酸酶 51U/L。
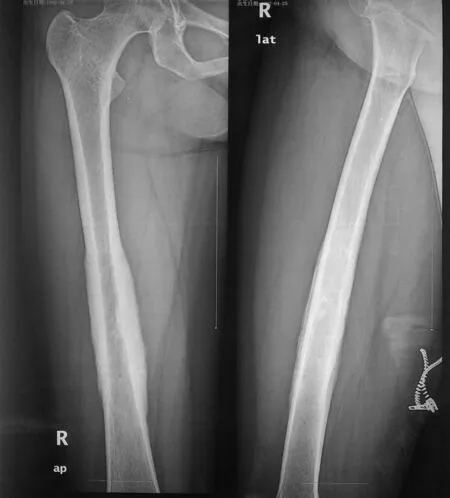
图1 术前X线片
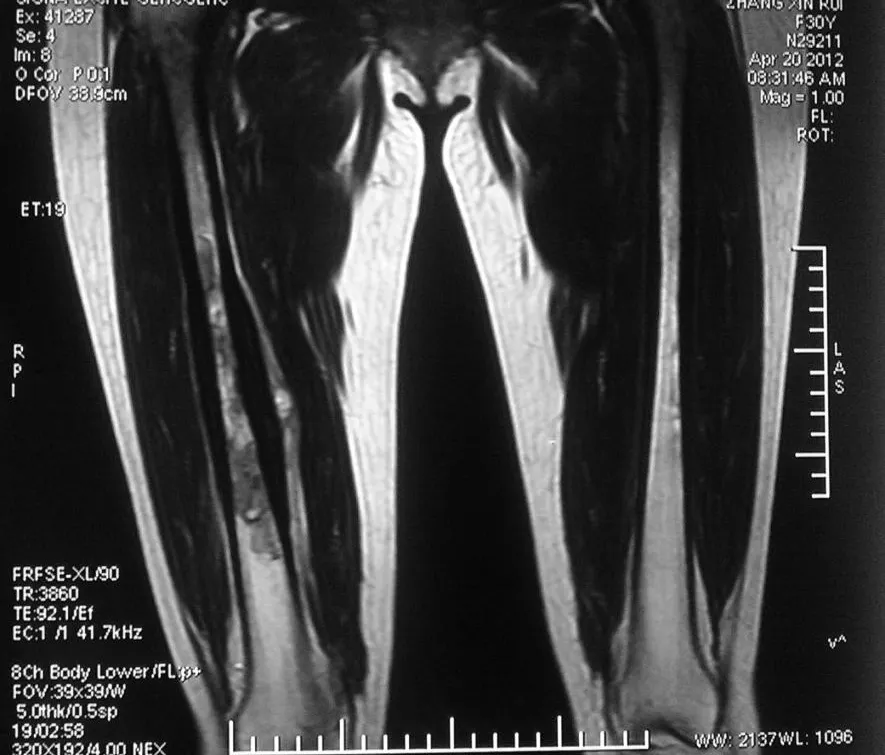
图2 术前患肢冠状位MRI示 T1呈中等偏短的混杂短信号
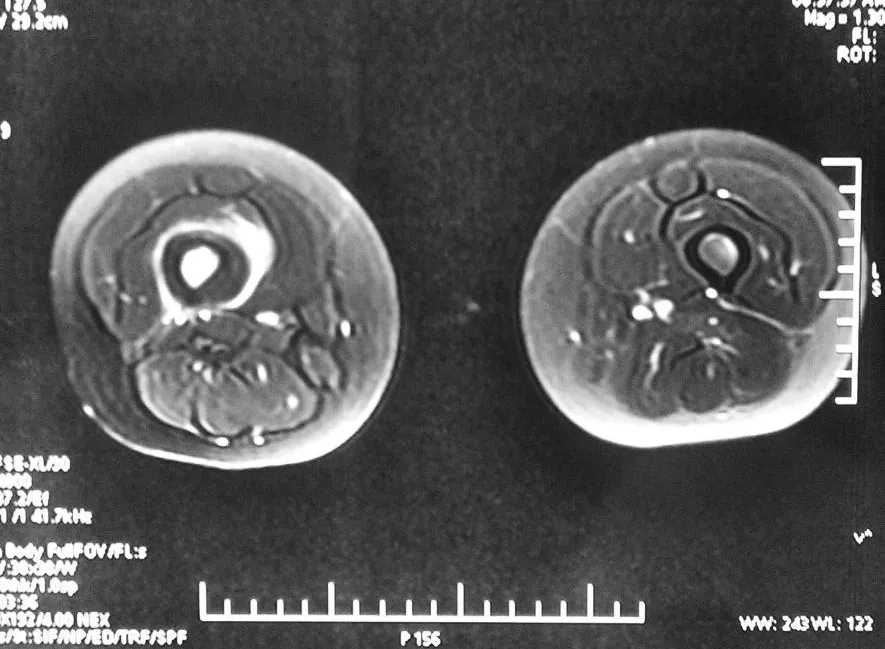
图3 横断面 MRI示 T2呈长信号
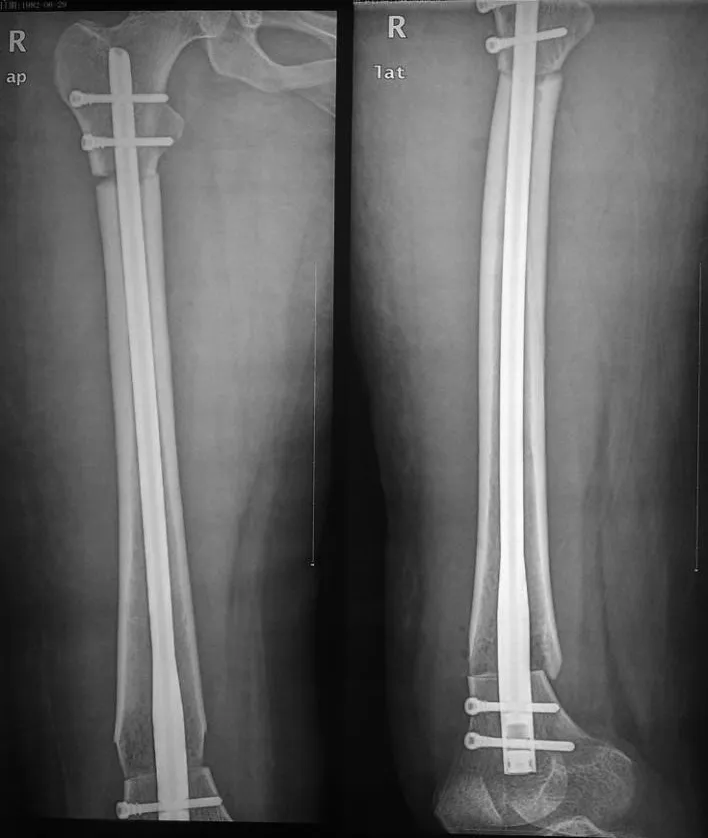
图4 术后正侧位X线片
1.2 方法 入院后诊断为慢性骨髓炎,预行病灶刮除置管冲洗术,后认为不能排除恶性骨肿瘤(尤其是 Ewing瘤),遂更改手术方案为先取活检,行术中冰冻;病理回报为骨肉瘤,遂结束手术,待切口愈合后患者接受化疗两个疗程,在此过程中,根据MRI确定截骨范围,定制 26cm长大段同种异体骨。化疗结束后,在全麻下行瘤段骨截除并行大段同种异体骨移植髓内针固定术(见图4),肿瘤及包裹的侵蚀软组织切除完整。手术时间 3h,输血 400mL。
2 结 果
术毕剖开见股骨干皮质不规则增厚,与骨膜增生融为一体,髓腔广泛肿瘤变,部分钙化灶。术后当晚发热,体温 39℃,但次日早即退热,考虑为输血反应。患者术后对植入物耐受良好,无不良主诉,术后 14 d拆线,切口一期愈合。病理报告为骨肉瘤。现患者患肢疼痛消失,髋、膝关节屈曲大于90°,根据 Enneking骨肿瘤术后功能评定标准评价为优。
3 讨 论
股骨干骨肉瘤因发病率低,发病部位特殊,临床症状较轻且发病年龄相对偏大,病变侵袭广泛,在工作中易导致误诊。本例患者曾在术前被多家医院诊断为“慢性骨髓炎”,后到我院门诊后再次被诊断为“慢性骨髓炎”收住院,住院后初次病例讨论会仍以“慢性骨髓炎”诊断制定出病灶刮除置管冲洗的手术方案,但在二次病例讨论中,考虑到 Ewing瘤的可能,把手术方案改为更加谨慎稳妥的“冰冻活检术+随机术”的手术方案,即术中冰冻如为慢性骨髓炎,则扩大切口行病灶刮出置管冲洗术,如为恶性肿瘤,则结束活检术,等待病理进一步确定后再制定下一步治疗计划。事实证明这样做是正确的,及时地避免了一次草率的医疗过错。在股骨干骨肉瘤的鉴别诊断中,有以下疾病需要特别注意区分:a)Ewing瘤:多发生于青少年,是这个年龄组继骨肉瘤后的第二好发恶性骨肿瘤,但超过 30岁的患者也常有,因其最好发于股骨干,并有骨膜葱皮样增生的特征性影像学表现,使得其与本例患者难以鉴别。我们术前一度疑诊本例为 Ewing瘤,没有考虑到骨肉瘤,可见其临床的相似性。 Ewing瘤无论在病理破坏、影像学表现上均与股骨骨干骨肉瘤较难鉴别,尤其是小细胞型骨肉瘤,往往需要借助病理学检查 ,但 Ewing瘤发病年龄略低,对放射治疗极其敏感,可进行诊断性治疗[3,4]b)不典型骨髓炎:缺乏明显感染病史,病史一般较长,多发生于下肢长骨骨干,并纵行扩展延伸,但其软组织肿胀不明显,周围骨质骨膜增生较轻微或无骨膜增生。c)骨纤维结构不良:在病理和X线表现上较难与骨干低级别中心型骨肉瘤鉴别[5],但骨纤维结构不良较少突破骨皮质并形成软组织肿块,骨髓腔受侵范围较局限且瘤周软组织水肿相对少见。
术中冰冻是一个良好的解决两难问题的方法,在不确定情况下,可以设计两个或多个手术方案,先行术中冰冻,根据结果再选择下一步方案,这样不仅可以做出正确选择,并能缩短治疗周期。在瘤段骨切除时,术中冰冻同样可以为我们提供可靠的判断截骨安全范围的方法,虽然本例术前根据MRI已经制定出截骨范围,但术中对截骨端分别送术中冰冻,确定为无瘤区后再行移植,使得治疗更安全。
在手术方法上,大段同种异体骨由于为订制品,总会和实际截骨后留下的移植区存在差异,首先为长度上差异,虽然术前根据MRI能够较精确测量出需要截骨的安全范围,但术中还要根据截骨端术中冰冻进一步确定,因此,植入物可能会出现较原计划变短的情况,这就要求术前在定制异体骨时要多余出 2~3 cm,利于术中修正;其次为粗细和形态上的差异,异体骨和截骨端难以完全吻合,需要进行必要的修整,一方面促进骨诱导,一方面减少对周围软组织的摩擦。如果为异体骨粗,则需要截除多余的边角等,修整异体骨断端基本与截骨端吻合,但要注意,一定要保证至少相对的两侧骨皮质不受破坏。如果为截骨端粗,则一般可以不做处理,免得使皮质的支撑性下降。
目前对于股骨干骨肉瘤的保肢治疗主要有瘤段骨灭活再植、全股骨人工假体置换和大段同种异体骨移植等方法。瘤段骨灭活再植对于病灶有较高的要求,病灶不能破坏骨皮质太多,否则会直接影响稳定性和骨愈合 ,此外,灭活效果难以鉴定,术后复发率高。全股骨置换是一个较彻底的解决办法,但缺点也是显而易见的,手术创伤大、出血多、术后功能差,假体其他常规的并发症如松动、下沉、感染、磨损等同样无法避免。大段同种异体骨移植相对于全股骨置换最大的优点就是保留了上下关节,最大限度地提高了术后功能,同时具有手术时间短、创伤小、出血等优点。大量的基础和临床研究表明,冷冻同种异体骨具有良好的骨组织结构、形态、强度、骨诱导能力和较低的免疫性以及与宿主骨有较强的愈合能力等优点,已成为修复大段骨缺损的良好材料。Muscolo等[6-8]对 80例采用同种异体骨移植修复股骨远端缺损患者进行了平均长达 125个月的随访,其中 76例患者患有恶性肿瘤,发现 5年和 10年植入同种异体骨存活率可达78%。对 52例患者行胫骨近端肿瘤切除同种异体骨移植重建术后随访发现,32人愈合良好,移植骨 5年和 10年存活率为 65%。Kharrazi等[9]对 16例因肿瘤致肘部骨缺损后行大段同种异体骨移植患者进行随访,平均 9.9年,结果 14例恢复良好,可重新正常工作,1例因感染而失败。他认为,同种异体骨移植治疗肢体大段骨损失对肘关节功能重建起到很大作用。牛晓辉等长期追踪 164例因骨肉瘤或骨巨细胞瘤切除后造成不同部位骨缺损行同种异体骨移植患者,结果:21例患者有局部复发;38例患者骨不连;晚期发生移植骨骨折并发症患者11例;18例患者发生感染;发生关节稳定行不良 ,半脱位者占13例;因局部复发或严重感染的10例患者行截肢术。他们认为同种异体骨与宿主骨的形状、强度、骨传导和骨诱导性相仿,可用于骨肿瘤切除后缺损的重建[10]。
同种异体骨的移植效果逐渐被认可,但大段同种异体骨移植目前仍存在诸多问题有待解决,如能否完全诱导成骨,能否达到骨性愈合等等;此外,术中固定、术后感染、继发疲劳骨折、肿瘤复发等等这些问题都无法回避。因此,虽然牛晓辉等承认其重建作用,但仍指出其并发症较高,要慎重对待,他进一步总结认为彻底切除肿瘤是减少同种异体骨移植并发症的有效方法[10]。我们本例 26 cm长度同种异体骨移植治疗少见的股骨干骨肉瘤算是一个尝试,但由于术后时间较短,其长期的效果有待进一步观察了解。
[1] Haworth JM,Watt I,Park WM,et al.Diaphyseal osteosarcoma[J].Br J Radiol,1981,54(647):932-938.
[2] 姚健,孙鼎远,王林森.原发性骨干骨肉瘤的影像学表现 [J].中华骨科杂志,2000,20(1):40-43.
[3] Dahlin DC Bone tumors.In: Dahlin DC,ed.Osteosarcoma[M].2n d ed.New York:Spring field,1986:270-276.
[4] Bertoni F,Bacchini P,Fabbri N,et al.Osteosarcoma.Low-grade intraosseous-type osteosarcoma,histologically resembling parosteal osteosarcoma,fibrous dysplasia,and desmoplastic fibroma[J].Cancer,1993,71(2):338-345.
[5] Andresen KJ,Sundaram M,Unni KK,et al.Imaging features of low-grade central osteosarcoma of the long bones and pelvis[J].Skeletal Radio,2004,33(7):373-379.
[6] Muscolo DL,Ayerza M A,Aponte-Tinao LA,et al.Ues of distal femoral osteoarticular allografts in limb salvage surgery[J].JBone Joint Surg(Am),2005,87(11)2449-2455.
[7] Muscolo DL,Ayerza M A,Farfalli G,Aponte-Tinao LA,et al.Proxi-mal tibia osteoarticular allografts in tumor limb salvage surgery[J].Clin Orthop Relat Res,2010,468(5):1396-1404.
[8] Muscolo DL,Ayerza M A,Aponte-Tinao LA,et al.Unicondyiar Os-teoarticular allografts of the knee.Surgical technique[J].JBone Jiont Surg(Am),2008,90(Suppl2):206-217.
[9] Kharrazi FD,Busfield BT,Khorshad DS,et al.Osteoarticular and total elbow allograft reconstruction with severe bone loss[J].Clin Orthop Relat Res,2008,466(1):205-209.
[10] Niu X H,Hao L,Zhang Q,et al.Massive allograft replacement in management of bone tumors[J].Zhonghua Wai Ke Za Zhi,2007,45(10):677-680.
