镰形棘豆总黄酮软膏剂的制剂工艺研究
2012-01-25陈志鹏瞿敏明刘丹肖衍宇蔡宝昌陈新梅
陈志鹏,瞿敏明,刘丹,肖衍宇,蔡宝昌*,陈新梅
(1.南京中医药大学,江苏省中药炮制重点实验室,江苏南京210029;2.中国药科大学,江苏南京210009;3.山东中医药大学,山东济南250355)
镰形棘豆Oxytropis falcata Bunge是豆科棘豆属的多年生无茎草本植物,藏药名为“俄达夏”,具有消炎镇痛、生肌愈疮、止血等功效,在临床上广泛应用于治疗痛风、湿痹、“冈巴”、疮疖肿痛、骨伤疼痛等,是藏医“三消炎药”之一,被称为“草药之王”[1],是奇正消痛贴膏、青鹏膏剂、藏奇神风湿贴、奇正藏贴、万痛筋骨帖、藏药奇正贴、风骨1号、藏红花油等数十种藏药复方或藏成药的主要药物。本课题组前期研究结果表明其总提物口服有一定的镇痛抗炎活性[2],有效部位筛选其总黄酮部位口服具有明显的抗炎镇痛活性[3],但其生物利用度较低[4]。本研究的目的是以镰形棘豆的主要成分2',4'-二羟基查尔酮(2',4'-dihydroxychalcone,TFC)为指标性成分[5](TFC在镰形棘豆中为主要活性成分,其抗菌[6]、抗氧化[7]、抗肿瘤[8]作用显著),以其体外累积透过量为指标,尝试将镰形棘豆总黄酮制备为软膏剂,在单因素考察的基础上优化总黄酮软膏剂处方,以期得到渗透性能良好的镰形棘豆总黄酮软膏剂,达到提高其生物利用度的目的,为进一步的研究奠定基础。
1 仪器与试药
1.1 仪器
Varian 920-LC高效液相色谱仪(美国Agilent公司);RYJ-6A型药物透皮扩散仪(上海黄海药检仪器厂);SHZ-88台式水浴恒温振荡器(江苏太仓市实验设备厂);CZX-9140MBE型高速离心机(上海博迅实业有限公司医疗设备厂);AG-285电子天平(瑞典METTLER公司)。
1.2 材料
TFC,由本实验室自制,经熔点测定、UV、1HNMR和13C-NMR等确定其结构,HPLC测定其纯度大于98.0%;色谱纯乙腈(德国CNW公司),其他试剂为分析纯。SD大鼠,180~220 g,雄性,由南京中医药大学动物实验中心提供。
1.3 总黄酮的制备方法与定量测定
称取100.0 g药材粉末,加入1 L无水乙醇于室温下超声提取3次,每次60 min,药渣再用50%乙醇超声提取3次,每次60 min,减压滤过,收集所有滤液并于50℃下减压浓缩成浸膏,加入2%氢氧化钠水溶液,超声促溶解,减压滤取碱水液,重复溶解多次至滤液近无色,合并所有碱水液,用1%盐酸溶液调节至pH5,依次用三氯甲烷和乙酸乙酯萃取各6次,合并萃取液,50℃下减压浓缩至小体积后,转入洁净并已称定质量的蒸发皿中,于80℃水浴中加热挥干溶剂,再次称定质量,总黄酮得率2.4%。
总黄酮测定以芦丁为标准品,采用紫外吸光度标准曲线法,计算样品中黄酮的质量分数为83.7%;采用HPLC标准曲线法测定总黄酮有效组分中TFC的质量分数为6.07%。
2 方法与结果
2.1 体外透皮皮肤的处理
取体质量(200±20)g健康大鼠,采用机械脱毛法,剥离腹部皮肤,去除皮下脂肪层及黏液组织,用无菌生理盐水洗净后,冷藏备用。
2.2 体外透皮实验方法的建立
2.2.1 将镰形棘豆总黄酮溶液或乳膏剂均匀涂抹于预处理动物的皮肤。将皮肤固定于改进的Franz扩散池的供药池,角质层面朝向供药池。在接受室中注入接受液,液面恰与皮肤内层接触,开动电磁搅拌器恒速搅拌和恒温水浴(37±0.5)℃,在设定时间点取样1 mL,置于离心管中。每次取样后均补加相同体积的新鲜接受液并排除接收室中的气泡,样品溶液用HPLC法测定吸收值,计算TFC的质量浓度,并按下式计算累积透过量:

其中,Cn校:n点的校正药物质量浓度;Cn测:n点实际测得的的药物质量浓度;∑n-1Ci:该取样点前各点的测定质量浓度之和;V0:接受池中接受液的体积;V:取样量;Qn:n点时药物单位体积的累积释药量;A:扩散池横截面积;C载药:载药质量浓度;Cd:供给池中供试液药物质量浓度。
计算累积渗透量Qn,并计算累积渗透率Qn%,比较不同透皮实验的累积透过量Q%,确定合适的实验方法与制剂配比。
2.2.2 HPLC法测定TFC的色谱条件[3]汉邦ODS-2色谱柱(4.6 mm×250 mm,4.5 μm);检测波长365 nm;柱温28℃;流动相为乙腈-0.1%甲酸水溶液(60∶40);体积流量1.0 mL/min;检测波长365 nm;进样量10 μL。
2.3 体外透皮方法学考察
2.3.1 标准曲线的绘制精密称取5.35 mg TFC标准品置于5 mL棕色量瓶中,加甲醇溶解并稀释至刻度,摇匀,精密移取1 mL于5 mL棕色量瓶中,用甲醇稀释至刻度,摇匀,得21.4 μg/mL的TFC贮备液。精密吸取贮备液0.1,0.125,0.25,0.5,1,2 mL,置于10 mL量瓶中,加甲醇稀释至刻度,摇匀,得到稀释成0.214,0.268,0.535,1.07,2.14,4.28,21.4 μg/mL的标准品溶液。按照2.2.2项下方法进样测定。以峰面积(Y)为纵坐标,进样量(X,ng)为横坐标进行线性回归,计算得到线性回归方程:Y=0.061 2X-3.621 5,r=0.999 9,线性范围:214~21 400 ng/mL。
2.3.2 体外透皮接收液的筛选由于镰形棘豆总黄酮溶解性较差,为满足漏槽条件,我们对常见接受液进行饱和溶解度的测定。结果见表1。故选用PES[PEG400-乙醇-生理盐水(20∶30∶50)]作为体外透皮实验的接收液。将累积渗透量Q对时间t进行线性回归得到Q=2.160 5t+4.839 7,得透皮速率常数Js=2.160 5 μg/(cm2·h)。

表1 镰形棘豆总黄酮中TFC在不同介质中的溶解度(μg/mL)(n=3)Tab.1 The solubility of TFC in different solvent(μg/mL)(n=3)
2.4 软膏剂处方单因素考察
2.4.1 软膏剂的制备称取处方量的硬脂酸、单硬脂酸甘油酯、蓖麻油和羊毛脂为油相,置于蒸发皿中,于水浴上加热至80℃左右混合熔化。另将三乙醇胺和蒸馏水置烧杯中,于水浴上亦加热至80℃左右。在等温下将水相缓缓倒入油相中,并于水浴上不断搅拌至呈乳白色半固体状,在室温下搅拌至近冷凝。
溶液剂的制备:镰形棘豆总黄酮有效组分溶于40%乙醇作为溶液剂试药,药物质量浓度为1.028 mg/mL,将1 mL试药溶液缓慢加入供给室皮肤表面。
2.4.2 载药量对软膏剂体外累积透皮率的影响制备含有不同药物质量分数(选取0.5%、1%和5%,w/w)的镰形棘豆总黄酮软膏剂,并进行体外累积透皮率实验,计算软膏剂的累积透皮率。结果如图1所示。
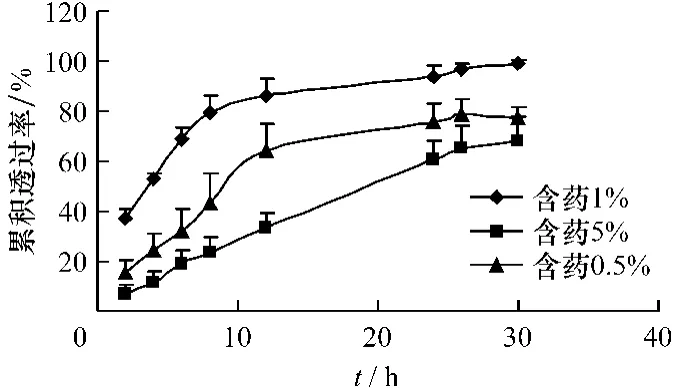
图1 含不同质量分数药物溶液体外透皮累积透过率(n=3)Fig.1 Penetration cumulative percentage of different concentrations of drugs in vitro transdermal permeability(n=3)
2.4.3 促渗剂的种类对镰形棘豆软膏剂累积透过量的影响分别制备含有促渗剂氮酮、龙脑、油酸1%的软膏剂,并进行累积透皮率实验,计算3种促渗剂对软膏剂中TFC的累积透过率的影响。结果见图2。
2.4.4 乳化剂配比对体外累积透皮率的影响制备单硬脂酸甘油酯与三乙醇胺的配比分别为15∶1、30∶1、45∶1的软膏剂,并进行累积透皮率实验,考察乳化剂配比对软膏剂中TFC的累积透过率的影响,结果见图3。

图2 不同促渗剂对软膏剂中TFC的体外透皮累积透过率的影响(n=3)Fig.2 Effect of different penetration enhancers on transdermal ointment in the TFC transmission of the cumulative(n=3)

图3 不同乳化剂配比对体外累积透皮率的影响(n=3)Fig.3 Effect of different emolsifier matching on transdermal ointment in the TFC transmission of the cumulative(n=3)
2.4.5 利用正交设计优化软膏剂处方以促渗剂油酸用量、载药浓度、单硬脂酸甘油酯和三乙醇胺配比三个因素为考察指标,每个因素设置三个水平,以体外透皮累积透过率为考察指标,选用L9(34)进行正交试验,见表2。软膏剂处方筛选结果见表3、4,最优促渗效果的处方为油酸(1%)、载药浓度(0.5%)、单硬脂酸甘油酯-三乙醇胺(30∶1)。
2.5 总黄酮软膏剂的体外透皮实验镰形棘豆总黄酮溶于40%乙醇作为溶液剂试药,将1 mL试药溶液缓慢加入供给室皮肤表面;软膏剂按照2.4.1项优化处方制得,将100 mg试药均匀涂抹在供给室皮肤表面,分别在0.5、1、2、4、6、8、10、18、24、26、30h取样,按照2.2.2项方法测定TFC并计算溶液剂与软膏剂的累积透皮率,结果见图4。

表2 因素水平Tab.2 Experiment scheme of the orthogonal design

表3 正交实验结果Tab.3 Experiment scheme of the orthogonal design

表4 方差分析Tab.4 The analysis of variance

图4 溶液剂与软膏剂体外透皮累积透皮率比较(n=3)Fig.4 Penetration cumulative percentage of solutions and ointments(n=3)
3 讨论
3.1 实验中油酸促渗的效果在1%时最佳,可能与油酸促渗的机理有关[9],一般认为油酸与皮肤中的脂肪酸有相似的结构,使角质层细胞间类脂分子排列发生变化,增加类脂的流动性,在油酸增加到一定浓度后,其改变类脂分子的变化的能力降低,抑制了药物透皮的效果。在体外透皮实验中,由于累积透过效果明显,故没有在实验中选择复合促渗剂进行筛选。
3.2 有文献报道,体外透皮实验中,以有效部位中主要成分作为透皮性能筛选指标能一定程度上反映该有效部位的透皮性能[10]。本课题前期研究总黄酮有效组分的不同剂量镇痛抗炎药理活性实验中,结合不同剂量药动学实验发现,TFC在体内的血药浓度与其镇痛抗炎药理活性具有剂量相关性,因此体外透皮以TFC作为考察试药总黄酮的透皮性能具有可行性。
3.3 实验中不同浓度药物体外透皮实验的结果表明含药1%的试药释放最完全,实验中采用累积透过率作为考察指标,出现了药物累积透过率不以浓度为依赖的结果,而药物累积透过量依然为5%试药浓度最高,这一结果与药物浓度为体外透皮主要影响因素并不矛盾。有文献报道[11]高浓度的药物可能对自身透皮有阻碍作用,也有可能药物的渗透系数与浓度的变化呈非线性关系[12]。
3.4 载药量考察中主要参考溶液剂在经皮给药药理实验中的体积分数[13],选取0.5%~5%的范围考察其体外透皮特性。
4 结论
在单因素考察的基础上,通过正交设计优化软膏剂的处方。与溶液剂相比,镰形棘豆总黄酮软膏剂的体外透皮累积透皮率明显增加,提示将中药有效部位包裹于软膏剂中可提高药物渗透能力,有利于炎症和疼痛等局部疾病的治疗。
但是,本研究中对于制剂的考察指标较少,在今后的研究中将进一步研究制剂的稳定性、刺激性等,此外,虽然软膏剂在体外具有良好的渗透能力,但是其在体内的性质有必要进一步的研究。
[1]姜华,胡君茹,刘霞,等.藏药镰形棘豆的研究进展[J].中草药,2006,37(2):314.
[2]王栋,杨欢,童丽,等.藏药镰形棘豆的镇痛抗炎活性[J].药学与临床研究,2008,16(2):90-93.
[3]杨欢.藏药镰形棘豆的抗炎活性及化学成分研究[D].南京:南京中医药大学,2008.
[4]Chen Z P,Qu M M,Cai B C,et al.The studies of anti-inflammatory and analgesic activities and pharmacokinetics of Oxytropis falcate Bunge extraction after transdermal administration in rats.[J].Fitoterapia,2011,82(3):426-433.
[5]楼成华,杨欢,蔡皓,等.反相高效液相色谱法测定藏药镰形棘豆中2',4'-二羟基查耳酮的含量[J].中国药学杂志,2009,44(6):477-478.
[6]Jiang H,Hu J R,Liu X.Screening for fractions of Oxytropis falcata Bunge with anti bacterial activity[J].Nat Prod Res,2009,23(10):953-959.
[7]Jiang H,Hu J R,Liu X.Antioxidant activities of extracts and flavonoid compounds from Oxytropis falcate Bunge[J].Nat Prod Res,2008,22(18):1650-1656.
[8]Lou C H,Wang M Y,Cai B C,et al.Preliminary studies on anti-tumor activity of 2',4'-dihydroxychalcone isolated from Herba Oxytropis in human gastric cancer MGC-803 cells[J].Toxicol In Vitro,2009,23(5):906-910.
[9]褚爱武,崔跃红,刘文波,等.油酸经皮促透作用微观机理的研究[J].电子显微镜学报,2002,21(2):184.
[10]Gu S Y,Gao J,Hou X M,et al.Effects of penetration enhancers on Shuangwu traumatic formula:In vitro percutaneous absorption and in vivo pharmacodynamic evaluation of an herb medicine[J].Eu J Pharm Biopharm,2009,73(3):385.
[11]翁伟宇,徐惠南.川芎嗪体外透皮的特性[J].上海医科大学学报,1999,26(5):336.
[12]白志华,方晓玲.三七总皂苷中人参皂苷Rg1体外透皮吸收的实验研究[J].中成药,2006,28(5):639-641.
[13]瞿敏明,陈志鹏,蔡宝昌.镰形棘豆经皮给药后抗炎镇痛活性有效部位的筛选[J].安徽医药,2011,15(1):14-16.
