用毛细管流变仪考察溴化丁基橡胶的热稳定性能
2012-01-16许良瑞李树新郭文莉
许良瑞, 李树新, 郭文莉
(1.北京化工大学材料科学与工程学院,北京100029;2.北京石油化工学院材料科学与工程系,北京102617)
溴化丁基橡胶(BIIR)是丁基橡胶(IIR)的一种改性品种[1-2]。通常是在一定温度下,丁基橡胶与溴元素发生离子取代反应得到的。目前对于溴化丁基橡胶合成工艺条件研究较多,专门研究后处理干燥环境的影响的报道却很少,由于胶厂在溴化丁基装置中的后处理线上是用双螺杆膨胀干燥机干燥,在实际操作中,螺杆出口温度的波动范围很大(通常是150~180℃)在这个阶段聚合物结构性能很容易发生变化。考虑到溴化丁基橡胶的实际干燥环境(螺杆挤出干燥机)与毛细管料筒挤出的环境非常相似,二者都能使胶料在一定温度下同时受热空气和剪切力的影响,因此本文采用毛细管流变仪对干燥环节进行模拟实验,探索了温度和受热时间对胶料的影响。
毛细管流变仪的结构一般为柱塞式。物料在电加热的料桶里被加热熔融,料桶的下部安装有一定规格的毛细管口模。该仪器可在较宽范围调节聚合物在料筒中的停留(预热)时间以及料筒的温度,温度稳定后,料桶上部的料杆在驱动马达的带动下以一定的速度或以一定规律变化的速度把物料从毛细管口模中挤出来。
本文采用毛细管流变仪进行实验,结合实际,考察了150℃和180℃下,改变溴化丁基橡胶在毛细管流变仪料筒中的停留时间,核磁氢谱表征挤出胶料,并根据核磁图计算溴化丁基橡胶溴含量以及其各微观结构的变化。
1 实验部分
1.1 主要材料
燕山-1751丁基橡胶(不饱和度1.8%(摩尔分数));液溴(分析纯),氢氧化钠(化学纯),硬脂酸钙(工业级),均为北京化工厂生产;己烷溶剂(工业级,北京燕山石油化工厂);环氧大豆油(ESBO)(工业级,杭州硕州油脂化工厂),抗氧剂1330(化学纯,东京化成工业株式会社)。
1.2 实验仪器
反应釜(2L),北京先达力公司;
1H-NMR分析仪,DRX AVANCE 400MHz型,瑞士Bruker公司;
MCR301毛细管流变仪,奥地利安东帕有限公司。
1.3 试样制备
取干燥的丁基橡胶40g,剪成小块放入反应釜中,倒入350mL己烷溶剂。室温下搅拌溶解,约10 h后形成均匀的胶液,胶液质量分数约15%。用水浴加热至50℃左右,于黑暗条件下迅速加入0.66 mL液溴,剧烈搅拌,反应约2min后加入质量分数为5%的氢氧化钠溶液30mL进行中和,10min后停止搅拌。然后往胶液中注入300mL去离子水并进行搅拌,目的是去除胶液中残留的杂质和离子,静置分层后,将下层的水抽出,如此往复水洗3次。随后加入环氧大豆油、抗氧剂1330以及硬脂酸钙,充分搅拌使其分散。最后加入沸水闪蒸除去溶剂,取出橡胶,将橡胶真空干燥后,在100℃的开练机上开练2min,去除水分[3]。将上述溴化丁基橡胶剪成粒状,便于放入毛细管流变仪的料筒。
1.4 试样表征
采用瑞士Bruker公司生产的DRX AVANCE型波普仪测定,氢谱工作频率为400.13MHz,样品在室温下用氘代氯仿溶解配制成质量分数2%溶液,以TMS为内标,室温下测试。
一个绿裙少女从玉米地里走过来,对树上的少女喊:“乔瞧,我们该回家了。”见秀容月明满脸是水,掏出手帕,一言不发地递给他。
由核磁谱图分析可以看出溴化丁基橡胶的几种主要微观结构,各吸收峰及其对应的化学位移归属如表1所示。表1给出了溴化丁基橡胶核磁谱图中各吸收峰的化学位移及归属,溴化丁基橡胶的3种主要微观结构如图1所示。
其中Ⅰ结构表示未溴化的丁基橡胶,Ⅱ结构为溴代仲位烯丙基,Ⅲ结构为溴代伯位烯丙基[4-5]。生产过程中聚合物性能最容易发生改变的阶段在于后处理过程中,因为后处理通常要经过高温、强剪切、高压力等过程,这与毛细管流变仪挤出物料的过程十分相似。但是毛细管流变仪料筒中活塞不具有螺杆挤出机螺杆的可供排水的螺纹结构,故在本文的研究中,只用其考察挤出过程中温度和停留时间对溴化丁基橡胶溴含量和微观结构的影响。

表1 BIIR核磁谱图中吸收峰的化学位移归属Table 1 Assignment of signals in the 1 H-NMR sprctrum of BIIR

Fig.1 Microstructure of bromobutyl rubber图1 溴化丁基橡胶的3种主要微观结构
2 结果与讨论
2.1 BIIR溴含量的计算
核磁图中各个吸收峰的面积与其对应的结构含量成正比,故可以根据各结构的吸收峰面积(峰归属见表1)计算出BIIR的含溴质量分数,计算公式如式(1)所示:
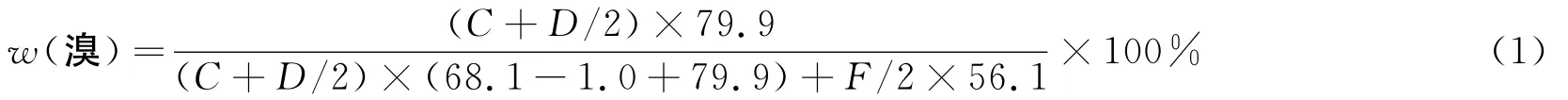
Cottle D L[6]等对溴化丁基橡胶的溴含量进行理论计算,得出的一个溴含量理论最大值,该值可用式(2)计算:

其中,L—丁基橡胶的不饱和度,%;
M1—异丁烯的相对分子质量;
M2—异戊二烯的相对分子质量;
79.9 —溴原子的相对分子质量。
2.2 不同停留时间对BIIR溴含量的影响
溴含量直接关系到双键的反应活性以及交联密度,为满足工业需求,通常BIIR中的含溴质量分数在1.8%~2.1%。
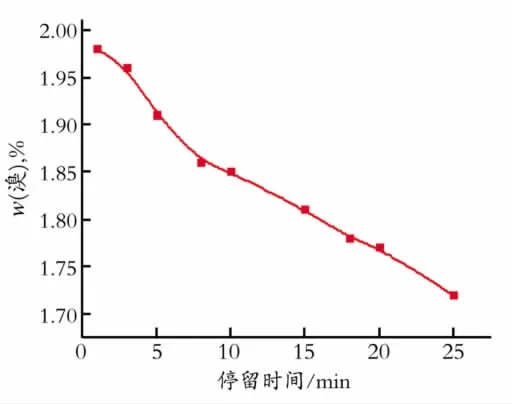
Fig.2 The effect of residence time to brominate content of BIIR at 150℃图2 150℃下不同停留时间对BIIR溴含量的影响
由图2可以看出,在150℃下,料筒中BIIR的溴含量随着停留时间的延长在不断的减少,至18 min时含溴质量分数为1.77%,已经达不到工业要求的溴含量。这是因为液溴与丁基橡胶发生取代反应生成烯丙基溴,溴化丁基橡胶在受热过程中,发生了脱HBr反应,导致结合溴含量减少。
设定毛细管流变仪预热温度180℃,不同停留时间下对挤出胶料做核磁表征,根据式(1)计算溴含量,结果如图3所示。
图3表现出来的趋势与图2一致,即随着受热时间的增加,溴含量会逐渐减少,180℃下受热8 min时,含溴质量分数降至1.77%,已经达不到工业要求,对比图2和图3,可以看出在180℃下溴含量的减少速率明显比150℃时快,说明高温会加速脱溴化氢反应。
2.3 不同停留时间对BIIR微观结构的影响
由图1可知,制备的溴化丁基橡胶主要有3种结构,其中Ⅰ结构表示未溴化的丁基橡胶,Ⅱ结构为溴代仲位烯丙基结构CHBr,其化学位移为4.34,即表1中的C峰;Ⅲ结构为溴代伯位烯丙基结构CH2Br,其化学位移4.08与4.04,即表1中的D峰。伯位溴元素比仲位溴元素更加稳定,不易被取代,而且溴代伯位烯丙基结构含量越多,硫化速度更快,与不饱和橡胶的硫化粘合力更佳,因而溴代伯位烯丙基结构的相对含量是评价溴化丁基橡胶性能的重要参数。

Fig.3 The effect of residence time to brominate content of BIIR at 180℃图3 180℃下不同停留时间对BIIR溴含量的影响
通常要求结构Ⅰ和结构Ⅲ的含量要小于20%,结构Ⅱ的含量要大于60%,这是因为结构Ⅰ(为未溴化的丁基橡胶)过多则说明溴化的效率低,而结构Ⅲ含量过高会降低焦烧安全性。
Vukov R[7]揭示了溴化丁基橡胶模型化合物在150℃下加热一定时间,则聚合物分子结构将会发生重排,该反应历程如式(3)所示。

150℃下,不同停留时间对BIIR微观结构的影响见图4。

Fig.4 The effect of residence time to microstructure of BIIR at 150℃图4 150℃下不同预热时间对BIIR微观结构的影响
由图4可以看出,在150℃下,随着胶料在料筒中停留时间延长,结构Ⅲ含量由10%增至21%,而结构Ⅱ的含量由70%降至50%,结合(3)式可以推断出,随着受热时间增加,溴化丁基橡胶中的烯丙基溴发生了一定程度的脱卤化,Ⅱ结构(伯位)向Ⅲ结构(仲位)重排,这是因为溴代伯位烯丙基比溴代仲位烯丙基的热稳定性更好[8],而卤素原子从仲位到伯位的重排程度与脱卤化氢程度成正比。脱除的HBr会形成酸性环境,促进仲位向伯位烯丙基重排。
180℃下,不同停留时间对BIIR微观结构的影响见图5。
由图5可以看出180℃下,溴化丁基橡胶的3种微观结构变化趋势与150℃时相同,并且在180℃下,胶料在被加热10min时,Ⅱ结构的损失为29.4%,Ⅲ结构的含量则增加了116%(150℃下加热1 0min时这两种微观结构的变化量分别是14.3%和70.0%),说明升高温度会促进脱溴化氢反应,并且会加速Ⅱ结构和Ⅲ结构之间的重排。

Fig.5 The effect of residence time to microstructure of BIIR at 180℃图5 180℃下不同停留时间对BIIR微观结构的影响
3 结束语
利用毛细管流变仪的结构特性模拟螺杆挤出机挤出干燥过程,实验结果表明,溴化丁基橡胶在一定温度下停留会发生脱溴化氢反应导致溴含量减少,且仲位烯丙基结构会减少,伯位烯丙基结构增加,这是由于仲位烯丙基向热稳定性更好的伯位烯丙基转化,延长停留时间和升高温度都会加剧这一现象。
[1] 钱寒东.溴化丁基橡胶性能研究[J].世界橡胶工业,2004,31(12):6-11.
[2] 谢遂志.橡胶工业手册[M].北京:化学工业出版社,1989.
[3] 伍一波,李树新,郭文丽.溴化丁基橡胶的制备与结构表征[J].合成橡胶工业,2006,29(4):267-270.
[4] Chia Yeh Chu,Rastko Vuko.Determination of the structure of butyl rubber by NMR Spectroscoppy[J].Macromolecules,1985,18:1423-1430.
[5] Cheng D M,Gardner I J,Wang H C,et al.Spectroscopic studies of the structures of butyl rubber and bromobutyl rubbers[J].Rubber chemistry and technology,1990,63:265-275.
[6] Cottle Delmer L,Minckler Jr Leon S,Theodore Lemiszka.Process for brominating copolymers:US,2962482[P].1960-11-29.
[7] Van Tongerloo A,Vukov R.Butyl rubber-halogenation mechanisms[R].Milan Italy:Proceeding of international rubber conference,1979.
[8] Gardner I J,Fanwood N J.Conjugated diene butyl elastomer copolymer:US,4288575[P].1981-09-08.
