芒果苷衍生物的合成及其PTP1B酶抑制活性研究
2011-11-22胡丽娜罗剑飞俞世冲吴秋业
周 宇,胡丽娜,罗剑飞,俞世冲,吴秋业
(1.解放军第82医院,江苏 淮安 223001; 2. 第二军医大学有机化学教研室,上海 200433)
芒果苷衍生物的合成及其PTP1B酶抑制活性研究
周 宇1,胡丽娜2,罗剑飞2,俞世冲2,吴秋业2
(1.解放军第82医院,江苏 淮安 223001; 2. 第二军医大学有机化学教研室,上海 200433)
目的设计合成一系列芒果苷衍生物并进行体外蛋白酪氨酸磷酸酶1B(PTP1B)抑制活性实验。方法利用亲核取代反应在芒果苷上引入疏水苄基,设计合成8个新化合物4~11,采用比色法对化合物进行PTP1B抑制活性研究。结果设计合成的8个化合物对PTP1B酶都有一定的抑制作用。结论芒果苷衍生物的活性明显好于芒果苷本身的活性,苄基的对位取代活性要优于邻位和间位取代,且苄基上氯原子取代的衍生物要高于其它原子取代的化合物活性。
芒果苷;蛋白酪氨酸磷酸酶1B;化学合成;抑制活性
1 前言
芒果苷(mangiferin),又名芒果素,知母宁,是从百合科植物知母中提取的天然多酚类化合物,分子式为C19H18O11。芒果苷有多种重要生理活性,如抗氧化[1]、抗肿瘤[2]、抗炎[3]、神经保护[4]以及ACAT酶抑制作用[5]等。近来研究发现芒果苷通过抑制蛋白酪氨酸磷酸酶1B(PTP1B)表现出较好的抗糖尿病活性[6,7]。
PTP1B是胰岛素转导通路关键的负调控因子,它可以控制通路中信号蛋白(包括胰岛素受体) 的去磷酸化,拮抗激酶催化的磷酸化反应,从而对生物体产生影响[8~10]。临床研究发现PTP1B酶抑制剂可以通过降低PTP1B浓度来增强胰岛素的活性,PTP1B是治疗Ⅱ型糖尿病和肥胖症的有效靶点[11,12],因此关于PTP1B抑制剂的研究也成为国际研究的热点之一。
芒果苷本身溶解性不好,限制了进一步的应用。廖洪利等[13]其进行结构改造,引入烷基和苄基以提高其溶解性,并且发现结果化合物2和3有良好的 PTP1B酶抑制活性。基于以上研究,笔者设计合成了一系列苄基取代的芒果苷衍生物,并且对这些化合物进行PTP1B酶抑制活性测试。
2 合成实验
熔点用YRT-3熔点测定仪(温度未经校正)测定;质谱用安捷伦1100型质谱仪测定;核磁共振氢谱用Varian INOVA-600型核磁共振仪(DMSO-d6为溶剂,TMS为内标)测定。所用试剂均为市售分析纯。
2.1目标化合物4-11的合成 将芒果苷(420 mg, 1 mmol)溶于干燥的DMF (20 ml),加入碳酸钾(100 mg), 搅拌20 min后加入取代的氯苄(4 mmol),搅拌,油浴加热60 ℃, 10 h后,TLC显示反应完全。将反应混合液真空浓缩,柱层析,二氯甲烷/甲醇为洗脱剂,得到438 mg淡黄色粉末,为目标化合物4。其它目标化合物5-11均按此法合成,合成路线如图1,其结构、产率、熔点、MS和1H NMR数据见表1。

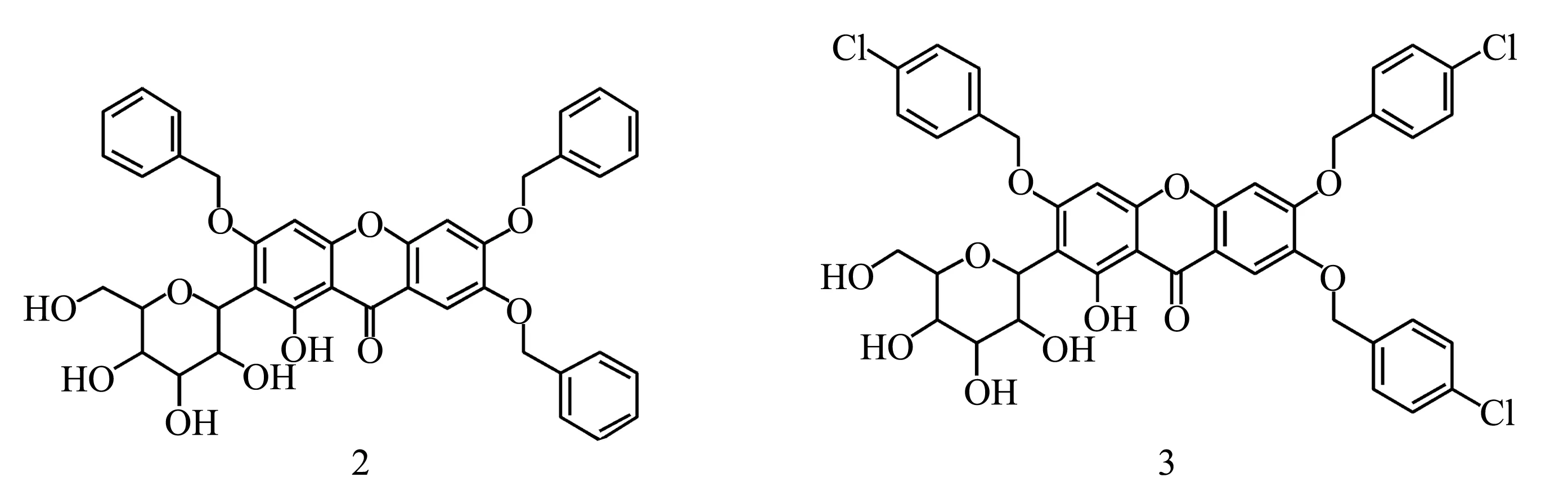
图1 目标化合物的合成路线
表1目标化合物的结构、熔点和光谱数据

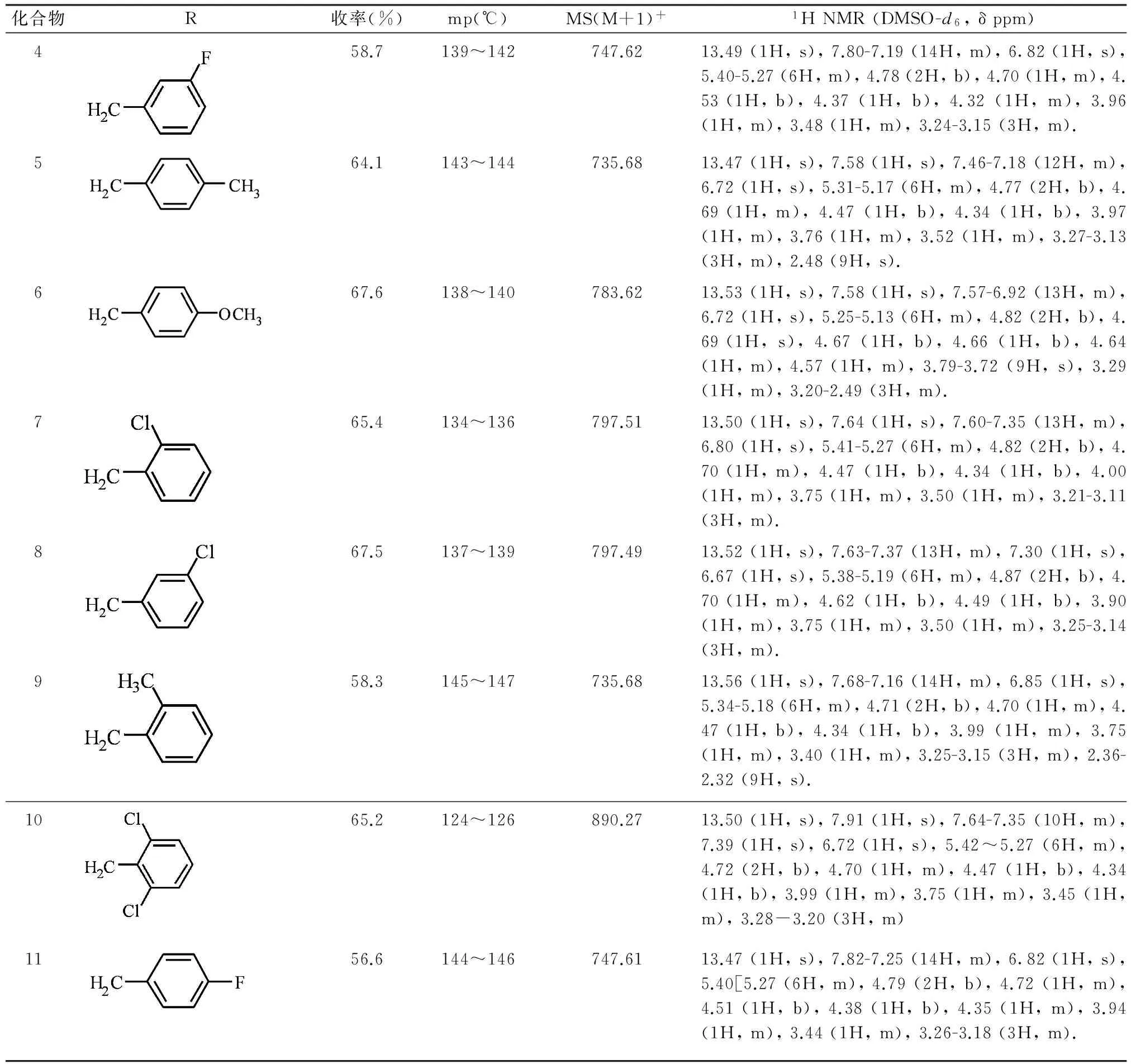
化合物R收率(%)mp(℃)MS(M+1)+1HNMR(DMSO-d6,δppm)458.7139~142747.6213.49(1H,s),7.80-7.19(14H,m),6.82(1H,s),5.40-5.27(6H,m),4.78(2H,b),4.70(1H,m),4.53(1H,b),4.37(1H,b),4.32(1H,m),3.96(1H,m),3.48(1H,m),3.24-3.15(3H,m).564.1143~144735.6813.47(1H,s),7.58(1H,s),7.46-7.18(12H,m),6.72(1H,s),5.31-5.17(6H,m),4.77(2H,b),4.69(1H,m),4.47(1H,b),4.34(1H,b),3.97(1H,m),3.76(1H,m),3.52(1H,m),3.27-3.13(3H,m),2.48(9H,s).667.6138~140783.6213.53(1H,s),7.58(1H,s),7.57-6.92(13H,m),6.72(1H,s),5.25-5.13(6H,m),4.82(2H,b),4.69(1H,s),4.67(1H,b),4.66(1H,b),4.64(1H,m),4.57(1H,m),3.79-3.72(9H,s),3.29(1H,m),3.20-2.49(3H,m).765.4134~136797.5113.50(1H,s),7.64(1H,s),7.60-7.35(13H,m),6.80(1H,s),5.41-5.27(6H,m),4.82(2H,b),4.70(1H,m),4.47(1H,b),4.34(1H,b),4.00(1H,m),3.75(1H,m),3.50(1H,m),3.21-3.11(3H,m).867.5137~139797.4913.52(1H,s),7.63-7.37(13H,m),7.30(1H,s),6.67(1H,s),5.38-5.19(6H,m),4.87(2H,b),4.70(1H,m),4.62(1H,b),4.49(1H,b),3.90(1H,m),3.75(1H,m),3.50(1H,m),3.25-3.14(3H,m).958.3145~147735.6813.56(1H,s),7.68-7.16(14H,m),6.85(1H,s),5.34-5.18(6H,m),4.71(2H,b),4.70(1H,m),4.47(1H,b),4.34(1H,b),3.99(1H,m),3.75(1H,m),3.40(1H,m),3.25-3.15(3H,m),2.36-2.32(9H,s).1065.2124~126890.2713.50(1H,s),7.91(1H,s),7.64-7.35(10H,m),7.39(1H,s),6.72(1H,s),5.42~5.27(6H,m),4.72(2H,b),4.70(1H,m),4.47(1H,b),4.34(1H,b),3.99(1H,m),3.75(1H,m),3.45(1H,m),3.28-3.20(3H,m)1156.6144~146747.6113.47(1H,s),7.82-7.25(14H,m),6.82(1H,s),5.40[5.27(6H,m),4.79(2H,b),4.72(1H,m),4.51(1H,b),4.38(1H,b),4.35(1H,m),3.94(1H,m),3.44(1H,m),3.26-3.18(3H,m).
3 药理实验
根据Goldstein等人的方法测定化合物的酶抑制活性[14]。将化合物用DMSO配制成浓度分别为20 μg/ml和4 μg/ml的供试品溶液,以p-NPP为底物,实验混合液包含10 mmol/L p-NPP,50 mmol/L HEPES缓冲液 (pH 7.0)以及1 mmol/L EDTA和DTT。当向体系中加入500 ml 0.1 mol/L NaOH时,反应停止,测定410 nm时的光吸收度。不含酶实验组用来校正非酶反应和反应体系中产生的对硝基苯酚盐离子浓度,用摩尔消光系数1.78×104来测定体系中对硝基苯酚盐离子浓度,钒酸钠为对照组(IC50, 2 mmol/L)。该类化合物的PTP1B酶抑制活性测试实验结果如表2所示。
从药理活性筛选结果发现:该类化合物表现出良好的PTP1B酶抑制活性。在4 mg/ml的浓度时,化合物8, 10和11的PTP1B酶抑制活性分别为24.1%, 37.6%, 40.9%。芒果苷本身的PTP1B酶抑制活性较弱,但是将芒果苷的C-3, C-6, C-7酚羟基取代可以显著增强抑制活性。构效关系表明:带有氯原子取代苄基的化合物活性要优于其他基团取代苄基的化合物。通过比较化合物4, 5和10, 11的活性,还发现:苄基的对位取代要优于邻位和间位取代的活性。
4 结论
目前国际上通过天然产物分离或化学合成的PTP1B酶抑制剂,由于电负性高、细胞膜通透性差及专一性差等原因,离最终成为临床药物还有一定距离。本课题以天然产物芒果苷为先导化合物,设计合成了一系列新衍生物4-11,并对其进行体外PTP1B 酶抑制活性测定,结果表明该类化合物表现出一定的PTP1B酶抑制活性,为以后对芒果苷进一步的结构修饰和构效关系研究奠定了基础。
表2目标化合物的体外PTP1B酶抑制活性


化合物RInh(%)20μg/ml4μg/ml4a-5a2.46a-745.4-8a24.19a-1061.937.611a40.9
注:a加入缓冲液后样品出现沉淀。
[1] Pardo-Andreu GL, Rene D, Alberto J,etal.MangiferaindicaL, extract (Vimang) inhibits 2-deoxyribose damage induced by Fe (Ⅲ) plus ascorbate[J].Phytother Res, 2006, 20(2):120.
[2] 彭志刚,罗 军,赖永熔,等.芒果苷对K562胞端粒酶活性和细胞周期的影响[J].中药药理与临床,2007, 23(1): 13.
[3] Rivera DG, Balmaseda IH, Leon AA,etal. Anti-allergic properties ofManglferaindicaL. extract (Vimang) and contribution of its glueosylxanthone mangiferin[J]. J Pham Pharmacol, 2006, 58(3): 385.
[4] Gottlieb M, Leal-Campanario R, Campos-Esparza MR,etal. Neuroprotection by two polyphenols following excitotoxicity and experimental ischemia[J]. Neurobiology of Disease, 2006, 23(2): 374.
[5] Hu HG, Liao HL, Zhang J,etal. First identification of xanthone sulfonamides as potent acyl-CoA: cholesterol acyltransferase (ACAT) inhibitors[J]. Bioorg Med Chem Lett, 2010, 20(10): 3094.
[6] Miura T, Ichiki H, Iwamoto N,etal. Antidiabetic activity of the rhizoma ofAnemarrhenaasphodeloidesand active components, mangiferin and its glucoside[J]. Biol Pharm Bull, 2001, 24(9): 1009.
[7] Miura T, Ichiki H, Hashimoto I,etal. Antidiabetic activity of a xanthone compound, mangiferin[J]. Phytomedicine, 2001, 8(2): 85.
[8] Pei Z, Liu G, Lubben TH,etal. Inhibition of protein tyrosine phosphatase 1B as a potential treatment of diabetes and obesity[J]. Curr Pharm Des, 2004, 10(28): 3481.
[9] Dadke S, Chernoff J. Protein-tyrosine phosphatase 1B as a potential drug target for obesity[J]. Curr Drug Targets Immune Endocr Metabol Disord, 2003, 3(4): 299.
[10] Kim HO, Blaskovich MA. Recent discovery and development of protein tyrosine phosphatase inhibitors[J]. Expert Opin Ther Patents, 2002, 12(6): 871.
[11] Elchebly M, Payette P, Michaliszyn E,etal. Increased insulin sensitivity and obesity resistance in mice lacking the protein tyrosine phosphatase-1B gene[J]. Science, 1999, 283(5407): 1544.
[12] Klaman LD, Boss O, Peroni OD,etal. Increased energy expenditure, decreased adiposity, and tissue-specific insulin sensitivity in protein-tyrosine phosphatase 1B-deficient mice[J]. Mol Cell Biol, 2000, 20(15): 5479.
[13] 廖洪利,陈 军,杨 倩.芒果苷衍生物的制备[J].药学实践杂志,2010, 27(5): 49.
[14] Goldstein BJ, Bittner-Kowalezyk A, White MF,etal. Tyrosine dephosphorylation and deactivation of insulin receptor substrate-1 by protein-tyrosine phosphatase 1B: Possible facilitation by the formation of a ternary complex with the GRB2 adaptor protein[J]. J Biol Chem, 2000, 275: 4283.
2011-01-06
[修回日期] 2011-03-10
SynthesisandPTP1Bactivityofenzymeinhibitionofmangiferinderivates
ZHOU Yu1, HU Li-na2, LUO Jian-fei2, YU Shi-chong2,WU Qiu-ye2
(1.NO. 82 Hospital of PLA, Huaian 223001,China; 2. Department of Organic Chemistry,School of Pharmacy,Second Military Medical University,Shanghai 200433,China)
ObjectiveTo synthetize and conduct PTP1B inhibitory activity experiment of series of novel mangiferin derivates.MethodsDifferent benzyl groups were introduced to mangiferin framework by nucleophilic substitution reaction. All the compounds were screened against protein tyrosine phosphatase 1B(PTP1B)with the colorimetrie assay.ResultsEight compounds were synthesized and all the compounds exhibited PTP1B inhibitory activity to some extent.ConclusionsDerivates of mangiferin remarkably enhanced the activity compared with mangiferin itself. In addition, the benzylated derivates with chloro atom had better inhibitory activity than other substitution groups. Furthermore,theparaposition of the benzyl was a better place for introducing substituent thanmetaandorthoposition.
mangiferin; protein tyrosine phosphatase 1B; chemical synthesis; inhibition
上海市科委基础重点项目 ( 08JC1405500).
周 宇(1962-),女,副主任药师.
吴秋业. Tel: (021)81871225, E-mail: wuqy6439@sohu.com.
R914.5
A
1006-0111(2011)03-0193-04
