舒筋通络外用颗粒的质量标准研究
2011-11-09潘志文广东佛山市药品检验所佛山市528000
潘志文(广东佛山市药品检验所,佛山市 528000)
舒筋通络外用颗粒为佛山市顺德区龙江医院的外用制剂,处方由大黄、当归、桂枝、独活等13味药材组成,其中大黄、当归、桂枝、独活以细粉入药,其余药味用水煎煮提取,提取液浓缩后与上述细粉混匀,制成颗粒。其用温水溶解后薰洗患处,具有温经通络、祛瘀止痛之功,用于治疗跌打损伤、筋骨疼痛、关节不利。为了控制该制剂质量,笔者采用薄层色谱(TLC)法对方中大黄、当归、桂枝、独活作定性鉴别,采用高效液相色谱(HPLC)法测定主药大黄有效成分大黄素和大黄酚的含量。
1 仪器与试药
1100型HPLC仪,包括Agilent化学工作站(美国Agilent公司);AE240电子分析天平(瑞士Mettler Toleto公司);KQ300超声波清洗器(昆山市超声仪器有限公司,频率:40 kHz,功率:300 W)。
大黄、当归、桂枝、独活对照药材和大黄素、大黄酚对照品(中国药品生物制品检定所,批号分别为9022-200207、9271-200110、1191-200101、0940-200205、110756-200110、110796-200311);舒筋通络外用颗粒样品(批号:0701、0702、0703)及阴性样品均由佛山市同德区龙江医院提供;薄层层析硅胶G(化学纯,青岛海洋化工集团公司);甲醇为色谱纯,水为超纯水,其余试剂均为分析纯。
2 定性鉴别
2.1 当归、桂枝、独活的TLC鉴别[1]
取本品3 g,研细,加乙醚40 mL,超声处理10 min,滤过,滤液置分液漏斗中,用0.1 mol·L-1氢氧化钠溶液洗涤3次,每次20 mL,洗液合并,备用,乙醚液再用水10 mL洗涤1次,挥干,残渣加无水乙醇1 mL使溶解,作为供试品溶液;取当归对照药材0.8 g、桂枝对照药材0.2 g、独活对照药材0.5 g,分别加乙醚30 mL,超声处理10 min,滤过,滤液挥干,残渣加无水乙醇1 mL使溶解,作为相应的对照药材溶液;分别取缺当归、缺桂枝、缺独活的阴性样品各3 g,按供试品溶液的制备方法制成相应的阴性对照溶液。照TLC法[1]试验,吸取上述7种溶液各2 μL,分别点于同一以羧甲基纤维素钠为黏合剂的硅胶G薄层板上,以石油醚(30~60 ℃)-甲酸乙酯-甲酸(15∶5∶1)的上层溶液为展开剂,展开,取出,晾干,置紫外光灯(365 nm)下检视。结果,供试品色谱中,在与当归对照药材色谱相应的位置上,显相同的亮蓝白色荧光斑点;在与桂枝对照药材色谱相应的位置上,显相同的绿色荧光斑点;在与独活对照药材色谱相应的位置上,显相同的蓝紫色荧光斑点;阴性对照无干扰。当归、桂枝、独活的TLC见图1。
2.2 大黄的TLC鉴别[1]
取“2.1”项下备用之洗液适量,用1 mol·L-1盐酸溶液调节pH值至1~2,用乙醚提取3次,每次20 mL,合并提取液,挥干,残渣加无水乙醇5 mL使溶解,作为供试品溶液;取大黄对照药材0.1 g,加乙醚30 mL,超声处理10 min,滤过,滤液挥干,残渣加无水乙醇1 mL使溶解,作为对照药材溶液;取缺大黄阴性样品3 g,按供试品溶液的制备方法制成阴性对照溶液。照TLC法[1]试验,吸取上述3种溶液各5 μL,分别点于同一以羧甲基纤维素钠为黏合剂的硅胶G薄层板上,以石油醚(30~60℃)-甲酸乙酯-甲酸(15∶5∶1)的上层溶液为展开剂,展开,取出,晾干,置紫外光灯(365 nm)下检视。结果,供试品色谱中,在与对照药材色谱相应的位置上,显相同的5个橙黄色荧光主斑点;阴性对照无干扰。大黄的TLC见图2。
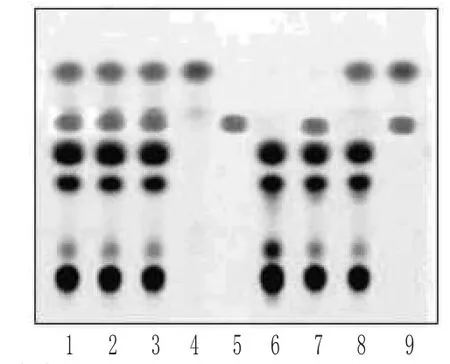
图1 当归、桂枝、独活的TLC1~3.供试品;4.当归对照药材;5.桂枝对照药材;6.独活对照药材;7.缺当归阴性对照;8.缺桂枝阴性对照;9.缺独活阴性对照Fig1 TLC of Angelica sinensis,Cinnamomum cassia and A.pubescens1~3.test samples;4.Angelicae Sinensis Radix reference substance;5.Cinnamomi Ramulus reference substance;6.Angelicae Pubescentis Radix reference substance;7.negative control without A.Sinensis;8.negative control without C.cassia;9.negative control withoutA.Pubescentis
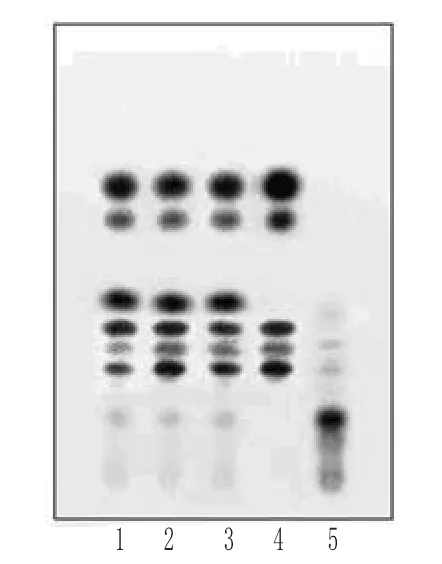
图2 大黄的TLC1~3.供试品;4.大黄对照药材;5.缺大黄阴性对照Fig2 TLC of Rhei Radix Et Rhizoma1~3.test samples;4.Rhei Radix et Rhizoma reference substance;5.negative control without Rhei Radix Et Rhizoma
3 含量测定[2]
3.1 色谱条件
色谱柱:Hypersil ODS2(200 mm×4.6 mm,5 μm);流动相:甲醇-0.1%磷酸溶液(85∶15);流速:1.0 mL·min-1;检测波长:254 nm;柱温:30 ℃;进样量:10 μL。
3.2 溶液的制备
3.2.1 供试品溶液的制备 取本品适量,研细,取约1 g,精密称定,置具塞锥形瓶中,精密加入甲醇25 mL,称定重量,加热回流1 h,放冷,再称定重量,用甲醇补足失重,摇匀,滤过。精密量取续滤液5 mL,置烧瓶中,挥去溶剂,加8%盐酸溶液10 mL,超声处理2 min,再加三氯甲烷10 mL,加热回流1 h,放冷,置分液漏斗中,用少量三氯甲烷洗涤容器,并入分液漏斗中,分取三氯甲烷层,酸液再用三氯甲烷提取3次,每次10 mL,合并三氯甲烷液,减压回收溶剂至干,残渣加甲醇使溶解,转移至10 mL量瓶中,加甲醇至刻度,摇匀,滤过,取续滤液,即得。
3.2.2 混合对照品溶液的制备 精密称取大黄素对照品和大黄酚对照品适量,加甲醇制成每1 mL含大黄素10 μg、大黄酚25 μg的混合溶液,即得。
3.2.3 阴性对照溶液的制备 取缺大黄阴性样品适量,按“3.2.1”项下方法制备阴性对照溶液。
3.3 空白试验
取上述混合对照品溶液、供试品溶液和阴性对照溶液各适量,按上述色谱条件进样测定。结果,阴性对照溶液在大黄素、大黄酚对照品色谱峰相应的位置上无干扰峰。色谱见图3。
3.4 线性关系考察
精密吸取混合对照品溶液 1、2、5、10、20、50 μL,注入HPLC仪,按上述色谱条件测定。分别以大黄素、大黄酚进样量(X)为横坐标,峰面积积分值(Y)为纵坐标,进行线性回归,得回归方程分别为Y大黄素=3 737.4X大黄素-1.365 9(r=0.999 9,n=6)、Y大黄酚=5 224.3X大黄酚-3.870 6(r=0.999 9,n=6)。结果表明,大黄素、大黄酚进样量分别在0.01~0.50、0.025~1.250 μg范围内与各自峰面积积分值呈良好线性关系。
3.5 精密度试验
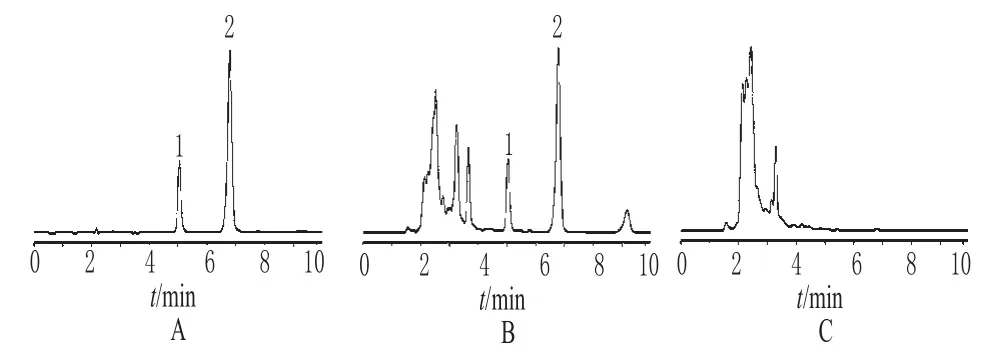
图3 高效液相色谱图A.混合对照品;B.供试品;C.阴性对照;1.大黄素;2.大黄酚Fig3 HPLC chromatogramsA.mixed control;B.test sample;C.negative control;1.emodin,2.chrysophanol
精密吸取混合对照品溶液10 μL,重复进样6次,按上述色谱条件测定。结果,大黄素、大黄酚峰面积的RSD均为0.2%(n均为6),表明仪器精密度良好。
3.6 稳定性试验
精密吸取供试品溶液,分别于0、1、2、3、4、24 h注入HPLC仪,按上述色谱条件测定。结果,大黄素峰面积的RSD=0.2%,大黄酚峰面积的RSD=0.1%(n均为6),表明供试品溶液在24 h内稳定。
3.7 重复性试验
精密称取同一批样品适量,共6份,按“3.2.1”项下方法制备供试品溶液,按上述色谱条件测定,记录峰面积;另精密吸取混合对照品溶液10 μL,同法测定,外标法计算大黄素和大黄酚含量。结果,大黄素和大黄酚平均含量的RSD分别为1.3%和1.4%(n均为6),表明方法重复性良好。
3.8 加样回收率试验
取已知含量的样品(含大黄素0.665 4 mg·g-1、大黄酚1.640 mg·g-1)6份,各约0.5 g,精密称定,分别精密加入对照品溶液(含大黄素 50.00 μg·mL-1、大黄酚125.00 μg·mL-1)各 5 mL,混匀,水浴蒸干,按“3.2.1”项下方法制备供试品溶液,按上述色谱条件测定,记录峰面积;另精密吸取混合对照品溶液10 μL,同法测定,外标法计算样品含量,并计算加样回收率,结果见表1。
3.9 样品含量测定
取3批样品适量,分别按“3.2.1”项下方法制备供试品溶液,按上述色谱条件测定,记录峰面积;另精密吸取对照品溶液10 μL,同法测定,用外标法计算样品中大黄素和大黄酚的含量,结果见表2。
4 讨论
因大黄的5个蒽醌类成分对当归、桂枝、独活的TLC鉴别有干扰,故先用0.1 mol·L-1的氢氧化钠溶液将其分离出去。曾用石油醚(60~90℃)-醋酸乙酯(4∶1)为展开剂对供试品溶液进行薄层层析,但当归的色谱斑点与桂枝的色谱斑点分离度欠佳,当选用大黄的TLC展开剂系统时,当归、桂枝、独活的色谱成分均能达到有效分离。大黄的蒽醌类成分用0.1 mol·L-1的氢氧化钠溶液分离出来后,用1 mol·L-1盐酸溶液酸化,再用乙醚进行提取,制得的供试品溶液与当归、桂枝、独活的鉴别同板展开。一块板同时鉴别4个药材成分,方便、省时。
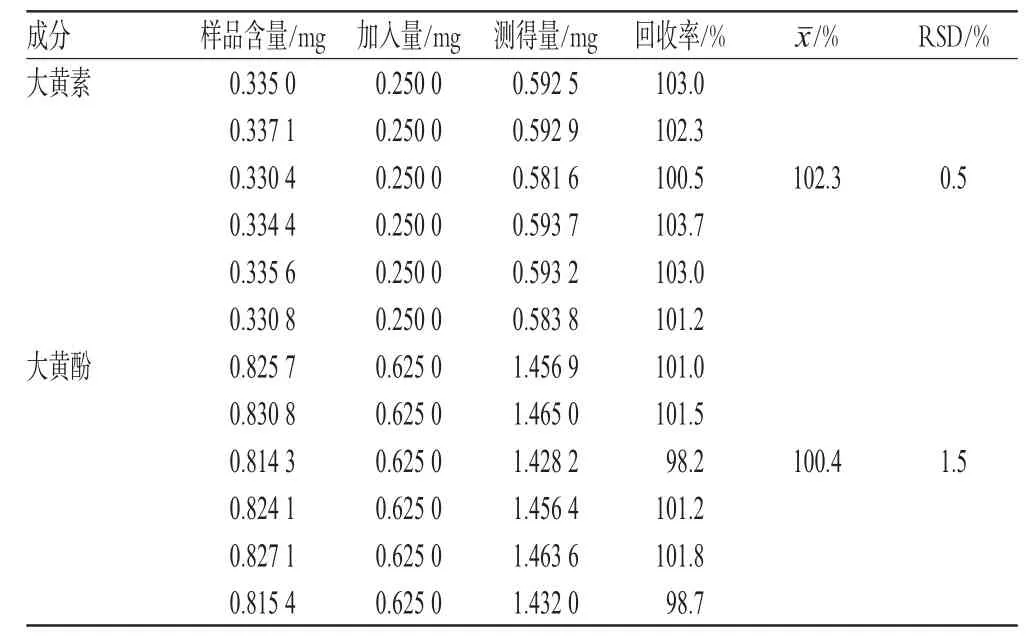
表1 加样回收率试验结果(n=6)Tab 1Results of recovery tests(n=6)
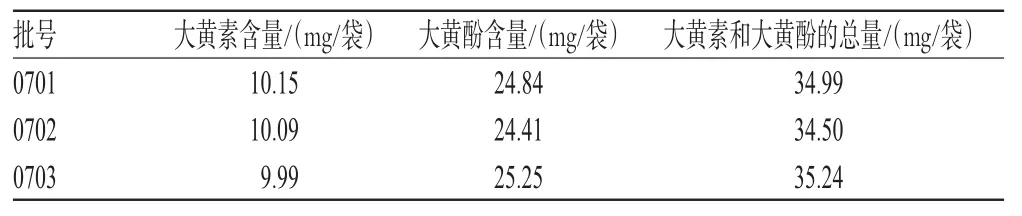
表2 样品含量测定结果Tab2 Results of content determination
本品处方由13味中药组成,其中大黄为主药,大黄素和大黄酚是其主要有效成分,故选其为含量测定指标。参照2010年版《中国药典》(一部)“大黄”项下收载的含量测定方法,采用HPLC法测定两者的总量。结果表明,在选定的色谱条件下,其他成分不干扰大黄素和大黄酚的测定,系统的适用性、方法回收率符合要求,测定结果准确、重复性好。
按2010年版《中国药典》(一部)“大黄”项下的质量要求,结合本制剂大黄的处方量,暂订本品每袋含大黄按大黄素和大黄酚的总量计,不得少于13.0 mg。
[1]国家药典委员会编.中华人民共和国药典(一部)[S].2010年版.北京:中国医药科技出版社,2010:附录34、22、124、246、259.
[2]郭 澄,王雯佶,江春霞,等.高效液相色谱法测定减肥降脂片中大黄酸、大黄素的含量[J].中国药房,2003,14(4):241.
