HPLC指纹图谱结合系统聚类分析法对灵芝孢子油质量的研究
2011-11-09冯柏康李其凤李卫民广州中医药大学广州市510405
冯柏康,李其凤,李卫民,肖 飞(广州中医药大学,广州市 510405)
灵芝孢子油是以灵芝Ganoderma lucidum(Leysds.Fr.)Karst.在生长成熟期产生的孢子为原料,采用超临界CO2技术获得的提取物。现代药理研究证明,灵芝孢子油具有多种生物活性。目前,在已上市的灵芝孢子油中,多以灵芝总三萜作为产品的功效性成分,大部分厂家在测定该成分时采用的是分光光度法。在试验应用中,笔者发现这种方法的专属性、稳定性及重复性均较差,测定结果难以准确反映灵芝孢子油中三萜类成分的含量。同时,灵芝孢子油中是否含有灵芝三萜在学术界仍存在一定的争议,灵芝孢子油的质量控制标准仍需进一步深入研究。鉴于此,笔者采用反相高效液相色谱(RP-HPLC)法,按照《中药注射剂指纹图谱研究的技术要求(暂行)》[1],对灵芝孢子油进行分析,建立灵芝孢子油HPLC指纹图谱[2],尝试为灵芝孢子油的质量控制提供一种新思路;并采用系统聚类法[3,4]对样品的指纹图谱进行分析,考察不同采收时间、产地及破壁工艺对灵芝孢子油质量的影响。
1 仪器与试药
2695型HPLC仪、2420型蒸发光散射检测器、WATERS EMPOWER色谱工作站(美国Waters公司)。
甲醇、异丙醇为色谱纯;甘油三油酸酯对照品(中国药品生物制品检定所,批号:111692-200901);样品由广州中医药大学首席教授徐鸿华提供并鉴定,为灵芝菌科灵芝G.lucidum(Leysds.Fr.)Karst.破壁孢子的超临界CO2提取物,根据其产地、采收时间、破壁工艺的差异按表1进行编号(由于涉及到商业秘密,样品的3个产地分别以字母开头的L、P、J代替,破壁工艺则以数字1和2代替)。
2 方法与结果
2.1 灵芝孢子油供试品溶液的制备
取灵芝孢子油20 mg,精密称定,置10 mL容量瓶中,用甲醇-异丙醇(40∶60)溶解并稀释至刻度,摇匀,过滤,取续滤液,即得。
2.2 参照峰的选择
灵芝孢子油气-质联用法的分析结果显示,甘油三油酸酯在灵芝孢子油中含量较高,也较为稳定,故选用甘油三油酸酯峰作为参照峰。
2.3 色谱条件与系统适用性试验
色谱柱:LiChrospher RP-18e(250 mm×4.6 mm,5 μm);流动相:甲醇(A)-异丙醇(B),梯度洗脱(洗脱顺序见表2);流速:0.8 mL·min-1;检测器漂移管温度:60 ℃;增益:135;压力:25 Psi。理论板数按甘油三油酸酯峰计算不小于3 000。
2.4 测定方法
分别取各批灵芝孢子油供试品溶液10 μL,注入液相色谱仪,记录1 h的色谱图,即得。
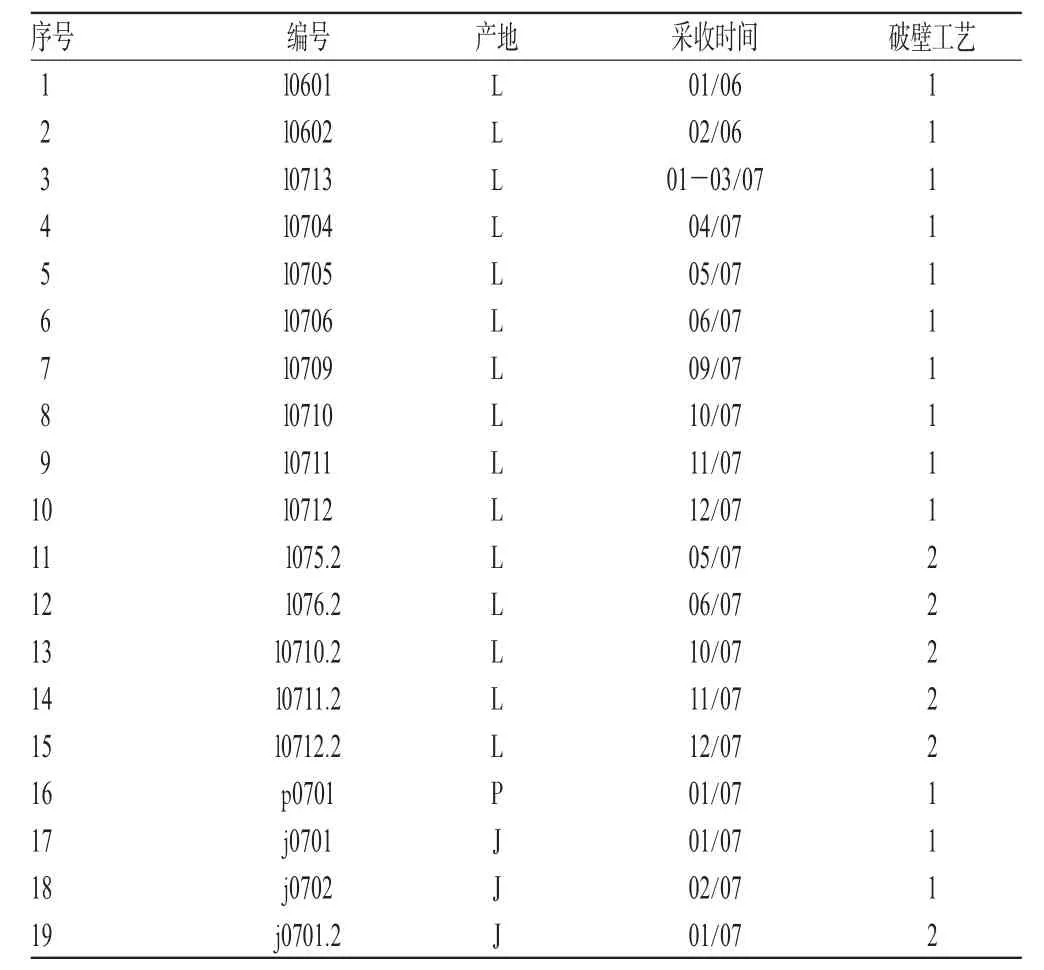
表1 19批灵芝孢子油原料的编号Tab1 The batch number of 19 batches of G.lucidum spore oil raw material
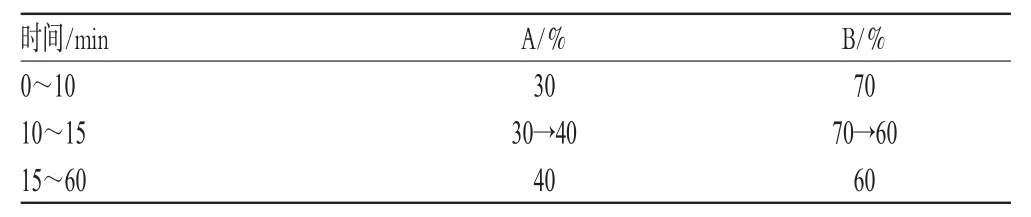
表2 梯度洗脱顺序Tab2 Gradient elution processes
2.5 方法学考察
2.5.1 精密度试验 取同一灵芝孢子油供试品溶液(p0701)适量,按上述色谱条件连续进样6次。结果,各供试品共有峰的相对峰面积和相对保留时间无明显变化(RSD<3%),表明本方法精密度良好。
2.5.2 稳定性试验 取同一灵芝孢子油供试品溶液(p0701)适量,按上述色谱条件分别于0、2、4、8、16、24 h进样测定。结果,24 h内各供试品共有峰的相对保留时间和相对峰面积无明显变化(RSD<3%),表明供试品溶液在24 h内保持稳定。
2.5.3 重复性试验 取同一批灵芝孢子油样品(p0701)适量,共6份,按“2.1”项下方法分别制备供试品溶液,按上述色谱条件进样测定。结果,各供试品共有峰的相对保留时间和相对峰面积无明显变化(RSD<3%),表明本方法重复性良好。
2.6 HPLC指纹图谱的建立
取各批灵芝孢子油样品适量,分别按“2.1”项下方法制备供试品溶液,按上述色谱条件进样分析,结果显示个别供试品的图谱差异比较大。19批灵芝孢子油的HPLC指纹图谱见图1。
2.7 系统聚类分析
从图1可见,19批灵芝孢子油并不完全一致。为寻找对灵芝孢子油质量影响的主要因素,现采用系统聚类分析法对样品HPLC指纹图谱中各特征峰进行分析,结果见图2。
从图2可见,上述19批灵芝孢子油可分为两大类,具体见表3。
3 分析
3.1 产地分析
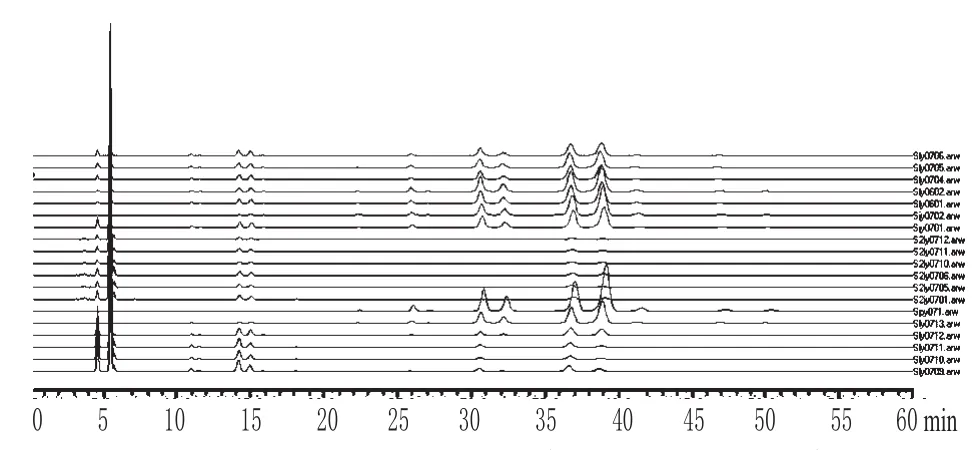
图1 19批灵芝孢子油的HPLC指纹图谱Fig1 HPLC fingerprint of 19 batches of G.lucidum spore oil
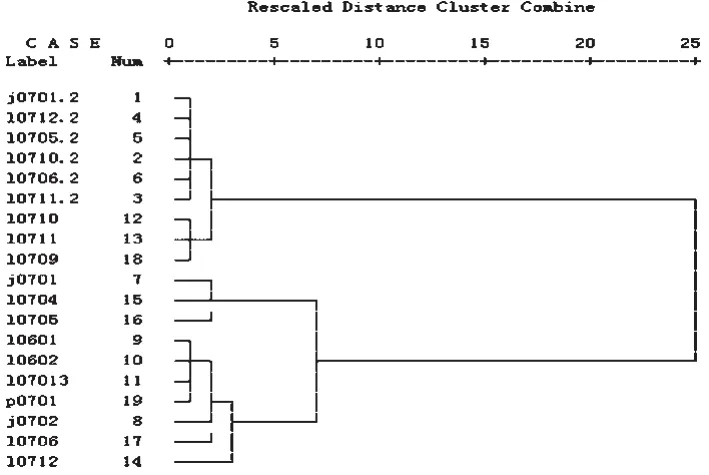
图2 离差平方和法对欧氏距离的聚类树形图Fig2 Clustering dendrogram of euclidean distance using sum of deviations squre method

表3 19批灵芝孢子油样品聚类分析结果Tab3 Results of cluster analysis of 19 batches of G.lucidum spore oil
图2显示,L、P、J产地的样品在聚类树形图中混合在一起,没有明确分开。提示不同产地之间灵芝孢子油的差别并不太大,初步推断产地对灵芝孢子油的质量不产生决定性影响。
3.2 采收时间分析
从图2可见,采用工艺1破壁的灵芝孢子,12、1、2、3、4、5、6月采收的孢子均聚于同一大类,而9、10、11月的聚于另一大类。由此推断,上一年12月-本年上半年(6月前)的孢子是基本相似的,而9、10、11月采收的孢子则与上述差别较大。较为可惜的是现无7、8月的数据,未能完全说明整年的变化。
3.3 破壁工艺分析
图2还显示,采用破壁工艺2所得的灵芝孢子在第一大类中是自成一小类的,说明破壁工艺对孢子油质量的影响是明显的。
4 讨论
从上述分析结果可见,同一批灵芝孢子原料在不同的破壁工艺下,所获得的灵芝孢子油有着显著的区别,破壁工艺对控制产品一致性的影响是明显的,因此厂家必须在充分试验后确定固定的破壁工艺。
从现有的试验结果看,上一年12月-本年上半年(6月前)的灵芝孢子是基本相似的,而9、10、11月采收的灵芝孢子则与上述差别较大。
针对目前灵芝孢子油有效成分尚不明确的现状,下一步的研究工作需通过对灵芝孢子油药理学与临床研究客观反映上述两大类灵芝孢子油的药理效能,确定灵芝孢子油最适宜的采收时间、破壁工艺等,从而稳定灵芝孢子油原料的来源;然后对灵芝孢子油建立标准化提取物的指纹图谱,解决产品的质量控制问题,最终使产品的质量标准基本稳定在同一水平上,达到控制中间体、成品的一致性,减少批间差异的目的。
[1]国家药品监督管理局.中药注射剂指纹图谱研究的技术要求(暂行)[J].中成药,2000,22(10):671.
[2]周玉新.中药指纹图谱研究技术[M].北京:化学工业出版社,2002:8.
[3]游元元,万德光,裴 谨,等.不同品种桑叶高效液相指纹图谱的聚类分析[J].时珍国医国药,2008,19(11):2 661.
[4]范俊安,夏永鹏,邱宗荫,等.重庆垫江牡丹皮HPLC指纹图谱研究(Ⅰ)——不同因素的影响及牡丹皮最适宜种植条件选择[J].中国药房,2009,20(21):1 667.
