正交试验优选盐酸川芎嗪脂质体的制备工艺
2011-11-21杜兆香鞠建峰山东中医药大学附属医院济南市250011
杜兆香,鞠建峰(山东中医药大学附属医院,济南市 250011)
正交试验优选盐酸川芎嗪脂质体的制备工艺
杜兆香*,鞠建峰(山东中医药大学附属医院,济南市 250011)
目的:优选盐酸川芎嗪脂质体的制备工艺。方法:以乙醚注入法制备川芎嗪脂质体,采用正交试验,以包封率为指标,以药物与大豆卵磷脂用量比、PBS缓冲液的pH值、胆固醇与大豆卵磷脂用量比、乙醚与PBS缓冲液用量比为考察因素,优选制备工艺。结果:最佳工艺条件为药物∶大豆卵磷脂为1∶12,PBS缓冲液pH为7.5,胆固醇∶大豆卵磷脂为1∶2,乙醚∶PBS缓冲液为1∶2。结论:该制备工艺可行、稳定、重现性好,可为工业化生产提供理论依据。
盐酸川芎嗪;脂质体;正交试验;制备工艺
川芎嗪是从川芎中提取的有效成分四甲基吡嗪的盐类,是川芎根茎中的主要活性生物碱。现代医学表明,川芎嗪是一种新型钙离子拮抗剂,具有活血化瘀、抗血小板凝集、扩张血管、改善微循环等作用,临床用于心绞痛、脑血管以及肺动脉高压等呼吸系统疾病的治疗[1~3]。盐酸川芎嗪脂质体通过鼻黏膜给药,直接吸收进入体内,通过血-脑脊液屏障,具有药物吸收快、显效迅速、作用时间长的特点。本研究在单因素考察的基础上,以包封率为评价指标,采用正交试验,对盐酸川芎嗪脂质体的制备工艺进行优化。
1 仪器与试药
LC-10ATVP-ODS高效液相色谱仪、SPD-10Avp紫外检测器(日本岛津公司);FA-1140电子天平(上海天平仪器厂);5200H超声振荡器(上海科岛超声仪器有限公司);82-5B磁力加热搅拌器(南通科学仪器厂);UV-2102PCS紫外-可见分光光度仪(上海尤尼柯仪器公司);pHS-2C精密酸度计(上海雷磁仪器厂);G-50Sephadex凝胶柱(上海化学试剂厂)。
盐酸川芎嗪对照品(中国药品生物制品检定所,批号:0817-9803);盐酸川芎嗪原料(北京市燕京制药厂,批号:020502);大豆卵磷脂(EPC,上海源聚生物制品有限公司进口分装);胆固醇(上海源聚生物制品有限公司);空白脂质体(山东中医药大学附属医院自制);甲醇为色谱纯,其他试剂均为分析纯。
2 方法与结果
2.1 单因素试验
选择盐酸川芎嗪为模型药物,EPC、胆固醇为基本成膜材料,采用乙醚注入法制备盐酸川芎嗪脂质体。以制剂的形态、均匀性、放置是否分层、包封率等为主要指标考察其工艺。
2.1.1 磷酸盐缓冲液(PBS)pH值的影响 本试验考察了pH值分别为4.0、5.0、6.0、6.5、6.8、7.2、7.6、8.0的一系列PBS对脂质体稳定性的影响。结果表明,在pH低于6.5的PBS中不能制成脂质体或制得的盐酸川芎嗪脂质体稳定性较差,室温静置数天内,即有分层或沉淀等现象产生。
2.1.2 EPC用量的影响 本试验发现在一定的药物治疗浓度下,随着EPC浓度的增加,药物的包封率也有所提高;但EPC用量过大时,水化完全较困难,又易发生凝聚现象,在显微镜下观察,可见较多的磷脂块,分散不够好。兼顾包封率和稳定性,药物与EPC用量的比在1∶8~1∶12范围内较好。
2.1.3 胆固醇用量的影响 胆固醇是脂质体类脂膜的重要组成部分,具有调节流动性及稳定脂质双分子膜的功能[4],对脂质体膜的通透性具有双向调节作用[5]。用量适当,能使脂质体膜的刚性增强,曲率半径减少,包封率和稳定性提高;用量过大,使脂质体膜刚性过强,容易破裂,导致药物渗漏;用量过少,使膜的流动性增加,影响药物释放。参考有关文献并结合预试验结果,胆固醇与EPC的用量比在1∶2~1∶7范围内较好。
2.1.4 PBS用量的影响 预试验发现,PBS用量较大时,水化困难,超声时间较长,制备的脂质体粒径较大。
2.1.5 水化方法的影响 本试验发现,由于电磁振荡速度快,水化均匀,因此用电磁振荡器进行水化比超声波水化所需时间短,且粒径小,故采用电磁振荡进行水化。
2.1.6 水化温度的影响 预试验发现,水化温度过高所制备的脂质体粒径分布不均,而且温度过高,EPC容易氧化,故选择25℃作为水化时所用温度。
2.2 制备工艺试验设计
根据单因素考察结果,把药物与EPC的用量比(A)、PBS的pH值(B)、胆固醇与EPC的用量比(C)、乙醚与PBS的用量比(D)作为4个考察因素,以乙醚注入法制备川芎嗪脂质体。因素水平见表1。
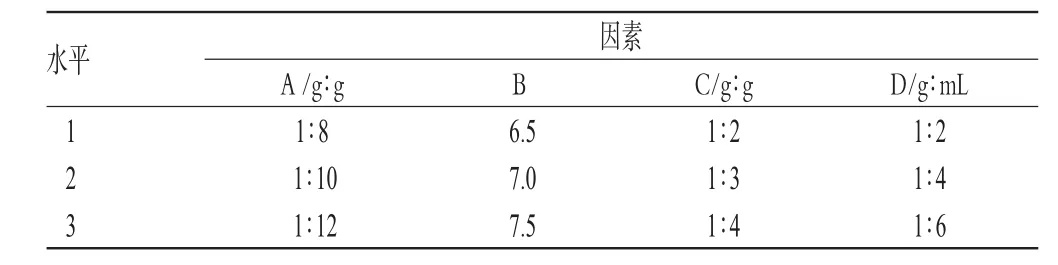
表1 因素水平Tab 1 Factor and levels
2.3 包封率的测定
2.3.1 色谱条件 色谱柱:SHIMADZU VP-ODS(150mm×4.6mm,10μm);流动相:甲醇-水(45∶55);流速:1.0mL·min-1;检测波长:292nm;柱温:室温;进样量:20μL。
2.3.2 标准曲线的制备 精密称取盐酸川芎嗪对照品0.008g,用生理盐水定容至25mL量瓶中,分别量取0.1、0.3、0.5、0.7、0.9mL,置于5mL量瓶中,加入生理盐水定容,制得浓度分别为6.4、19.2、32.0、44.8、57.6µg·mL-1的对照品溶液。分别取上述溶液20μL进样,测定峰面积。以峰面积积分值(Y)为横坐标,进样量(X)为纵坐标,进行线性回归,得回归方程为Y=0.0053X-12.259(r=0.9999,n=5)。结果表明,盐酸川芎嗪的进样量在6.4~57.6µg范围内与峰面积积分值呈良好的线性关系。
2.3.3 凝胶柱分离测定脂质体中游离药物浓度 吸取一定量的脂质体,上样于已用生理盐水平衡好的G-50Sephadex柱(1.0cm×20cm)上,用生理盐水洗脱,流速为0.5mL·min-1,分次收集洗脱液,每次1.0mL,通过观察流动池内溶液吸光度的变化监测脂质体与药物的分离情况。收集游离药物于50mL量瓶中,定容,取溶液适量经0.45µm微孔滤膜滤过,进样20μL,测定峰面积,以外标法计算药物浓度。
2.3.4 脂质体包封率的计算 包封率是脂质体的一个重要质量指标,一般可以用重量包封率(Qw)、体积包封率(Qv)或药脂包封比(Ew)来表示。本试验采用Qw来表示,即单位体积包入脂质体内的药物量(总药量-游离药物量,W包封)与总药量(W总)的比值,可用下式计算:Qw(%)=W包封/W总×100%。
2.4 正交试验结果
按表1中的安排制备9份样品,照“2.3”项下方法测定包封率,平行测定3次,以包封率总和(Y)为评价指标,优选工艺。正交试验结果见表2;方差分析结果见表3。
由表2、表3可知,各因素均对川芎嗪脂质体包封率有显著性影响,其影响大小依次为B>A>D>C,最佳处方组合为A3B3C1D1,即在pH7.5的PBS中,选用药物∶EPC为1∶12、胆固醇∶EPC为1∶2、乙醚∶PBS为1∶2的比例制备脂质体。
2.5 工艺验证试验
按优化处方制备3批盐酸川芎嗪脂质体,照“2.3”项下方法测定包封率。结果,3批样品的包封率分别为75.56%、77.73%、76.19%,均在理论预测范围之内,表明优化的处方重现性好,其包封率稳定。

表2 正交试验结果Tab 2 Result of orthogonal experiment
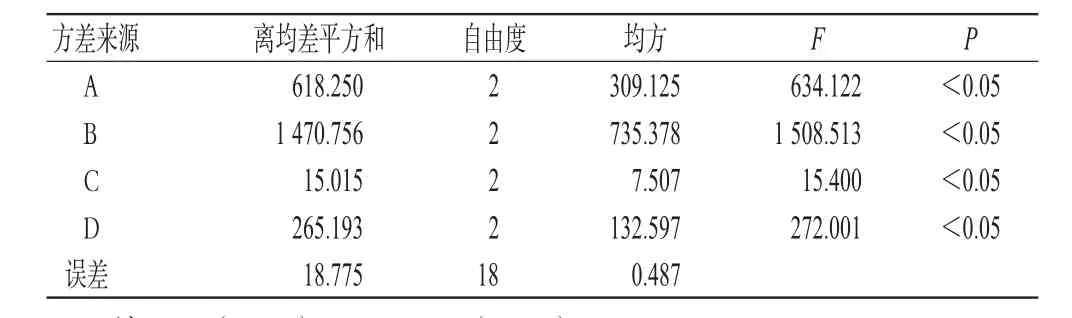
表3 方差分析结果Tab 3 Result of analysis of variance
3 讨论
在脂质体制备过程中,影响最终产品质量的因素较多[6],本文根据单因素考察,发现影响脂质体制备的主要因素有EPC和胆固醇含量、有机相与水相体积比、药物量和缓冲液pH值。在此基础上采用正交设计优化脂质体的制备工艺,充分考察了4个因素不同水平对药物包封率的影响,从数据处理的结果来看,优化的制备条件重现性好、包封率高、稳定性好。
[1] 胡国芬,王建平.川芎嗪的药理作用及临床应用进展[J].中国药物与临床,2006,6(10):773.
[2] 梁爱群.川芎嗪的药理及机理研究[J].时珍国医国药,2005,16(6):532.
[3] 刘永明,李桂芝,张 慧,等.盐酸川芎嗪的荧光光谱研究及应用[J].光谱实验室,2001,18(4):536.
[4] 赵荣生,侯新朴,严宝霞.脂质体载体材料卵磷脂的制备及质量标准研究[J].中国现代应用药学杂志,2001,18(1):39.
[5] 王闻珠.酮洛芬脂质体喷雾剂的研究[D].沈阳:沈阳药科大学,2001.
[6] 张俭俭,孙晓东.新型脂质体的应用研究进展[J].中国药房,2007,18(31):2465.
Optimization of the Preparation Technology of Ligustrazine Hydrochloride Liposome by Orthogonal Design
DU Zhao-xiang,JU Jian-feng(The Affiliated Hospital of Shandong University of Traditional Chinese Medicine,Jinan 250011,China)
OBJECTIVE:To optimize the preparation technology of ligustrazine hydrochloride liposome.METHODS:The liposomes were prepared by ether injection method.The preparation technology was optimized by orthogonal design with encapsulation coefficency as index using ratio of drugs to soybean lecithin,pH value of PBS buffer solution,ratio of cholesterol to soybean lecithin and ratio of diethyl ether to buffer solution as factors.RESULTS:The ideal preparation technology was as follows:drug∶soybean lecithin=1∶12,pH values of PBS was 7.5,cholestrol∶soybean lecithin=1∶2,diethyl ether∶PBS buffer solution=1∶2.CONCLUTION:The preparation technology is feasible,stable and reproducible and it serves as theoretic basis of industrial production.KEY WORDS Ligustrazine hydrochloride;Liposome;Orthogonal design;Preparation technology
R284.2;R283.69
A
1001-0408(2011)35-3303-02
*副主任药师。研究方向:药物制剂新技术。电话:0531-68617919。E-mail:tsunping@163.com
2011-06-15
2011-07-22)
