离子色谱法测定水产品中亚硫酸盐的含量
2011-10-21邵宏宏周向阳周秀锦傅谧妮徐君辉
邵宏宏,周向阳,周秀锦,傅谧妮,沈 飚,徐君辉
(舟山出入境检验检疫局,浙江舟山 316000)
亚硫酸盐作为食品添加剂广泛使用于食品加工工程中,能起到漂白、脱色、防腐、抗氧化、防止食物褐变等作用。水产品中二氧化硫超标问题一直是困扰水产品出口的疑难问题。产生二氧化硫的原因主要是渔民滥用亚硫酸盐保鲜剂,在使用方法上普遍存在操作随意、剂量不匀的现象,导致水产品中二氧化硫超标。但是,亚硫酸盐具有一定的毒性,可与蛋白质巯基进行可逆反应,刺激消化道黏膜,出现恶心、呕吐、腹泻等症状;摄入过量的亚硫酸盐,不仅会影响人体对钙的吸收,并破坏B族维生素;长期摄入则会对肝脏造成损害。因此对其使用量及在食品中的残留量应控制在合适的范围内。美国食品药品监督管理局(FDA)和欧盟规定,凡食品中亚硫酸盐含量超过10 mg/kg,必须在食品标签上注明本食品有亚硫酸盐。
目前,作为虾蟹类水产品的主要进口国,韩国对我国出口的甲壳类产品,主要是梭子蟹实施了严于国际要求的亚硫酸盐检测标准,把生、熟的梭子蟹制品均设定为30 mg/kg。我国目前采用的亚硫酸盐检测方法虽然有很多种[1-5],如国标中采用的盐酸副玫瑰苯胺比色法和蒸馏滴定法等,其他检测方法如化学发光法[10-12]、电化学法[13]、酶光度分析法[14]等检测方法也陆续有人报道,但均各有其不足之处。如盐酸副玫瑰苯胺比色法除需要大量使用有毒性的四氯汞钠之外,此方法定量限仅为10 mg/kg,且易受干扰。面对水产品出口的严峻形势,加强对水产品中亚硫酸盐残留检测成为当务之急。然而,目前采用的国标方法已经不能很好的满足检测需求。还缺少一种适应目前贸易需求的简单、环保、快速、准确度较高的检测方法。
离子色谱法是目前分析阴离子的首选方法,本文尝试建立离子色谱-抑制电导检测器测定水产品中的亚硫酸盐的方法,取代传统的盐酸副玫瑰苯胺比色法,此法将不需要有毒性的四氯汞钠作为提取剂,其检出浓度可达到0.1 mg/kg,且干扰小、稳定性好、操作简单,效率高,方法可满足出口检测的要求(<30 mg/kg),进一步做好水产品中亚硫酸盐的源头验收把关工作,更好的为地方经济的发展服务。
1 材料和方法
1.1 主要试剂与仪器
试剂除特别说明外均为分析纯,水为18.2 MΩ的去离子水,经0.45 μm滤膜过滤后使用。
SO32-标准储备液:称取Na2SO312.600 g,用少量水溶解,加入10 mL甲醛,加水定容至1 L,摇匀,冰箱储藏。临用时用硫代硫酸钠标准溶液标定SO32-(以SO2计)的含量。
超声波清洗器;漩涡振荡器(IKA 公司MSI);低温高速离心机(西格玛公司3-18K);0.22 μm微孔滤膜;Millipore超滤杯;戴安ICS3000离子色谱仪,配电导检测器;chromeleon色谱工作站。
1.2 样品预处理
称取约 5.0 g(精确至 0.001 g)样品,均质后,加入 50 mL 10 mM NaOH,2%甲醛溶液提取液,经充分混匀后超声10 min,然后以6 000 r/min离心10 min,取上清液20 mL于millipore超滤杯,9 000 r/min低温高速离心30 min,取滤液,经0.22 μm水相微孔滤膜过滤后,取1 mL滤液用1%甲醛溶液定容至5 mL,收集于自动进样器样品瓶中,待测。
1.3 色谱条件
分离柱:IonPac AS11-HC;保护柱 IonPac AG11-HC;淋洗液:20 mmol KOH 溶液,流速 1.0 mL/min,自动抑制模式,抑制电流125 mA;检测:抑制电导,进样量25 μL,以保留时间定性,峰面积定量;柱温:30℃。
2 结果与讨论
2.1 稳定剂的选择
亚硫酸盐不稳定,其水溶液极易水解/氧化,样品在前处理过程中以及标准溶液中必须加入稳定剂,根据有关资料[6-8],三乙醇胺、甘露醇和甲醛等均可作SO32-的稳定剂,其中甲醛最有效。本文选用甲醛作为稳定剂,经试验表明,随着甲醛浓度提高,会降低检测的灵敏度,样品和标准溶液的甲醛加入浓度为1%时,样品的回收率较好。
另外,亚硫酸盐在酸性条件下易分解,释放出SO2,SO32-在中性和碱性溶液中较稳定。根据资料[15],当提取溶液碱性过大时,SO32-峰面积会增大,但是与SO42-分离度变小,当溶液中OH-浓度为10~20 mmol/L较合适。为达到较好的分离度,因此我们选择10 mmol/L NaOH提取样品中的亚硫酸盐,并加入1%甲醛作为稳定剂。
2.2 样品前处理方法的对比试验
有些食品样品组成复杂,含有较多蛋白质油脂色素纤维素等成分,这些组分不仅会堵塞管道而且还直接作用于分离柱,影响柱的性能和寿命,因此我们尝试采用Kjeltec Auto Distillation Foss Tecator蒸馏法[5,9],通过加酸使SO32-转化为SO2,使亚硫酸盐以气体的形式蒸馏出来,碱溶液或沉淀剂吸收SO2,经固相萃取柱后,再用离子色谱法进行测定。同时蒸馏时加入过量的强酸和发泡剂碳酸钠,两者反应后产生CO2气体逸出,用CO2气体取代氮气将SO2气体带出,提高了蒸馏效率。这种前处理方式虽然能较好去除食品中所含的蛋白质油脂色度等成分,减少对测定的干扰,但是过量的强酸会使部分样品碳化,并且强酸具有较强的氧化性且反应较剧烈,其与发泡剂碳酸钠反应产生的过大的CO2气体反而会影响SO2气体的吸收,导致回收率不够理想。
鉴于水产品主要是虾仁和螃蟹,其主要成分是蛋白质,几乎不含色素等成份,因此我们前处理过程中,采用碱溶液并加入一定的亚硫酸盐稳定剂甲醛溶液来提取水产品中的亚硫酸盐,超声后,经冷冻离心,将上清液过Millipore超滤杯,在高速离心下,它可过滤掉3 kD大小以上的蛋白质,即可将样品净化完全。我们分别采用不同的超声时间和不同体积的提取液对样品进行预处理对比试验。试验表明,提取过程中,采用50 mL体积提取液是较为理想的提取体积,当提取液体积缩小到20 mL时,回收率下降5%。另外,采用50 mL提取液提取样品中的亚硫酸盐,分别用不同的超声时间对样品进行处理。随着超声时间的延长,回收率下降,当超声时间由10 min增加到40 min时,回收率下降10%,在相同条件下,样品超声10 min平均回收率均可达到85%以上。因此超声10 min即可基本上将样品中亚硫酸盐被提取液所溶解,超声时间的延长反而会因为超声时产生的热量影响亚硫酸盐的稳定性。
2.3 仪器系统的稳定性
2.3.1 色谱条件及色谱图
本实验使用20 mmol KOH溶液为淋洗液,可有效的将亚硫酸根与其它离子分开,亚硫酸盐标准溶液的离子色谱图如图1所示,空白样品和加入SO32-标准溶液的样品的色谱对比图如图2所示。根据本文的实验方法和色谱条件,SO32-保留时间在13.9 min左右,色谱峰峰形良好,可满足亚硫酸盐的检测分离要求。标准工作曲线和进样重复性试验表明,该系统仪器条件对于测定亚硫酸盐的含量是稳定的。
2.3.2 标准工作曲线
吸取SO2储备液0.5 mL于100 mL容量瓶中,加1%甲醛溶液定容到刻度,得到10.0 mg/L SO2标准使用液。再进一步用1%甲醛溶液稀释成SO2浓度分别为0.10、0.20、0.40、0.60、1.00、2.00、4.00、10.00、20.00、40.00 mg/L系列标准使用液。在设定色谱条件下进样分析,以标准系列质量浓度为横坐标,峰面积为纵坐标,绘制校准曲线。标准工作曲线方程为Y=0.468 8 X-0.052 3,线性相关系数为0.998 4,该方法线性关系良好,能够准确进行定量。
2.3.3 进样重复性和最低检出限
用浓度为 0.05 mg/L、0.1 mg/L、0.2 mg/L的SO2标准液,每个浓度重复进样,0.05mg/L时检测不到信号。在0.1 mg/L浓度时,测定结果的平均值为0.106 3 mg/L,相对标准偏差为4.1%,重复性较好,见表1。并且S/N≥3,因而0.1 mg/L为本方法的最低检出限。
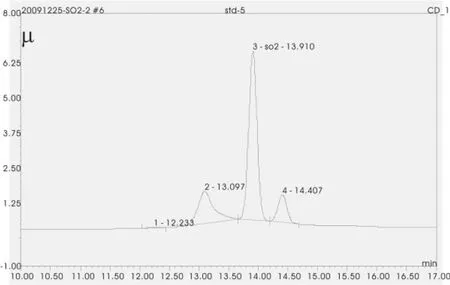
图1 SO32-标准溶液色谱图Fig.1 Chromatogram of sulphite standard by IC
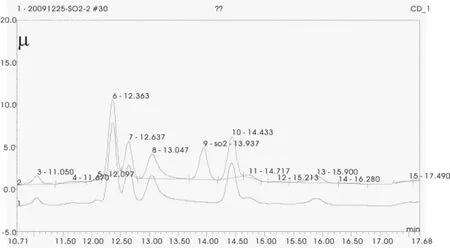
图2 空白样品和加标后样品SO32-的色谱对比图(1为空白样品的色谱图;2为空白加标的色谱图)Fig.2 Chromatogram of blank and spiked sample by IC

表1 最低检出限试验Tab.1 Results of detection limit test
2.4 定量限试验
准确称取虾仁空白样品5.0 g,分别加入不同浓度的标准溶液,当SO2加标浓度最低为4.4 mg/kg时,信噪比S/N≥10,做6个平行,测定结果见表2。回收率在86.6%~99.7%之间,RSD=5.2%,结果满意。根据回收率试验,能可靠测得的最低浓度确定定量限为4.5 mg/kg。
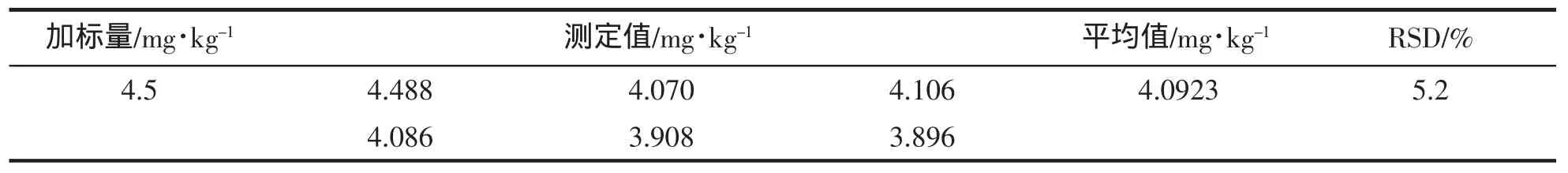
表2 定量限试验Tab.2 Results of determination limit test
2.5 精密度试验
分别准确称取2组各6个虾仁空白样品5.0 g,两组分别加入不同浓度的标准溶液,经过同样的样品前处理上机检测,结果见表3。由表3可知,测定结果的标准偏差分别为3.6%和6.6%,结果满意。表明该方法满足残留测定的要求。

表3 精密度试验结果(n=6)Tab.3 Results of precision of the method from fortified samples(n=6)
2.6 回收试验
按本文方法对已知含量的空白样品进行标准加入回收试验,测定结果和回收率计算结果见表4。由表4可知,此方法的平均加标回收率为85.4%~93.5%,回收率较好。
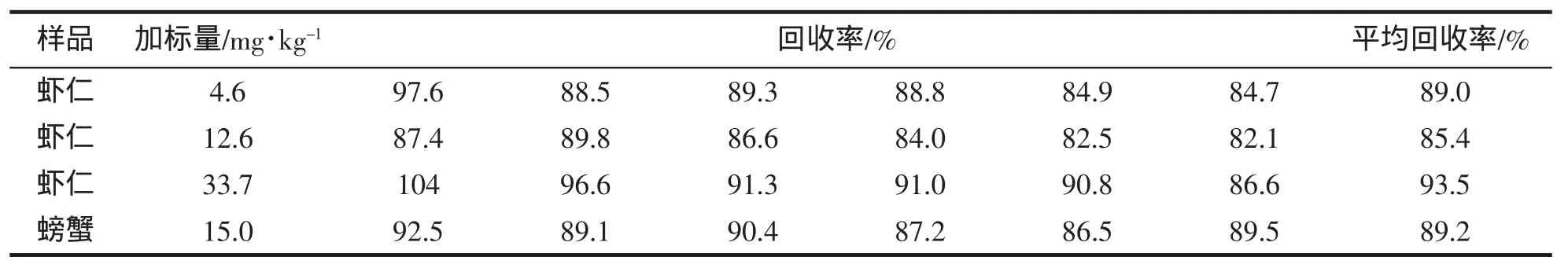
表4 方法回收率试验(n=6)Tab.4 Results of recovery test from fortified samples(n=6)
2.7 比对试验
为进一步验证方法的准确性,本文采用的离子色谱法(IC法)与我国食品卫生标准检验方法[5]:盐酸副玫瑰苯胺紫外分光光度法分别对虾仁和螃蟹样品进行对比测定。紫外分光光度法定量限为10 mg/kg,测定结果见表5。
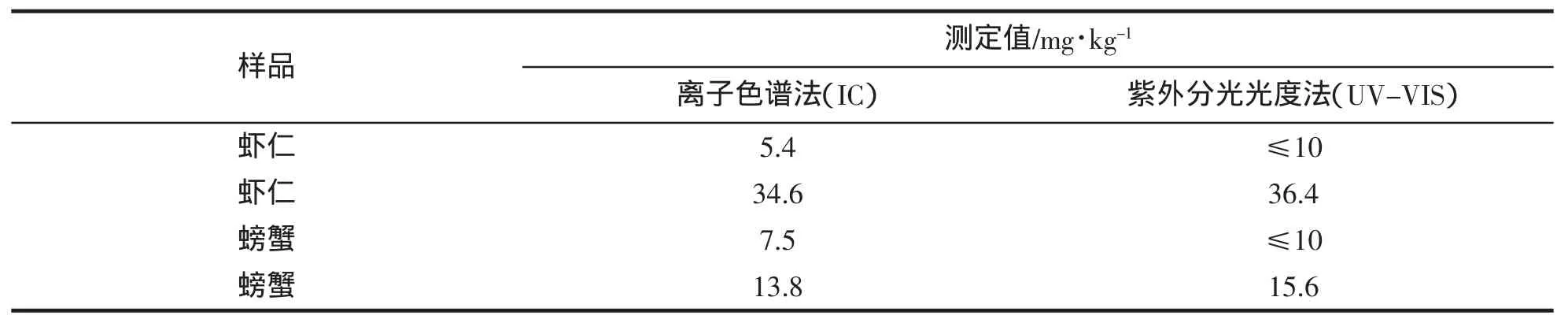
表5 方法比对试验Tab.5 Results of comparative test between IC and UV-VIS method
由表5可知,用本文的离子色谱法和紫外分光光度法对水产品中的亚硫酸盐含量进行检测,两种方法的结果具有较好的一致性。但在低浓度检测时,离子色谱法灵敏度比传统的分光光度法高。
3 结论
采用离子色谱法可简便、快速、准确测定水产品主要是虾仁和螃蟹中的亚硫酸盐含量,不仅减少了传统国标法中使用有毒试剂对操作人员健康的危害和对环境的影响,并且提高了检测的灵敏度,为出口水产品的检测提供技术支持,保障水产品中亚硫酸盐的源头验收把关工作,更好的为地方经济的发展服务。
[1]陈青川,牟世芬.离子色谱法在食品分析中的最新应用[J].色谱,2000,18(2):120-124.
[2]范华峰,查河霞.离子色谱法测定食品中亚硫酸盐的方法探讨[J].中国卫生杂志,2001,11(6):727-731.
[3]吴风武,何治柯,罗庆尧.二氧化硫分析研究进展[J].分析科学学报,2000,16(3):248-252.
[4]李丽丽.离子色谱法测定沸腾炉尾气中的二氧化硫[J].珠冶科技,2000,28(2):47-51.
[5]GB/T 5009.34-2003食品中亚硫酸盐的测定[S].北京:中国标准出版社,2003.
[6]牟世芬,刘克纳.离子色谱方法及应用[M].北京:化学工业出版社,2000:55-58.
[7]VILLASENOR S R.[J].Anal Chem,1991,63:1 362-1 366.
[8]瞿国栋,张金锐.离子色谱法测定催化裂化再生烟气中的酸性组分[C]//第六届全国离子色谱学术报告论文集.1997:35-36.
[9]杨一超,许春斌.离子色谱法测定食品中总二氧化硫含量[J].中国卫生检验杂志,2004,14(4):463-464.
[10]PALLS D A,TOWNSHEND A.Enhancement by cycloalkanes of the chemiluminnescent oxidation of sulfite[J].Analyst,1996,121:831-834.
[11]BALASUBRAMANIAN N,KUMARB S M.Extration-Spectrophotometric of Sulphur Dioxide[J].Analyst,1991,116(2):207-212.
[12]MARQUES E P.Sepectrometric Determination of sulphite based on the calaytic oxidation of hydrongen sulphite[J].Analyst,1990,1 115(6):795-797.
[13]王丽丽,纪淑娟,李 顺.食品中二氧化硫及亚硫酸盐的作用与检测方法[J],食品与药品,2007,9(2A):64-66.
[14]狄俊伟,孟良辛.酶光度分析法测定痕量亚硫酸盐[J],苏州大学学报:自然科学版,2000,16(3):68-71.
[15]钟志雄,梁春穗,杜达安.离子交换色谱-电导检测法测定食品中的亚硫酸盐[C]//第九届全国离子色谱学术报告会论文集.2002:55-59.
