SPECT/CT断层融合显像在分化型甲状腺癌131I治疗后的应用价值
2011-09-29宋长祥
刘 永,宋长祥,陆 武,杜 鹏
(连云港市第一人民医院核医学科,江苏 连云港 222002)
分化型甲状腺癌(Differentiated thyroid carcinoma,DTC)包括乳头状甲状腺癌和滤泡状甲状腺癌,约占甲状腺恶性肿瘤的94%。常规影像学检查包括超声、CT、99mTcO4-甲状腺显像、131I全身显像(I-WBS)等,其检查价值各有优劣。对于DTC术后患者在行131I治疗后,131I显像可以了解有无局部及远处转移灶、转移灶部位、判断疗效和指导下一步治疗计划。131I平面显像对病灶精确定位较为困难,且分辨率受到一定限制。随着SPECT/CT临床应用的开展,SPECT/CT断层显像及解剖显像融合逐渐应用于DTC术后转移灶的检查。本研究应用SPECT/CT对分化型甲状腺癌131I治疗后进行平面及断层显像,结果与病理等其他检查对比,旨在评价SPECT/CT断层融合显像在分化型甲状腺癌131I治疗后转移灶诊断的临床应用价值。
1 资料与方法
1.1 一般资料 2008年1月至2011年6月我院收治的DTC术后患者49例,男15例,女34例;年龄28~74岁,中位数年龄44.3岁。其中41例病理组织学为甲状腺乳头状癌,8例为甲状腺滤泡状癌。患者均在停服甲状腺素片或优甲乐2~4周、促甲状腺激素(TSH)均大于30 IU/L以上进行131I治疗,治疗剂量3.7~7.4 GBq。
1.2 检测仪器及参数131I由成都中核高通同位素公司提供。显像装置为GE公司生产的可变角双探头符合线路Infinia Hawkeye型SPECT/CT成像系统。所有患者均在口服131I治疗后5~7 d行全身平面及颈胸部或其他可疑部位断层显像检查。平面显像采用能峰364 KeV,窗宽20%、矩阵256×1 024,扫描速度10 cm/min,ZOOM:1.0。断层显像先行透射扫描随后行发射扫描。CT电压140 kV,电流2.5 mA;SPECT显像的矩阵为128×128,旋转360°,6°/帧,每帧30 s。采集后的图像用迭代法重建,获得横断面、矢状面和冠状面断层图像,再将获得的SPECT和CT图像经计算机软件进行图像融合。
1.3 图像分析 由3名固定的核医学科医师共同分析图像。平面显像除鼻咽、残甲、唾液腺、消化道、膀胱和弥漫性肝脏显影外,其他高于本底的放射性浓聚灶判为异常。SPECT/CT图像除上述排除标准外,尚需结合CT解剖图像定位进一步判读。诊断为异常的结果分别与金标准(病理或其他影像检查加临床随访)对照分析。
1.4 统计学处理 全部资料采用SPSS13.0软件分析,结果比较采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 两种显像方法定位诊断结果对比 平面显像所示放射性浓聚灶,根据其所在平面位置,只能大致判断位于颈部甲状腺床或胸、腹部等处;断层显像融合CT图像能够较准确地判断转移灶的部位、范围和数目,比如确定放射性浓聚灶位于甲状腺残留组织抑或颈部淋巴结,位于肺部某肺叶或纵隔淋巴结等;并能够容易地确定位于体表的污染灶(图1~图3)。
2.2 两种显像方法定性诊断准确率对比 以病理或其他影像检查加临床随访(6个月以上)结果为诊断金标准,49例DTC患者术后各部位转移灶共46处。平面显像诊断转移灶40处,其中真阳性35处,其灵敏度、准确率分别为76.09%(35/46)、68.63%(35/51)。断层显像诊断转移灶45处,其中真阳性43处,其灵敏度、准确率分别为93.48%(43/46)、89.58%(43/48)。断层显像诊断准确率高于平面显像,差异有统计学意义(χ2=6.4975,P=0.0112)(表1)。
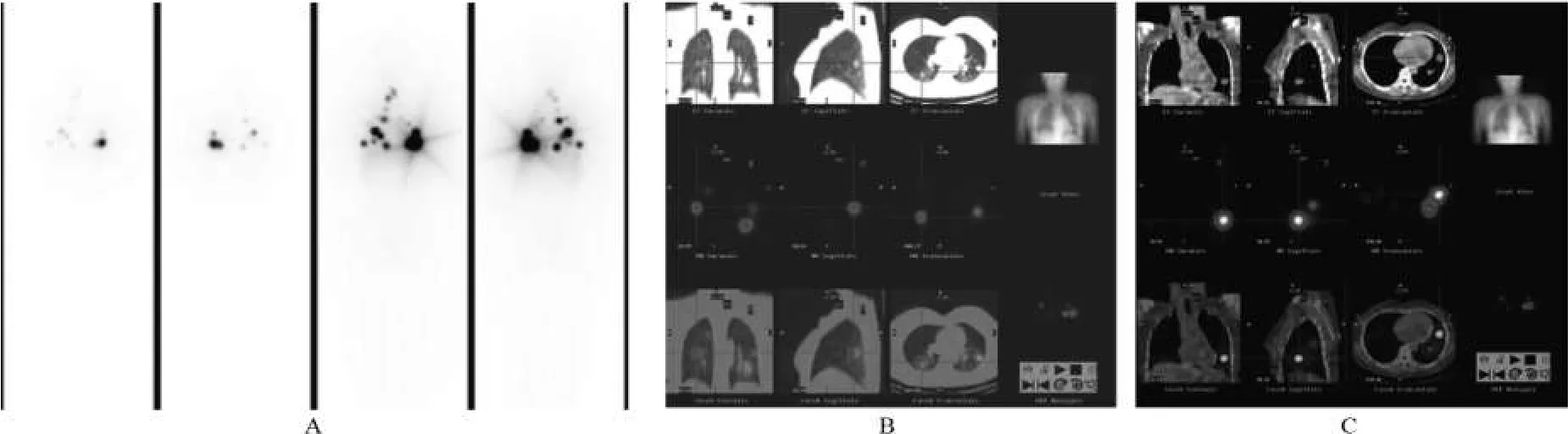
图1 同一女患者两种显像方法定位图示
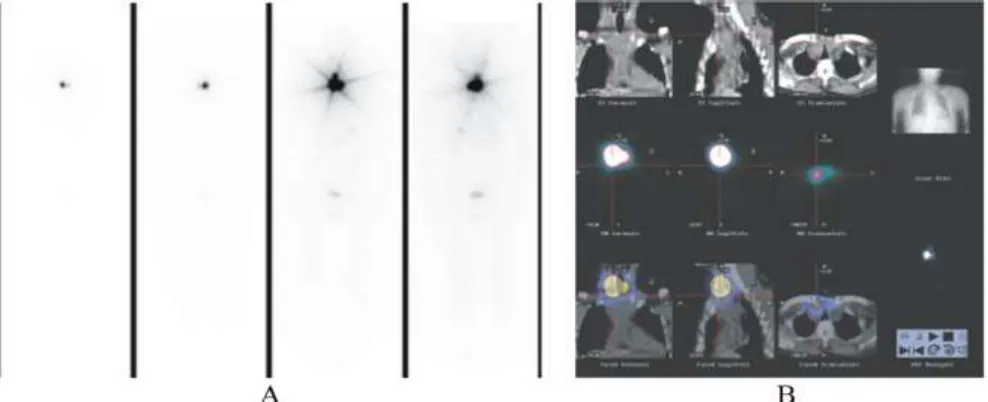
图2 同一女患者两种显像方法定位图示
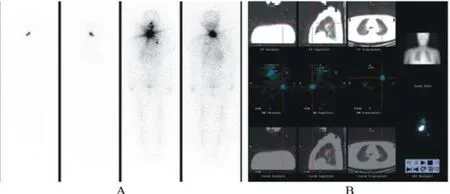
图3 同一男患者两种显像方法定位图示

表1 两种显像方法定性诊断准确率对比
3 讨 论
DTC的治疗除手术全切、淋巴结清扫以外,一般辅以131I治疗以清除甲状腺残留组织并治疗转移灶,在临床已经普遍成熟应用[1]。与其他绝大部分恶性肿瘤相比,DTC预后较好,但治疗后仍需要随访观察;在DTC行131I治疗后通常进行全身显像以确定甲状腺组织残留、转移灶的部位、数目及摄碘情况,从而对治疗方案进行评价和调整。
传统ECT平面显像由于分辨率较低,不易发现较小的甲状腺癌转移灶,更不能精确定位,从而大大降低了对甲状腺癌术后寻找转移灶的诊断价值。CT可进行准确定位病灶,但对于<1 cm的淋巴结却难以区分正常抑或为转移,也很难区分肿瘤复发与术后瘢痕、纤维组织增生等解剖结构的改变,不能发现无实体瘤的转移灶[2]。而SPECT/CT融合显像可以利用X线对核医学图像进行衰减校正,使融合后的图像既有精确的解剖结构,又有血流代谢等功能信息,为甲状腺癌及其转移灶的精确定位定性提供可靠的依据。
本研究选择病例均为大剂量131I治疗后的患者,在131I全身显像的基础上加上SPECT/CT断层图像融合。除了能够提供转移灶摄碘情况,还能够对病灶进行解剖定位,提高空间分辨力;对131I治疗后全身显像可疑阳性病灶但难以进行病灶定性及解剖定位者,具有明显的优势[3-6]。另外还能够排除污染引起的假阳性,提高对DTC的诊断能力。
平面显像假阳性与假阴性较高,主要与定位不精确及分辨率限制相关。本研究中有些病例因平面显像的固有缺陷认为正常,断层融合显像发现淋巴结转移灶(图2);有些病例疑为转移灶却被断层显像明确为污染(图3)。SPECT/CT断层融合显像大大提高了准确率,但不可避免仍有一定假阳性与假阴性。结合本研究病例分析考虑其原因与定位CT及核素显像分辨率有关,病灶太小造成漏诊或者颈部部分淋巴结与残余甲状腺组织分辨不清。
总之,SPECT/CT断层显像与同机CT图像融合技术对DTC术后131I治疗后的患者,可以明确诊断其残余病灶、转移和复发,同时为再次治疗提供依据。和单纯平面显像相比,该法大大克服了其局限性;对DTC术后131I治疗后患者有无复发及转移的全面评价及指导治疗方案具有重要的应用价值。
[1]Derey T,Paul G.Role of131I in the treatment of well differentiated thyroid cancer[J].Gury Oncol,2005,89:114-121.
[2]Akoglu E,Dutipek M,Bekis R,et al.Assessment of cervical lymph node metastasis with different imaging methods in patients with head and neck squamous cell carcinoma[J].J Otolaryngol,2005,34(6):384-394.
[3]陈立波,罗全勇,余永利,等.分化型甲状腺癌患者的131I-SPECT/CT断层融合显像[J].中国医学影像技术,2004,20(7):1111-1113.
[4]Angela S,Maria E,Francesca C,et al.131I SPECT/CT in the follow-up of differentiated thyroid carcinoma:incremental value versus planar imaging[J].J Nuc Med,2009,50(2):184-190.
[5]郭一玲,陈佐伟,张英男,等.131I-SPECT/CT融合显像对分化型甲状腺癌术后诊断临床价值分析[J].现代肿瘤医学,2009,17(12):2297-2298.
[6]栾兆声,周 雯,唐为国,等.131I-SPECT/CT断层融合显像在分化型甲状腺癌中的临床价值[J].中国医学影像学杂志,2010,18(1):86-88.
