局限性肺磨玻璃密度影的高分辨CT表现及病理(附32例报告)
2011-07-13栾杰
栾 杰
(咸宁市第一人民医院放射科,湖北 咸宁 437000)
局限性肺磨玻璃密度影(ground-glass opacity,GGO)表现为肺密度轻度增高,但低于肺血管和支气管壁,是一种非特异性 CT征象[1]。笔者回顾分析2002年至2010年我院行CT检查,32例表现为局限性GGO的患者在高分辨率CT(HRCT)上的表现,以探讨此征象的病理基础,提高临床对局限性GGO的认识,现报告如下。
1 材料与方法
本组患者男22例,女10例。年龄35~70岁。病人先作常规CT扫描,层厚10mm,层间距10mm,仰卧位吸气末扫描。CT机为 GE16层,HRCT 扫描参数为层厚 2.0mm,130kV,200mAs,骨重建,重建视野(FOV)300mm。窗宽1600HU,窗位-600HU。观察每例磨玻璃密度出现的部位、密度、边缘。病变主要分布在外带者为外周分布,中内带分布者为中央分布。GGO分为单纯GGO和混合型GGO,单纯GGO在HRCT上表现为除了血管及支气管影外,病灶密度均匀,混合型GGO在HRCT上表现为磨玻璃影内软组织结节影。
2 结果
32例单发局限性GGO中,肺腺癌16例,7例细支气管肺泡癌,4例非特异性炎症,3例局限性纤维化,1例腺上皮增生,1例非典型性腺瘤样增生。32例GGO在HRCT表现位置、类型及边缘见表1。HRCT表现为纯磨玻璃影(pure ground-glass opacity,pGGO)和混合型(mixed ground-glass opacity,mGGO),pGGO 13 例,表现为密度均匀,边缘模糊,呈多边形,与邻近胸膜之间可见长索条影,邻近胸膜凹陷及增厚:其中局灶性纤维化3例,腺上皮增生1例,非特异性炎症4例,非典型腺瘤样增生 1例,肺泡癌 4例。mGGO19例在HRCT上表现为磨玻璃影中软组织结节影,16例腺癌及3例细支气管肺泡癌表现为mGGO。32例中15例穿刺活检证实,14例手术病理证实,3例临床确诊。
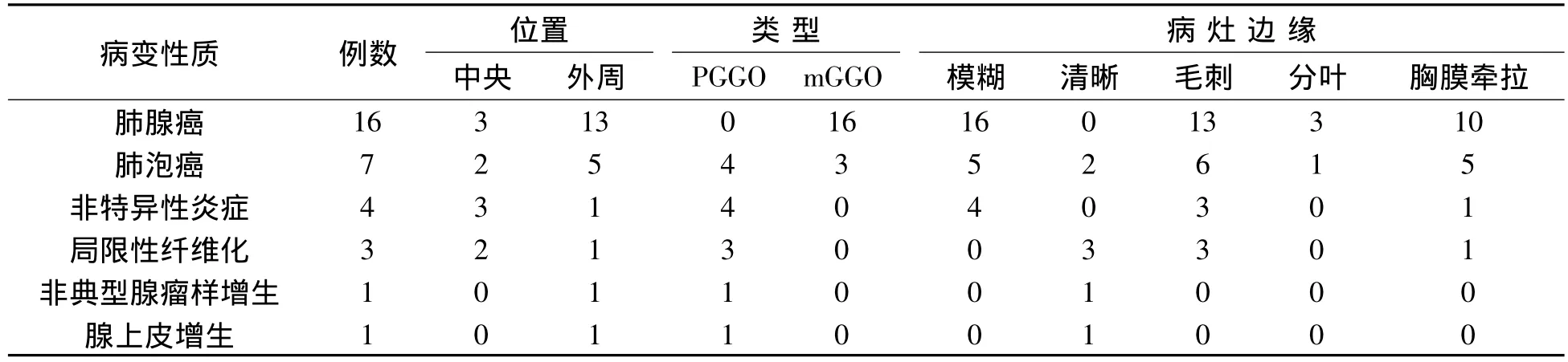
表1 32例GGO在HRCT表现的位置、类型及边缘
3 讨论
3.1 肺磨玻璃密度的定义及特征
肺磨玻璃密度表现为肺密度轻度增高,它可见于各类疾病,该征象对于疾病的诊断特征性不明显。在分析GGO时,它只在肺窗显示,纵隔窗无法显示。在常规CT扫描时由于吸气不足,正常肺组织可以显示出磨玻璃样密度,尤以坠积部位明显,但改变体位扫描可以消除。同时肺野内某些密度较低的小结节,由于容积效应可以呈磨玻璃密度影,但是并非实际意义上的磨玻璃密度。本组病例均在常规CT的基础上再行高分辨CT扫描,我们认为判断肺磨玻璃密度影必需在HRCT 扫描的条件下进行[2],结合文献[3,4]判断GGO应满足以下条件:①肺内病灶密度轻度升高;②病灶密度低于肺血管密度;③薄层(2mm以下)扫描和骨重建;④深吸气末扫描增加肺与病灶的对比;⑤采用窗宽1500~2000HU、窗位-500~-700HU观察。
3.2 局限性磨玻璃影的病理基础
肺GGO反映了肺气腔的不完全填充,局限性磨玻璃影可以是多种疾病的早期阶段,若长时间存在则多为肺纤维化或肿瘤病变。肿瘤所致的局限性GGO,病理改变为肿瘤细胞沿肺泡壁生长,无或部分肺泡塌陷,有残留的含气肺泡组织,肿瘤内弹性纤维轻、中度增生在以间质为主的病变中,磨玻璃密度是间质纤维化形成和(或)肺泡炎的表现,由于分辨率有限,HRCT不能区分肺泡炎和肺泡壁的间质纤维化。所以临床上碰到此类患者,均建议先抗炎后复查,本组病例中有3例GGO患者抗炎后病灶完全吸收。纤维化病变病理为肺泡萎陷和纤维增生,同时可见肺泡间隔纤维性增厚。对于肿瘤性病变及局限性纤维化,必须采用肺穿刺活检或手术才能确诊。而肺通气血流障碍性疾病也可表现GGO,病理改变为肺血流量增加,病变区动静脉血管增粗。随着病变的进展或转归,磨玻璃影可以完全消失,或者发展成为网状、蜂窝状阴影等,因此,HRCT上表现为GGO的一类疾病,其病理表现复杂。
3.3 GGO的部位与边缘
本组病例中GGO在肺内的发生部位与定性诊断,由于本组病例数有限,且以恶性病变为主,恶性病变约占78.1%(25/32),良恶性病灶在肺内的发生位置没有明显的特征性,所以根据病灶的位置判断GGO的良恶性价值不大。GGO由于密度较低,与正常肺组织对比不大,恶性肿瘤与炎症其边缘一般与正常肺组织分界不清,部分肺泡癌的GGO边缘清晰,其它良性病变如局限性纤维化、非典型腺瘤样增生、腺上皮增生边界清晰。毛刺和分叶多见于腺癌,位于外周紧邻胸膜的腺癌易形成胸膜牵拉及胸膜凹陷。外周肺腺癌胸膜牵拉发生率约76.9%(10/13);腺上皮增生及非典型腺瘤样增生分叶、毛刺不常见。局限性纤维化由于纤维化形成其病灶边缘可见毛刺,非特异性炎症的毛刺比较粗大、长,与腺癌的不同,但是在腺癌合并炎症时,需综合判断,位于胸膜下炎症可以累及胸膜导致胸膜增厚。非典型腺瘤样增生一般认为是癌前病变,故临床还是要积极处理。腺上皮增生良性病变,其在CT上表现为局限性GGO,与肺泡癌及非典型腺瘤样增生鉴别困难,需借助于病理。
3.4 GGO的类型对其定性诊断的价值
根据HRCT的特征,GGO分为pGGO与mGGO。文献报道pGGO与mGGO是病变发展的不同阶段,病灶早期主要表现为pGGO,随着病变的发展,恶性病灶内细胞数目增加,肺泡含气量减少,导致病灶密度增加而表现为软组织结节影。本组19例mGGO病理均为恶性病变,因此,mGGO对恶性病变的阳性预测值为100%,临床上mGGO对于良恶性病变鉴别诊断具有非常重要的价值。文献报道,mGGO软组织成分与磨玻璃成分的比例不同其预后也不同,目前比较一致的观点认为,pGGO是mGGO的早期阶段[5]。由于本组病例数有限,故没有对此展开讨论。pGGO既可见于良性病变,也可见于肺泡癌,临床上难以确定pGGO的良恶性时,一般建议抗炎复查,随访中发现pGGO出现软组织成分体积增大,则临床高度怀疑腺癌,并主张积极手术治疗[6]。
总之,单发GGO在CT上是非特异性的影像学征象,它不仅仅见于细支气管肺泡癌和肺腺癌,还可见于非典型腺瘤样增生、局限性纤维化、非典型肺炎、腺上皮增生等多种良性疾病,不同疾病其病理表现不同,但它们的共同点是,病变组织并没有完全取代肺泡组织,肺泡内含有气体。
[1]Wallace T,Miller J,Rosita MS.Isolated diffuse groundglass opacity in Thoracic CT:Causes and Clinical Presentations[J].AJR,2005,184:613
[2]Tsubamoto M,Kuriyama K,Kido S,et al.Detection of lung cancer on chest radiographs:analysis on the basis of size and extent of ground-glass opacity at t hin-section CT[J].Radiology,2002,224(1):139
[3]贺文,马大庆,冯捷,等.肺磨玻璃密度高分辨率CT的诊断和鉴别诊断意义[J].中华放射学杂志,2001,35(1):52
[4]Chang MP,Jin MG,Hyun JL,et al.Nodular ground-glass opacity at thin-section CT:histologic correlation and evaluation of change at follow-up[J].Radio Graphics,2007,27(2):391
[5]Nakajima R,Yokose T,Kakinuma R,et al.Localized pure ground-glass opacity on high-resolution CT:Histologic characteristics[J].J Comput Assist Tomogr,2002,26(3):323
[6]Shan Y,Yuan HS,Guan LJ,et al.Investigation of highresolution CT findings in bronchioloalveolar carcinoma[J].Chin J Med Imaging Technol,2002,18(12):1250
