离子色谱法测定牛黄上清丸中二氧化硫残留量*
2011-06-02乔蓉霞杨瑞瑞刘海静袁向辉
乔蓉霞,杨瑞瑞,刘海静,袁向辉
(1.陕西省食品药品检验所,陕西 西安 710061;2.陕西中医学院,陕西 咸阳 712046)
牛黄上清丸是传统中成药,具有清热泻火、散风止痛的功效,主要用于热毒内盛、风火上攻所致头痛眩晕、目赤耳鸣、咽喉肿痛、口舌生疮、牙龈肿痛、大便燥结等证,由人工牛黄、薄荷、菊花、荆芥穗、白芷、黄连、黄芩、黄柏、川芎、栀子、大黄、连翘、赤芍、当归、地黄、桔梗、甘草、石膏、冰片加工而成[1]。2010年版《中国药典(一部)》附录以蒸馏法作为二氧化硫残留量的测定方法。笔者建立了测定牛黄上清丸中二氧化硫残留量的离子色谱法,现报道如下。
1 仪器与试药
Dionex ICS-1100型离子色谱仪;电导检测器;万能粉碎机;水蒸气蒸馏装置;超纯水系统(TTL-10B)。氢氧化钾、亚硫酸钠、乙二胺四乙酸、硫代硫酸钠、碘、淀粉均为分析纯;实验用水均为电阻率为18.2 MΩ·cm的去离子水;硫酸盐标准溶液购自国家标准物质中心(编号为 0942,标示值为 1 000 μg/mL)。
2 方法与结果
2.1 色谱条件
色谱柱:AS-11-HC阴离子分析柱(250 mm×4 mm),保护柱为AG-11-HC(50 mm×4 mm);淋洗液:20 mmol/L氢氧化钾溶液,等度淋洗;流速:1.0 mL/min;进样量:25 μL 。
2.2 溶液制备
取硫酸盐标准溶液,用去离子水逐级稀释成质量浓度分别为500,300,200,150,100,50,30,20,10,5,3,2,1,0.5,0.3,0.2,0.1 μg/mL的溶液,作为对照品溶液。取牛黄上清丸(大蜜丸,约6 g)1粒,剪碎,精密称定,置水蒸气蒸馏装置的样品瓶中,加水20 mL润湿,使其分散,在100 mL量瓶中加入3%的双氧水20 mL作为接收液,吸取盐酸5 mL快速加入样品瓶,立即密封,进行水蒸气蒸馏;至接收瓶中液体接近100 mL时,停止蒸馏,取下接收瓶;用去离子水稀释至刻度,摇匀,作为供试品溶液。
2.3 方法学考察
专属性试验:用牛黄上清丸组方中含有的菊花(未熏硫)作阴性对照,按供试品溶液制备方法同法制成阴性对照品溶液,依法测定。由图1可见,没有经过硫磺薰制的菊花中未检出二氧化硫。

图1 离子色谱图
线性关系考察:将2.2项下不同质量浓度的对照品溶液分别进样25 μL,以峰面积和进样量绘制标准曲线。结果表明,硫酸根进样量在0.1~500 μg范围内与峰面积线性关系良好,r=0.999 9。
精密度试验:取已制备好的同一对照品溶液,平行进样6次。结果峰面积分别为 453.7,473.2,456.9,479.6,451.1,456.8,RSD 为2.58%(n=6),表明仪器精密度良好。
稳定性试验:取已制备好的同一供试品溶液,分别于0,2,4,8,12,24 h 时进样。结果峰面积分别为 438.3,449.0,435.7,449.2,457.6,450.2,RSD为1.83%(n=6),表明供试品溶液24 h内稳定性良好。
重复性试验:取同一批牛黄上清丸,依法平行制备6份供试品溶液并测定。结果样品中二氧化硫平均含量为24.18 μg/g,RSD为4.51%(n=6),表明方法重复性较好。
加样回收试验:精密称定无水亚硫酸钠,以0.05%乙二胺四乙酸溶解,临用前用碘量法标定[2],以二氧化硫计质量浓度为0.474 0 g/L。取牛黄上清丸1粒(约6 g),精密称定,用滴定管分别精密加入亚硫酸钠对照品溶液0.4,1.2,6.0 mL,按供试品溶液的制备与测定方法每个质量浓度平行操作3份,计算回收率。结果见表1。
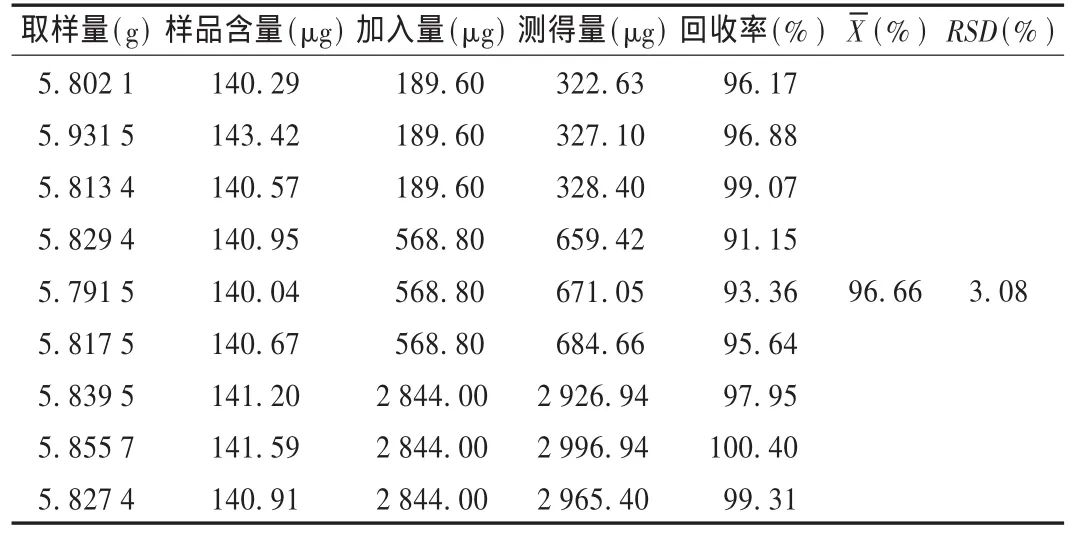
表1 加样回收试验结果(n=9)
2.4 样品含量测定
取6批样品,依法检测其中二氧化硫残留量。结果批号为1002114,90603,90603,15057,15060,7015101 的 6 批样品中,二氧化硫残留量分别为 32,37,11,24,14,8 mg/kg,RSD 分别为 1.3%,0.9% ,1.3%,1.2% ,0.7%,1.0% 。
3 讨论
牛黄上清丸的生产工艺是将方中饮片粉末研细、过筛、混匀后加炼蜜制成,其中甘草、当归、菊花、白芷、桔梗等中药饮片在传统加工过程中常采用硫磺熏蒸以达到洁白、防虫、防霉的效果,导致这些饮片中残留有二氧化硫。而牛黄上清丸是以饮片粉末直接投料制成的,硫磺熏蒸过的饮片会将残留的二氧化硫带入到制剂中。二氧化硫多以结合态的亚硫酸盐存在,亚硫酸盐具有一定的毒性,可与蛋白质的巯基发生可逆反应,刺激消化道黏膜,服用后会出现恶心、呕吐、腹泻等症状,进而导致免疫力下降;过量摄入亚硫酸盐,会影响人体对钙的吸收,并破坏B族维生素;长期摄入则会对肝脏造成损害[3]。目前,亚硫酸盐的安全性问题已引起广泛关注,因此各国纷纷限定食品和药品中二氧化硫和亚硫酸盐的残留量。目前我国食品卫生标准对食品中亚硫酸盐的允许量(GB 2706-1996)和检测方法(GB/T 5009.34-1996)均作出了规定[4]。
加样回收试验时,将硫酸根与亚硫酸根的量均折算成二氧化硫后计算;试验用水必须为电导率大于18 MΩ的超纯水,样品瓶及容量瓶都必须用超纯水荡洗;水蒸气蒸馏法对样品进行提取时,应注意密封。所建立的方法操作简便快速、干扰少、易于掌握,测定的精密度较好。
[1]国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2010:554.
[2]国家药典委员会.中华人民共和国药典(二部)[M].北京:化学工业出版社,2005:894.
[3]陈飞东,戴志远.食品中亚硫酸盐测定方法的研究进展[J].食品研究与开发,2006,27(8):139-142.
[4]钟志雄,梁春穗,杜达安,等.离子色谱法测定食品中亚硫酸盐的应用研究[J].中国卫生检验杂志,2003,13(1):29-32.
